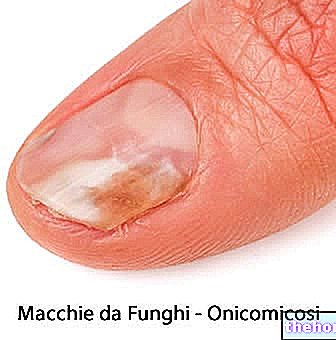
Definicja
Enzymy to białka wytwarzane w komórkach roślinnych i zwierzęcych, które działają jak katalizatory przyspieszające reakcje biologiczne bez modyfikacji.
Enzymy działają poprzez łączenie się z określoną substancją, aby przekształcić ją w inną substancję; klasycznymi przykładami są enzymy trawienne obecne w ślinie, żołądku, trzustce i jelicie cienkim, które pełnią istotną funkcję w trawieniu i pomagają rozkładać pokarm na podstawowe składniki, które mogą być następnie wchłonięte i wykorzystane przez organizm, przetwarzane przez inne enzymy lub wydalane jako odpady.
Każdy enzym ma określoną rolę: ten, który na przykład rozkłada tłuszcze, nie działa na białka ani węglowodany. Enzymy są niezbędne dla dobrego samopoczucia organizmu.Niedobór nawet pojedynczego enzymu może powodować poważne zaburzenia.Dobrze znanym przykładem jest fenyloketonuria (PKU), choroba charakteryzująca się niezdolnością do metabolizowania niezbędnego aminokwasu, fenyloalanina, której nagromadzenie może powodować deformacje fizyczne i choroby psychiczne.
Badanie biochemiczne
Enzymy to szczególne białka, które mają właściwość bycia katalizatorami biologicznymi, to znaczy mają zdolność rozkładania energii aktywacji (Eatt) reakcji, modyfikując jej ścieżkę tak, aby kinetycznie powolny proces był szybszy.
Enzymy zwiększają kinetykę możliwych termodynamicznie reakcji i, w przeciwieństwie do katalizatorów, są mniej lub bardziej specyficzne: dlatego posiadają specyficzność substratową.
Enzym nie bierze udziału w stechiometrii reakcji: aby tak się stało, końcowe miejsce katalityczne musi być identyczne z wyjściowym.
W działaniu katalitycznym prawie zawsze występuje faza powolna, która determinuje szybkość procesu.
Kiedy mówimy o enzymach, nie jest właściwe mówienie o reakcjach równowagi, zamiast tego mówimy o stan stabilny (stan, w którym pewien metabolit jest wytwarzany i konsumowany w sposób ciągły, utrzymując jego stężenie prawie na stałym poziomie w czasie). Produkt reakcji katalizowanej przez jeden enzym zwykle sam jest reagentem dla kolejnej reakcji, katalizowanej przez inny enzym i tak dalej.
Procesy katalizowane przez enzymy zazwyczaj składają się z sekwencji reakcji.
Ogólną reakcję katalizowaną przez enzym (E) można podsumować w następujący sposób:

E to enzym
S jest substratem;
ES reprezentuje addukt między enzymem a substratem;
P jest produktem;
K jest stałą szybkości reakcji.
Enzym generyczny (E) łączy się z substratem (S) tworząc addukt (ES) o stałej szybkości K1; może zdysocjować z powrotem do E + S o stałej szybkości K2 lub (jeśli "żyje" wystarczająco długo ) może przejść do postaci P ze stałą prędkości K3.
Produkt (P) może z kolei rekombinować z enzymem i reformować addukt ze stałą szybkości K4.
Kiedy enzym i substrat są zmieszane, jest ułamek czasu, w którym spotkanie między tymi dwoma gatunkami jeszcze nie nastąpiło: to znaczy, jest bardzo krótki odstęp czasu (który zależy od reakcji), w którym enzym i substrat mają jeszcze nie spełnione, po tym okresie enzym i substrat stykają się w coraz większych ilościach i powstaje addukt ES. Następnie enzym oddziałuje na substrat i uwalnia się produkt. Można wtedy powiedzieć, że c” jest początkowym przedziałem czasu, w którym nie można określić stężenia adduktu ES; po tym okresie przyjmuje się, że stan ustalony to znaczy, że szybkość procesów prowadzących do uzyskania adduktu jest równa szybkości procesów prowadzących do zniszczenia adduktu.
Stała Michaelisa-Mentena (KM) jest stałą równowagi (w odniesieniu do pierwszej równowagi opisanej powyżej); można powiedzieć, z dobrym przybliżeniem (ponieważ K3 należy również wziąć pod uwagę), że KM jest reprezentowany przez stosunek stałych kinetycznych K2 i K1 (odnoszących się do zniszczenia i utworzenia adduktu ES w pierwszej równowadze opisanej powyżej) .
Poprzez stałą Michaelisa-Mentena mamy „wskazanie powinowactwa między enzymem a substratem: jeśli KM jest małe c” jest „wysokim powinowactwem między enzymem a substratem, to addukt ES jest stabilny.
Enzymy podlegają regulacji (lub modulacji).
W przeszłości mówiono głównie o modulacji negatywnej, to znaczy hamowaniu zdolności katalitycznych enzymu, ale może również występować modulacja dodatnia, to znaczy istnieją gatunki zdolne do wzmacniania zdolności katalitycznych enzymu.
Istnieją 4 rodzaje zahamowań (uzyskane z przybliżeń wykonanych na modelu w celu dopasowania danych eksperymentalnych do równań matematycznych):
- konkurencyjne hamowanie
- hamowanie niekonkurencyjne
- niekonkurencyjne hamowanie
- hamowanie konkurencyjne
O hamowaniu kompetycyjnym mówimy wtedy, gdy cząsteczka (inhibitor) jest w stanie konkurować z substratem. W przypadku podobieństwa strukturalnego, inhibitor może reagować zamiast substratu; stąd terminologia „inhibicja kompetycyjna". Prawdopodobieństwo, że enzym zwiąże się z inhibitorem lub substratem zależy od stężenia obu i ich powinowactwa do enzymu; szybkość reakcji zależy zatem od tych czynników.
Aby uzyskać taką samą szybkość reakcji jak bez obecności inhibitora, konieczne jest wyższe stężenie substratu.
Wykazano eksperymentalnie, że w obecności inhibitora wzrasta stała Michaelisa-Menten.
Jeśli chodzi natomiast o „niekonkurencyjne hamowanie, interakcja między cząsteczką, która powinna działać jako modulator (inhibitor dodatni lub ujemny) a „enzymem”, zachodzi w miejscu innym niż to, w którym interakcja występuje między enzymem a substratem; mówimy zatem o modulacji allosterycznej (z greckiego allosteros → inna witryna).
Jeśli inhibitor zwiąże się z enzymem, może wywołać zmianę w strukturze enzymu, a w konsekwencji może zmniejszyć wydajność, z jaką substrat wiąże się z enzymem.
W tego typu procesie stała Michaelisa-Mentena pozostaje stała, ponieważ ta wartość zależy od równowagi między enzymem a substratem i nawet w obecności inhibitora równowagi te nie zmieniają się.
Zjawisko niekonkurencyjnego hamowania jest rzadkie; typowym inhibitorem niekonkurencyjnym jest substancja, która w sposób odwracalny wiąże się z adduktem ES, powodując ESI:

Hamowanie z powodu nadmiaru substratu może czasami być niekonkurencyjne, ponieważ ma to miejsce, gdy druga cząsteczka substratu wiąże się z kompleksem ES, dając początek kompleksowi ESS.
Z drugiej strony, inhibitor kompetycyjny może wiązać się tylko z adduktem enzymu substratu, jak w poprzednim przypadku: wiązanie substratu z wolnym enzymem indukuje modyfikację konformacyjną, która czyni miejsce dostępnym dla inhibitora.
Stała Michaelisa Mentena zmniejsza się wraz ze wzrostem stężenia inhibitora: najwyraźniej zatem wzrasta powinowactwo enzymu do substratu.
Proteaza serynowa
Są rodziną enzymów, do których należą chymotrypsyna i trypsyna.
Chymotrypsyna to enzym proteolityczny i hydrolityczny, który tnie na prawo od aminokwasów hydrofobowych i aromatycznych.
Produkt genu kodującego chymotrypsynę nie jest aktywny (aktywowany poleceniem); nieaktywna forma chymotrypsyny jest reprezentowana przez łańcuch polipeptydowy składający się z 245 aminokwasów. Chymotrypsyna ma kulisty kształt dzięki pięciu mostkom dwusiarczkowym i innym drobnym interakcjom (elektrostatyczne, siły Van der Waalsa, wiązania wodorowe itp.).
Chymotrypsyna jest wytwarzana przez komórki chymozy trzustki, gdzie jest zawarta w specjalnych błonach i wydalana przez przewód trzustkowy do jelita w czasie trawienia pokarmu: chymotrypsyna jest w rzeczywistości enzymem trawiennym. Białka i składniki odżywcze, które przyswajamy wraz z dietą, poddawane są trawieniu, aby zredukować je do mniejszych łańcuchów oraz zostać wchłonięte i przekształcone w energię (np. amylazy i proteazy rozkładają składniki odżywcze na glukozę i aminokwasy, które docierają do komórek przez naczynia krwionośne docierają do żyły wrotnej, a stamtąd trafiają do wątroby, gdzie podlegają dalszemu leczeniu).
Enzymy są produkowane w formie nieaktywnej i są aktywowane tylko wtedy, gdy dotrą do „miejsca, w którym muszą działać”; po zakończeniu ich akcji są dezaktywowane. Enzym raz zdezaktywowany nie może być reaktywowany: aby mieć „dalsze działanie katalityczne, musi zostać zastąpiony” inną cząsteczką enzymu. Gdyby chimitrypsyna była produkowana w aktywnej postaci już w trzustce, zaatakowałaby tę drugą: zapalenie trzustki to patologie spowodowane enzymami trawiennymi, które są już aktywowane w trzustce (a nie w wymaganych miejscach); niektóre z nich nie są leczone na czas, prowadzić do śmierci.
W chymotrypsynie i we wszystkich proteazach serynowych działanie katalityczne jest spowodowane obecnością anionu alkoholu (-CH2O-) w łańcuchu bocznym seryny.
Proteazy serynowe przyjmują tę nazwę właśnie dlatego, że ich katalityczne działanie jest spowodowane seryną.
Gdy cały enzym wykonał już swoje działanie, zanim będzie mógł ponownie działać na podłożu, musi zostać zregenerowany za pomocą wody; „uwalnianie” seryny przez wodę jest najwolniejszym etapem procesu i jest to ta faza co decyduje o szybkości katalizy.
Działanie katalityczne przebiega w dwóch fazach:
- tworzenie anionu o właściwościach katalitycznych (alkoholan anionu) i następujący po nim atak nukleofilowy na węgiel karbonylowy (C=O) z rozerwaniem wiązania peptydowego i utworzeniem estru;
- atak wody z przywróceniem katalizatora (zdolność do ponownego wywołania działania katalitycznego).
Różne enzymy należące do rodziny proteaz serynowych mogą składać się z różnych aminokwasów, ale dla wszystkich z nich miejsce katalityczne jest reprezentowane przez anion alkoholowy łańcucha bocznego seryny.
Podrodzina proteaz serynowych to podrodzina enzymów biorących udział w koagulacji (która polega na przekształceniu białka z jego formy nieaktywnej do „innej formy aktywnej). Enzymy te zapewniają, że koagulacja jest tak skuteczna, jak to możliwe i jest ograniczona w przestrzeni i czasu (koagulacja musi zachodzić szybko i musi zachodzić tylko w pobliżu uszkodzonego obszaru) Enzymy biorące udział w koagulacji są aktywowane kaskadowo (z aktywacji pojedynczego enzymu uzyskuje się miliardy enzymów: każdy aktywowany enzym z kolei aktywuje wiele innych enzymów).
Zakrzepica jest patologią spowodowaną nieprawidłowym działaniem enzymów krzepnięcia: jest spowodowana aktywacją, bez konieczności (ponieważ nie ma urazu), enzymów stosowanych w koagulacji.
Istnieją enzymy modulujące (regulacyjne) i enzymy hamujące inne enzymy: oddziałując z tymi ostatnimi, regulują lub hamują ich aktywność; nawet produkt enzymu może być inhibitorem enzymu.Istnieją również enzymy, które działają im więcej, im większy jest obecny substrat.
Lizozym
Luigi Pasteur odkrył, kichając na szalce Petriego, że w śluzie znajduje się enzym zdolny do zabijania bakterii: lizozym; z greckiego: liso = jaki rozmiar; Zimo = enzym.
Lizozym jest zdolny do rozbijania ściany komórkowej bakterii. Bakterie i ogólnie organizmy jednokomórkowe potrzebują struktur odpornych mechanicznie, które ograniczają ich kształt; wewnątrz bakterii panuje bardzo wysokie ciśnienie osmotyczne, które przyciągają wodę. Błona plazmatyczna eksplodowałaby, gdyby nie było ściany komórkowej, która sprzeciwiałaby się wnikaniu wody i ograniczałaby objętość bakterii.
Ściana komórkowa składa się z łańcucha polisacharydowego, w którym naprzemiennie występują cząsteczki N-acetylo-glukozaminy (NAG) i cząsteczki kwasu N-acetylomuraminowego (NAM); wiązanie pomiędzy NAG i NAM zostaje zerwane przez hydrolizę. Grupa karboksylowa NAM w ścianie komórkowej jest zaangażowana w wiązanie peptydowe z aminokwasem.
Pomiędzy różnymi łańcuchami tworzą się mostki składające się z wiązań pseudopeptydowych: rozgałęzienie jest spowodowane cząsteczką lizyny; struktura jako całość jest bardzo rozgałęziona, co zapewnia jej wysoką stabilność.
Lizozym jest antybiotykiem (zabija bakterie): działa tworząc pęknięcie w ścianie bakteryjnej; kiedy ta struktura (która jest odporna mechanicznie) pęka, bakteria pobiera wodę, aż pęknie. Lizozymowi udaje się zerwać wiązanie β-1,4 glukozydowe między NAM i NAG.
Miejsce katalityczne lizozymu jest reprezentowane przez rowek biegnący wzdłuż enzymu, w który wstawiony jest łańcuch polisacharydowy: w rowku umieszczono sześć pierścieni glukozydowych łańcucha.
W pozycji trzeciej rowka c "jest dławik: w tej pozycji można umieścić tylko jeden NAG, ponieważ NAM, który ma wyższe wymiary, nie może wejść. Rzeczywiste miejsce katalityczne znajduje się między pozycjami czwartą i piątą: ponieważ istnieje NAG w pozycji trzeciej, cięcie nastąpi między NAM i NAG (a nie odwrotnie), dlatego cięcie jest specyficzne.
Optymalne pH do działania lizozymu wynosi pięć. W miejscu katalitycznym enzymu, tj. pomiędzy pozycjami 4 i 5, znajdują się łańcuchy boczne kwasu asparaginowego i kwasu glutaminowego.
Stopień homologii: mierzy pokrewieństwo (tj. podobieństwo) między strukturami białkowymi.
Istnieje silny związek między lizozymem a syntazą laktozy.
Syntetaza laktozy syntetyzuje laktozę (która jest głównym cukrem mleka): laktoza jest galaktozyloglukozydem, w którym c” jest wiązaniem β-1,4 glukozydowym między galaktozą a glukozą.
Dlatego syntetaza laktozy katalizuje reakcję odwrotną do katalizowanej przez lizozym (który zamiast tego rozszczepia wiązanie β-1,4 glukozydowe)
Syntetaza laktozy jest dimerem, to znaczy składa się z dwóch łańcuchów białkowych, z których jeden ma właściwości katalityczne i jest porównywalny z lizozymem, a drugi jest podjednostką regulacyjną.
W czasie ciąży glikoproteiny są syntetyzowane przez komórki gruczołu sutkowego w wyniku działania transferazy galatozylowej (ma „homologię sekwencji 40% z lizozymem): enzym ten jest w stanie przenieść grupę galaktozylową ze struktury o wysokiej energii do struktura glikoproteiny W czasie ciąży indukowana jest ekspresja genu kodującego galaktozylotransferazę (występuje również ekspresja innych genów, które również dają inne produkty): następuje powiększenie piersi, ponieważ jest ona aktywowana gruczoł sutkowy (wcześniej nieaktywny), który musi wytwarzać mleko Podczas porodu wytwarzana jest α-laktoalbumina, która jest białkiem regulacyjnym: jest w stanie regulować zdolność katalityczną galaktozylotransferazy (poprzez rozróżnienie substratu). Galaktozylotransferaza modyfikowana α-laktalalbuminą jest w stanie przenieść galaktozyl na cząsteczkę glukozy: tworząc wiązanie β-1,4-glikozydowe i dając laktozę (syntetazę laktozy).
W związku z tym transferaza galaktozy przygotowuje gruczoł sutkowy przed porodem i wytwarza mleko po porodzie.
Aby wytworzyć glikoproteiny, transferaza galaktozylowa wiąże się z galaktozylem i NAG; podczas porodu albumina mleczanowa wiąże się z galaktozylotransferazą, dzięki czemu ta ostatnia rozpoznaje glukozę, a nie NAG, dając laktozę.






.jpg)