Analiza elementarna białek daje następujące średnie wartości: 55% węgla, 7% wodoru i 16% azotu, jasne jest, że białka różnią się od siebie, ale ich średni skład pierwiastkowy niewiele odbiega od wartości wskazanych powyżej .
Konstytucyjnie białka są makrocząsteczkami utworzonymi z naturalnych α-aminokwasów; aminokwasy łączą się przez wiązanie amidowe, które powstaje w wyniku reakcji między grupą aminową a-aminokwasu i karboksylem innego a-aminokwasu.
To wiązanie (-CO-NH-) jest również nazywane wiązaniem peptydowym, ponieważ wiąże peptydy (aminokwasy w połączeniu):
ten otrzymany jest dipeptydem, ponieważ składa się z dwóch aminokwasów. Ponieważ dipeptyd zawiera wolną grupę aminową na jednym końcu (NH2) i karboksyl na drugim (COOH), może reagować z jednym lub kilkoma aminokwasami i wydłużać łańcuch zarówno z prawej, jak i z lewej strony, w tej samej reakcji widać powyżej.
Sekwencja reakcji (które, nawiasem mówiąc, nie są tak proste) może trwać w nieskończoność: dopóki nie pojawi się polimer o nazwie polipeptyd lub białko. Rozróżnienie między peptydami a białkami wiąże się z masą cząsteczkową: zwykle dla mas cząsteczkowych wyższych niż 10 000 mówimy o białkach.
Wiązanie aminokwasów ze sobą w celu uzyskania nawet niewielkich białek jest trudnym zadaniem, chociaż ostatnio opracowano automatyczną metodę wytwarzania białek z aminokwasów, która daje doskonałe rezultaty.
Najprostsze białko składa się zatem z 2 aminokwasów: zgodnie z konwencją międzynarodową uporządkowana numeracja aminokwasów w strukturze białka zaczyna się od aminokwasu z wolną grupą a-aminową.
kodowanie tego białka), które napotyka nieistotne trudności chemiczne.
Uporządkowaną sekwencję aminokwasów można było określić poprzez degradację Edmana: białko poddaje się reakcji z izotiocyjanianem fenylu (FITC), początkowo dublet azotu α-aminowego atakuje izotiocyjanian fenylu tworząc pochodną tiokarbamylową; następnie otrzymany produkt cyklizuje dając pochodną fenylotiohydantoiny, która jest fluorescencyjna.
Edman opracował maszynę zwaną sekwencerem, która automatycznie dostosowuje parametry (czas, odczynniki, pH itp.) do degradacji i zapewnia pierwotną strukturę białek (za to otrzymał Nagrodę Nobla).
Struktura pierwszorzędowa nie jest wystarczająca do pełnej interpretacji właściwości cząsteczek białka; uważa się, że te właściwości zależą w zasadniczy sposób od konfiguracji przestrzennej, którą cząsteczki białka mają tendencję do fałdowania się na różne sposoby, to znaczy od założenia tego, co zostało zdefiniowane jako struktura drugorzędowa białek.
Struktura drugorzędowa białek migocze, to znaczy ma tendencję do rozpadu pod wpływem ogrzewania; następnie białka same się denaturują, tracąc wiele ze swoich charakterystycznych właściwości. Oprócz ogrzewania powyżej 70 ° C denaturacja może być również spowodowana napromieniowaniem lub działaniem reagentów (np. z mocnych kwasów).
Denaturację białek w wyniku efektu termicznego obserwuje się na przykład przez podgrzanie białka jaja: widać, że traci swój galaretowaty wygląd i zamienia się w nierozpuszczalną białą substancję. Jednak denaturacja białek prowadzi do zniszczenia ich struktury drugorzędowej, ale pozostawia niezmienioną ich strukturę pierwotną (konkatenacja różnych aminokwasów).
Białka przyjmują strukturę trzeciorzędową, gdy ich łańcuch, choć wciąż elastyczny pomimo wygięcia struktury drugorzędowej, zagina się w taki sposób, że powstaje powykrzywiany trójwymiarowy układ w kształcie ciała stałego. Za strukturę trzeciorzędową odpowiadają przede wszystkim wiązania dwusiarczkowe, które mogą powstać pomiędzy rozproszoną wzdłuż cząsteczki cysteiną-SH.
Natomiast struktura czwartorzędowa należy tylko do białek utworzonych przez dwie lub więcej podjednostek. Na przykład hemoglobina składa się z dwóch par białek (tj. we wszystkich czterech łańcuchach białkowych) umieszczonych na wierzchołkach czworościanu, tak aby utworzyć strukturę kulistą; cztery łańcuchy białkowe są utrzymywane razem przez siły jonowe i wiązania niekowalencyjne.
Innym przykładem struktury czwartorzędowej jest struktura insuliny, która wydaje się składać aż z sześciu podjednostek białkowych ułożonych parami w wierzchołkach trójkąta, w środku którego znajdują się dwa atomy cynku.
Białka włókniste
Są to białka o pewnej sztywności i znacznie dłuższej osi niż inne, włókniste białko obecne w większej ilości w naturze to kolagen (lub kolagen).
Białko włókniste może przybierać różne struktury drugorzędowe: α-helisę, β-arkusz oraz, w przypadku kolagenu, potrójną helisę; α-helisa jest najbardziej stabilną strukturą, a następnie β-arkusz, podczas gdy najmniej stabilna z trzech to potrójna helisa.
Prawidłowy jeżeli podążając za głównym szkieletem (zorientowanym od dołu do góry) wykonuje się ruch podobny do wkręcania śruby prawoskrętnej; gdy helisa jest z lewa ręka jeśli ruch jest analogiczny do wkręcania lewoskrętnej śruby.W prawoskrętnych α-helisach podstawniki -R aminokwasów są prostopadłe do głównej osi białka i skierowane na zewnątrz, podczas gdy w lewo- ręka a-helisy podstawniki -R skierowane są do wewnątrz. Prawoskrętne a-helisy są bardziej stabilne niż lewoskrętne, ponieważ między vati -R c "jest mniej interakcji i mniej przeszkód sterycznych. Wszystkie a-helisy znajdujące się w białkach są prawoskrętne.
Strukturę α-helisy stabilizują wiązania wodorowe (mostki wodorowe), które powstają między grupą karboksylową (-C = O) każdego aminokwasu a grupą aminową (-NH) znajdującą się później w czterech resztach sekwencja liniowa.
Przykładem białka o strukturze helisy α jest keratyna włosa.
Poprzez wydłużenie struktury α-helisy następuje przejście od α-helisy do β-kartki; również ciepło lub naprężenia mechaniczne pozwalają na przejście od helisy α do struktury arkusza β.
Zazwyczaj w białku struktury β-kartki są blisko siebie, ponieważ między łańcuchowymi wiązaniami wodorowymi mogą powstawać między częściami samego białka.
W białkach włóknistych większość struktury białka jest zorganizowana w α-helisę lub β-arkusz.
Białka kuliste
Mają prawie kulistą strukturę przestrzenną (ze względu na liczne zmiany kierunku łańcucha polipeptydowego); niektóre fragmenty bytu można prześledzić wstecz do struktury α-helisy lub β-kartki, a inne fragmenty nie są natomiast przypisane tym formom: układ nie jest przypadkowy, ale zorganizowany i powtarzalny.
Wspomniane dotychczas białka to substancje o całkowicie jednorodnej budowie: to znaczy czyste sekwencje połączonych aminokwasów; takie białka są powiedziane prosty; istnieją białka składające się z części białkowej i części niebiałkowej (grupa prostaty) zwane białkami sprzężony.
, w paznokciach, rogówce i soczewce oka, między przestrzeniami śródmiąższowymi niektórych narządów (np. wątroby) i tak dalej.
Jego struktura nadaje mu szczególne możliwości mechaniczne; ma dużą wytrzymałość mechaniczną związaną z dużą elastycznością (np. w ścięgnach) lub dużą sztywnością (np. w kościach) w zależności od funkcji, jaką ma pełnić.
Jedną z najciekawszych właściwości kolagenu jest jego konstytutywna prostota: składa się z około 30% proliny i około 30% glicyny; pozostałe 18 aminokwasów musi dzielić tylko pozostałe 40% struktury białka. Sekwencja aminokwasowa kolagenu jest niezwykle regularna: na każde trzy reszty trzecia to glicyna.
Prolina to aminokwas cykliczny, w którym grupa R wiąże się z azotem α-aminowym, co nadaje mu pewną sztywność.
Ostateczna struktura to powtarzalny łańcuch o kształcie „helisy; w łańcuchu kolagenowym nie ma wiązań wodorowych. Kolagen to „lewostronna helisa o skoku (długość odpowiadająca jednemu obrotowi helisy) większym niż „α-helisa; helisa kolagenowa jest tak luźna, że trzy łańcuchy białkowe są w stanie owinąć się wokół siebie tworząc „ pojedyncza lina: struktura potrójnej helisy.
Potrójna helisa kolagenu jest jednak mniej stabilna niż struktura α-helisy i β-kartki.
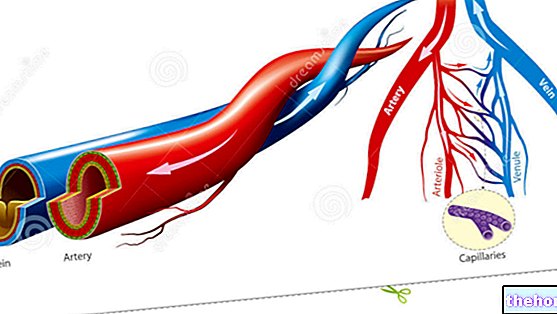
Przyjrzyjmy się teraz mechanizmowi produkcji kolagenu; rozważmy na przykład pęknięcie naczynia krwionośnego: temu pęknięciu towarzyszy mnóstwo sygnałów mających na celu zamknięcie naczynia, tworząc w ten sposób skrzep.
Koagulacja wymaga co najmniej trzydziestu wyspecjalizowanych enzymów. Po skrzepie należy kontynuować naprawę tkanki; komórki znajdujące się w pobliżu rany również produkują kolagen. Aby to zrobić, najpierw indukowana jest ekspresja genu, to znaczy organizmy, które wychodząc z informacji genu są w stanie wyprodukować białko (informacja genetyczna jest transkrybowana na mRNA, które opuszcza jądro i dociera do rybosomów w cytoplazma, w której informacja genetyczna jest tłumaczona na białko).Następnie kolagen jest syntetyzowany w rybosomach (wygląda jak helisa lewostronna złożona z około 1200 aminokwasów i mająca masę cząsteczkową około 150 000 d), a następnie gromadzi się w prześwitach, gdzie staje się substratem dla enzymów zdolnych do przeprowadzania modyfikacji potranslacyjnych (modyfikacje języka tłumaczonego przez „mRNA), w kolagenie modyfikacje te polegają na hydroksylacji niektórych łańcuchów bocznych, zwłaszcza proliny i lizyny.
Awaria enzymów prowadzących do tych zmian powoduje szkorbut: jest to choroba, która początkowo powoduje pękanie naczyń krwionośnych, pękanie zębów, po którym może dojść do krwotoku międzyjelitowego i śmierci; może to być spowodowane ciągłym stosowaniem żywności o przedłużonej trwałości.
Następnie, w wyniku działania innych enzymów, zachodzą inne modyfikacje polegające na glikozydacji grup hydroksylowych proliny i lizyny (cukier wiąże się z tlenem OH); Enzymy te znajdują się w obszarach innych niż światło, dlatego białko, ulegając modyfikacji, migruje do wnętrza retikulum endoplazmatycznego, by trafić do worków (pęcherzyków), które zamykają się i odrywają od retikulum: w nich znajduje się glikozydowany pro -monomer kolagenu – ten ostatni dociera do aparatu Golgiego, gdzie poszczególne enzymy rozpoznają cysteinę obecną w części karboksylowej glikozydowanego prokolagenu i powodują zbliżanie się różnych łańcuchów do siebie i tworzenie mostków dwusiarczkowych: w ten sposób trzy łańcuchy glikozydowany prokolagen otrzymuje się połączony ze sobą i jest to punkt wyjścia, z którego trzy wzajemnie przenikające się łańcuchy, następnie spontanicznie tworzą potrójną helisę.Trzy połączone ze sobą łańcuchy glikozydowanego prokolagenu docierają do pęcherzyka, dławiąc się, odrywa się od aparatu Golgiego, przenosząc trzy łańcuchy na obrzeże komórki, gdzie przez bezpiecznik jon z błoną plazmatyczną, trymetr jest wyrzucany z komórki.
W przestrzeni pozakomórkowej znajdują się szczególne enzymy, peptydazy prokolagenowe, które usuwają z gatunków wydalonych z komórki trzy fragmenty (po jednym dla każdej helisy) po 300 aminokwasów l "jeden, z końcowej części karboksylowej i trzy fragmenty (jeden na każdą helisę) po około 100 aminokwasów każdy, z części aminokońcowej: pozostaje potrójna helisa składająca się z około 800 aminokwasów na helisę, znana jako tropokolagen.
Tropokolagen ma wygląd dość sztywnego pręcika; różne trimery łączą się z wiązaniami kowalencyjnymi, tworząc większe struktury: mikrofibryle. W mikrowłókienkach różne trymery są ułożone naprzemiennie; wiele mikrowłókien stanowi wiązki tropokolagenu.
W kościach pomiędzy włóknami kolagenu znajdują się przestrzenie śródmiąższowe, w których osadzają się siarczany i fosforany wapnia i magnezu: sole te pokrywają również wszystkie włókna; to sprawia, że kości stają się sztywne.
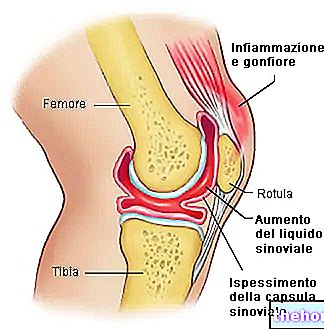
W ścięgnach przestrzenie śródmiąższowe są mniej zasobne w kryształy niż w kościach, podczas gdy obecne są mniejsze białka niż w tropokolagen, co nadaje ścięgnom elastyczność.
Osteoporoza to choroba spowodowana brakiem wapnia i magnezu, która uniemożliwia wiązanie soli w obszarach śródmiąższowych włókien tropokolagenu.