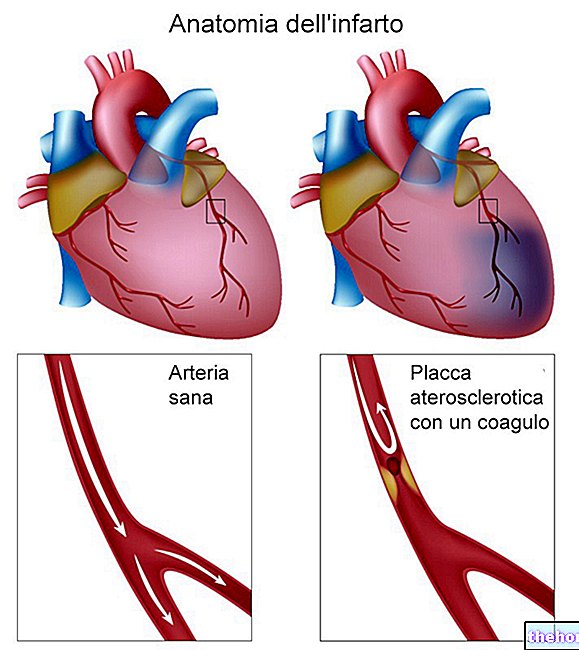
Co to jest Vitekta - elwitegrawir i w jakim celu się go stosuje?
Vitekta to lek przeciwwirusowy zawierający substancję czynną elwitegrawir. Jest wskazany w leczeniu dorosłych pacjentów zakażonych ludzkim wirusem niedoboru odporności typu 1 (HIV-1), wywołującym zespół nabytego niedoboru odporności (AIDS).Stosuje się go w skojarzeniu z lekami będącymi inhibitorami proteazy przyjmowanymi z rytonawirem oraz z innymi stosowanymi lekami. w leczeniu HIV u pacjentów, u których nie podejrzewa się oporności na elwitegrawir.
Jak stosuje się Vitekta - elwitegrawir?
Lek Vitekta jest wydawany wyłącznie na receptę, a leczenie powinien rozpoczynać lekarz mający doświadczenie w leczeniu zakażeń HIV. Vitekta jest dostępna w postaci tabletek (85 i 150 mg); zalecana dawka to jedna tabletka dziennie, przyjmowana z jedzeniem. Wybór dawki zależy od tego, jakie inne leki są podawane oprócz leku Vitekta. Produkt Vitekta należy przyjmować w tym samym czasie, co inhibitor proteazy podawany raz dziennie o tej samej porze lub z pierwszą dawką inhibitora proteazy podawaną dwa razy dziennie. Więcej informacji znajduje się w ulotce dołączonej do opakowania.
Jak działa Vitekta - elwitegrawir?
Substancja czynna leku Vitekta, elwitegrawir, jest rodzajem środka przeciwwirusowego zwanego „inhibitorem integrazy” Elwitegrawir blokuje enzym zwany integrazą, który bierze udział w etapie reprodukcji wirusa HIV. Jeśli enzym jest zablokowany, wirus nie może się normalnie rozmnażać, a rozprzestrzenianie się infekcji jest spowolnione. Vitekta nie leczy zakażenia HIV-1 ani AIDS, ale może opóźnić uszkodzenie układu odpornościowego oraz początek infekcji i chorób związanych z AIDS.
Jaką korzyść wykazuje Vitekta – elwitegrawir podczas badań?
Produkt Vitekta badano w jednym badaniu głównym z udziałem 712 pacjentów z HIV-1, którzy nigdy wcześniej nie byli leczeni inhibitorem integrazy. Główną miarą skuteczności było zmniejszenie liczby wirusów HIV (miano wirusa) we krwi.Uznano, że pacjenci z wiremią poniżej 50 kopii/ml po 48 tygodniach leczenia zareagowali na leczenie.W tym badaniu produkt Vitekta był co najmniej tak skuteczny jak raltegrawir (inny inhibitor integrazy) przyjmowany w skojarzeniu z innymi lekami stosowanymi w leczeniu zakażenia HIV. Po 48 tygodniach około 59% pacjentów leczonych produktem Vitekta (207 z 351) odpowiedziało na leczenie w porównaniu z około 58% pacjentów leczonych raltegrawirem (203 z 351).
Jakie jest ryzyko związane z Vitekta - elwitegrawirem?
Najczęstsze działania niepożądane związane ze stosowaniem leku Vitekta (mogące wystąpić nie częściej niż u 1 na 10 osób) to ból głowy, ból brzucha (ból żołądka), biegunka, wymioty, nudności, wysypka i zmęczenie (zmęczenie). Pełny wykaz działań niepożądanych zgłaszanych podczas stosowania leku Vitekta znajduje się w ulotce dla pacjenta Leku Vitekta nie wolno stosować z niektórymi innymi lekami, które mogą zmniejszać ich skuteczność lub zwiększać ryzyko oporności. Pełna lista ograniczeń znajduje się w ulotce dołączonej do opakowania.
Dlaczego zatwierdzono Vitekta - elwitegrawir?
Komitet ds. Produktów Leczniczych Stosowanych u Ludzi (CHMP) Agencji uznał, że korzyści płynące ze stosowania preparatu Vitekta przewyższają ryzyko, i zalecił jego dopuszczenie do stosowania w UE CHMP uznał, że korzyści płynące ze stosowania preparatu Vitekta w zmniejszaniu liczby zakażeń HIV we krwi były wyraźnie wykazane w kontekście badań. Profil bezpieczeństwa leku nie był uważany za problem, ponieważ działania niepożądane są porównywalne z działaniami innych leków. Komitet zauważył również, że istnieje znaczny potencjał interakcji z innymi produktami leczniczymi, co uwzględniono w ulotce dołączonej do opakowania.
Jakie informacje wciąż czekają na Vitektę - elwitegrawir?
Opracowano plan zarządzania ryzykiem, aby zapewnić jak najbezpieczniejsze użytkowanie produktu Vitekta. W oparciu o ten plan do charakterystyki produktu leczniczego i ulotki dołączonej do opakowania produktu Vitekta dodano informacje dotyczące bezpieczeństwa, w tym odpowiednie środki ostrożności, których powinni przestrzegać pracownicy służby zdrowia i pacjenci.
Więcej informacji o Vitekta - elwitegrawir
W dniu 13 listopada 2013 r. Komisja Europejska przyznała produkt Vitekta „Pozwolenie na dopuszczenie do obrotu” ważne na terenie całej Unii Europejskiej.W celu uzyskania dodatkowych informacji na temat leczenia preparatem Vitekta należy zapoznać się z ulotką dla pacjenta (dołączoną do EPAR) lub skonsultować się z lekarzem lub farmaceutą.
Ostatnia aktualizacja niniejszego podsumowania: 11/2013.
Informacje na temat Vitekta - elwitegrawir opublikowane na tej stronie mogą być nieaktualne lub niekompletne. Aby prawidłowo wykorzystać te informacje, zobacz stronę Wyłączenie odpowiedzialności i przydatne informacje.




















fortuna-di-halloween.jpg)