Przyczyną dystrofii mięśniowej Duchenne'a jest mutacja genu kodującego dystrofinę, białko niezbędne dla zdrowia i funkcjonowania mięśni.
Dystrofia mięśniowa Duchenne'a zaczyna objawiać się w pierwszych latach życia, wpływając na aktywność głównych mięśni kończyn, od tego momentu stan pacjentów pogarsza się powoli, ale stopniowo: w dzieciństwie zmusza ich do poruszania się na wózku inwalidzkim, między okresem dojrzewania a początkiem dorosłości powoduje pierwsze problemy z sercem i układem oddechowym, których ewolucja będzie najczęstszą przyczyną śmierci w wieku około 30 lat.
Niestety, wciąż nie ma lekarstwa na dystrofię mięśniową Duchenne'a; chorzy mogą jednak liczyć na różne leczenie objawowe, mogące złagodzić objawy i przedłużyć życie.
Krótkie przypomnienie Genetyki
Czym jest DNA?
Zawarty w jądrze komórkowym DNA jest biologiczną makrocząsteczką, która zawiera wszystkie informacje niezbędne do prawidłowego rozwoju i funkcjonowania komórek organizmów żywych, w których jest obecne.
Czym są chromosomy?
Chromosomy to jednostki strukturalne, w których zorganizowane jest DNA.
Każda komórka zdrowego człowieka zawiera 22 pary chromosomów autosomalnych (lub niepłciowych) i jedną parę chromosomów płci (u mężczyzn są to chromosomy X i Y, u kobiet dwa chromosomy X).
Jeden chromosom każdej pary z 23 pochodzi od matki, a drugi od ojca.
Czym są geny?
Geny to krótkie odcinki (lub sekwencje) DNA o podstawowym znaczeniu biologicznym: z nich w rzeczywistości wywodzą się cząsteczki fundamentalne dla życia: białka.
Dla każdego genu istnieją dwie wersje, zwane allelami, które należą, jedna do chromosomu matczynego, a druga do chromosomu ojcowskiego.
Co to jest mutacja genetyczna?
Jest to „zmiana sekwencji DNA, która tworzy gen.
Z powodu tej zmiany powstałe białko jest albo wadliwe, albo całkowicie nieobecne; w obu przypadkach skutki mogą być szkodliwe zarówno dla życia komórki, w której zachodzi mutacja, jak i całego organizmu.
Dystrofia mięśniowa Duchenne'a: na jakie mięśnie ma wpływ?
Dystrofia mięśniowa Duchenne'a dotyczy najpierw mięśni kończyn dolnych i górnych, które są w pewnym stopniu związane z tułowiem. Typowymi celami tej choroby są zatem: mięsień czworogłowy, mięsień biodrowo-lędźwiowy i pośladki w odniesieniu do kończyn dolnych oraz mięśnie naramienne, klatka piersiowa i podłopatkowa w odniesieniu do kończyn górnych.
Na późniejszym etapie DMD rozciąga się na mięśnie oddechowe i mięsień sercowy, chociaż nie są to dokładnie mięśnie dobrowolne.
Należy zauważyć, że pierwsze mięśnie, które kiedykolwiek cierpią na dystrofię mięśniową Duchenne'a, to mięśnie kończyn dolnych.
Epidemiologia: Jak powszechna jest dystrofia mięśniowa Duchenne'a?
W przypadku mechanizmów genetycznych, które zostaną omówione później, dystrofia mięśniowa Duchenne'a dotyka głównie mężczyzn i rzadko kobiety.
Według danych epidemiologicznych jeden na 3500-6000 mężczyzn urodziłby się z DMD.
Istnieją różne formy dystrofii mięśniowej; wśród nich najbardziej rozpowszechniony jest Duchenne.
Czy wiedziałeś, że ...
We Włoszech byłoby około 2000 osób z dystrofią mięśniową Duchenne'a.
Więcej informacji: Rodzaje dystrofii mięśniowej .Mutacja odpowiedzialna za DMD skutkuje całkowitym brakiem dystrofiny.
Dystrofina
Dystrofina to białko zawarte w komórkach tworzących włókno mięśniowe. Pełni różne funkcje, w szczególności:
- Łączy błonę włókna mięśniowego, zwaną sarkolemmą, z błoną komórkową i macierzą pozakomórkową.
- Reguluje ruchy jonów wapnia wewnątrz komórki (uwaga: wapń odpowiada za skurcz mięśni).
W przypadku braku dystrofiny procesy te zawodzą, a komórka mięśniowa ulega śmiertelnemu stresowi oksydacyjnemu.
Dystrofia mięśniowa Duchenne'a: patogeneza

Brak dystrofiny ma różne konsekwencje:
- Dochodzi do nadmiernej penetracji jonów wapnia do sarkolemy, co powoduje nadmierne wnikanie wody do mitochondriów komórek mięśniowych (miocytów), które „pękają”.
- Błony plazmatyczne komórek mięśniowych stają się kruche i łatwo pękają.
Ta kruchość błon, związana z utratą mitochondriów, prowadzi do martwicy komórek. - Opisane powyżej zdarzenia trwają zdecydowanie szybciej niż mechanizmy komórkowe odpowiedzialne za naprawę i wymianę uszkodzonych miocytów. To nieuchronnie prowadzi do postępującego pogarszania się sytuacji.
- Zastąpienie martwych miocytów to tkanka łączna (lub zwłóknieniowa) i komórki tłuszczowe. Proces ten podkreśla jedyne widoczne powiększenie niektórych mięśni, powiększenie, które eksperci określają terminem pseudoprzerost.
Dystrofia mięśniowa Duchenne'a: genetyka
Dystrofia mięśniowa Duchenne'a jest chorobą, która podlega recesywnemu dziedziczeniu sprzężonemu z chromosomem X:
- Połączony z chromosomem X oznacza to, że choroba zależy od mutacji genu zlokalizowanego na chromosomie płci X;
- Recesywny oznacza to, że oba allele odpowiedzialnego genu muszą być zmutowane, aby patologia mogła się ujawnić.
DMD dotyka głównie płci męskiej z bardzo specyficznego powodu genetycznego: mężczyzna ma tylko jeden chromosom X (drugi to chromosom Y), w konsekwencji mutacja genu w nim obecnego pozbawia cały organizm zakodowanego białka. gen, natomiast kobieta ma dwa chromosomy X i w przypadku chorób genetycznych o dziedziczeniu recesywnym mutacja tylko jednego z nich nie jest wystarczająca do ustalenia patologii (zdrowy chromosom rekompensuje braki zmutowany) .
Aby kobieta cierpiała na dystrofię mięśniową Duchenne'a, oba chromosomy X muszą być zmutowane w genie dystrofiny: jest to rzadka, ale nie niemożliwa okoliczność obserwowana u około jednej na 50 000 kobiet.
W rzeczywistości należy zauważyć, że z szeregu złożonych przyczyn genetycznych, które nie zostały tutaj opisane, DMD może również wystąpić u niektórych kobiet z tylko jednym zmutowanym chromosomem X.
Dystrofia mięśniowa Duchenne'a: dziedziczenie i transmisja

Dystrofia mięśniowa Duchenne'a może być chorobą dziedziczną; choroba genetyczna jest stanem spowodowanym mutacjami przekazanymi od jednego z rodziców (lub nawet obojga).
W większości przypadków dziedziczna DMD jest wywoływana przez „spotkanie zdrowego mężczyzny i kobiety, która jest zdrowym nosicielem choroby. mutacja w genie kodującym dystrofinę.
W takiej sytuacji chorować mogą tylko dzieci płci męskiej; z drugiej strony córki mogą być tylko zdrowymi nosicielkami choroby.
Wszystko to dzieje się z wyjaśnionego powyżej powodu, związanego z różną liczbą chromosomów X obecnych u obu płci.
Oto bardziej szczegółowo, co może się zdarzyć, gdy zdrowy mężczyzna i zdrowa kobieta z DMD począją dziecko:
- TEN synowie mają 50% szans na to, że będą chorzy lub zdrowi. Są chore, jeśli odziedziczą zmutowany chromosom X od swojej matki, natomiast są zdrowe, jeśli odziedziczą chromosom X bez mutacji od matki.
- ten córki mają 50% szans na bycie zdrowym lub zdrowym nosicielem choroby. Są zdrowi, jeśli odziedziczą zdrowy chromosom X od matki, natomiast są zdrowymi nosicielami, jeśli otrzymają zmutowany chromosom X od matki.
Jak widać, w badanej sytuacji, zarówno w przypadku synów, jak i córek, kluczową rolę zawsze odgrywa matka.
Należy zauważyć, że dziedziczna dystrofia mięśniowa Duchenne'a może być również wynikiem spotkania chorego mężczyzny ze zdrową kobietą, która jest nosicielką choroby.
W tej szczególnej sytuacji dzieci płci męskiej nadal mają 50% szans na to, że będą zdrowe lub chore (z tych samych powodów, co w poprzednim przypadku), podczas gdy córki córki mogą być zdrowymi nosicielkami choroby lub zachorować (biorąc pod uwagę, że z ich córki ojca zawsze dziedziczą zmutowany chromosom X, są chore, jeśli otrzymają również zmutowany chromosom X matki).
W porównaniu z pierwszym analizowanym przypadkiem ta druga sytuacja jest zdecydowanie rzadsza, czego dowodem jest to, że jedna kobieta na 50 000 rodzi się z DMA.
Nabyta dystrofia mięśniowa Duchenne'a
Chociaż bardzo rzadko, dystrofia mięśniowa Duchenne'a może być również stanem rozwijającym się wkrótce po zapłodnieniu, podczas rozwoju embrionalnego, w wyniku spontanicznej mutacji.
W tym przypadku mówimy o nabytej dystrofii mięśniowej Duchenne'a.
W nabytych postaciach DMD rodzice są zdrowi, a zdarzenie mutacyjne jest całkowicie nie do rozważenia.
i biegać; następnie walczy również o poruszanie rękami i szyją.
Pomiędzy okresem dojrzewania a początkiem dorosłości osłabienie postępuje dalej i dotyczy prawie wszystkich mięśni, w tym mimowolnych odpowiedzialnych za oddychanie i mięśnia sercowego.
Należy zauważyć, że w przebiegu choroby u niektórych pacjentów rozwijają się również deficyty poznawcze i zaburzenia zachowania.
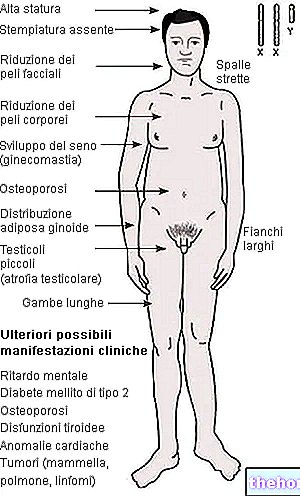
Więcej informacji: Objawy dystrofii mięśniowej Duchenne'aDystrofia mięśniowa Duchenne'a: objawy motoryczne
Charakterystyczne objawy motoryczne dystrofii mięśniowej Duchenne'a to:
- Opóźnienie pierwszych kroków (Uwaga: może wystąpić również u zdrowych dzieci);
- Trudności w chodzeniu, bieganiu, skakaniu i wchodzeniu po schodach z powodu osłabienia mięśni kończyn dolnych;
- Chód jest kołysany, podobny do „gęsiego” (chód machający lub przechylający);
- Hipostenia mięśni kończyn górnych i szyi;
- Trudności w podnoszeniu się z ziemi. Pacjent „wspina się” na sobie, podtrzymując kończyny górne i kolana (objaw Gowera);
- Powiększenie cieląt w wyniku wspomnianego już zjawiska zwanego pseudoprzerostem;
- Skolioza lędźwiowa i hiperlordoza z powodu osłabienia mięśni zginaczy biodra;
- Przykurcze spowodowane długotrwałym unieruchomieniem, a następnie zaburzenia stawów.
Od końca dzieciństwa do początku okresu dojrzewania trudności ruchowe kończyn dolnych są takie, że zmuszają pacjenta do korzystania z wózka inwalidzkiego.
Zwykle w wieku 21 lat osoba cierpiąca na DMD jest sparaliżowana od szyi w dół.
Dystrofia mięśniowa Duchenne'a: objawy poznawcze
Zgodnie z przewidywaniami, niektórzy pacjenci z DMD z czasem rozwijają deficyty poznawcze i zaburzenia behawioralne.
Stany te obejmują na przykład dysleksję, ADHD (zespół nadpobudliwości psychoruchowej z deficytem uwagi) i deficyty pamięci krótkotrwałej.
Dystrofia mięśniowa Duchenne'a: powikłania
Dystrofia mięśniowa Duchenne'a, zwykle rozpoczynająca się w okresie dojrzewania lub późnym okresie dojrzewania, rozciąga się na mięśnie serca (mięsień sercowy), powodując postać kardiomiopatii rozstrzeniowej.
Następnie choroba obejmuje również mięśnie mimowolnego oddychania (mięśnie przepony i międzyżebrowe) oraz mięśnie odpowiedzialne za żucie; to dalsze pogorszenie, początkowo jedynie predysponuje do infekcji dróg oddechowych (np. zapalenia płuc), a później powoduje niewydolność oddechową.
Należy zauważyć, że w międzyczasie pojawiają się również osteoporoza (z powodu wymuszonego unieruchomienia) oraz problemy żołądkowo-jelitowe (zaparcia) związane z utratą funkcji mięśni gładkich jelita.
Kardiomiopatia i problemy z oddychaniem postępują aż do zgonu: zwykle w rzeczywistości śmierć pacjentów z dystrofią mięśniową Duchenne'a następuje z powodu powikłań sercowo-oddechowych.
Wiek śmierci większości pacjentów to około 30 lat.
(badanie lekarskie);Pomiar kinazy kreatynowej
Krew zawiera enzym kinazę kreatynową (CK lub CPK).
Stwierdzono, że pacjenci z DMD mają bardzo wysokie dawki kinazy kreatynowej, od 10 do 100 razy wyższe niż normalnie.
Pomiar poziomu kinazy kreatynowej we krwi jest przydatny w identyfikacji nieprawidłowego stanu wpływającego na mięśnie, ale nie jest zbyt szczegółowy: oprócz DMD, w rzeczywistości, kilka innych stanów powoduje znaczny wzrost CK.
Biopsja mięśnia
Biopsja mięśnia jest zwykle kolejnym krokiem po teście kinazy kreatynowej. Analiza próbki tkanki mięśniowej pozwala w rzeczywistości zbadać komórki, które ją tworzą, ocenić stan włókien mięśniowych i określić ilościowo poziom dystrofiny.
Usunięcie kawałka mięśnia polega na niewielkiej operacji w znieczuleniu miejscowym.
Biopsja mięśnia u pacjenta z DMD: wyniki analiz
- Całkowity brak dystrofiny (niskie poziomy charakteryzują inne formy dystrofii mięśniowej).
- Obecność tkanki włóknisto-tłuszczowej zamiast mięśni (objaw pseudoprzerostu).
- Włókna mięśniowe ulegają degeneracji.
Elektromiografia
Elektromiografia to procedura diagnostyczna mająca na celu ocenę stanu zdrowia mięśni i nerwów obwodowych kontrolujących ich aktywność.
W oparciu o użycie elektrod, elektrod igłowych i instrumentu zwanego elektromiografem, test ten pozwala nam analizować aktywność mięśni w odpowiedzi na bodźce nerwowe.
U osób z dystrofią mięśniową Duchenne'a elektromiografia pokazuje, że mięśnie nie reagują na impulsy nerwowe, jak w normalnych warunkach.
Elektromiografia pomaga w diagnozowaniu DMD, ponieważ odróżnia patologie spowodowane dysfunkcjami mięśni (takie jak dystrofie mięśniowe) od chorób pochodzenia nerwowego, które mają wpływ na mięśnie (np. choroby neuronu ruchowego).
Test genetyczny
Analiza genetyczna profilu chromosomalnego osobnika pozwala zidentyfikować wszelkie mutacje genetyczne wpływające na chromosomy.
Badanie genetyczne profilu chromosomalnego jest zwykle badaniem diagnostycznym potwierdzającym obecność lub brak dystrofii mięśniowej Duchenne'a.
Ocena genetyczna może być wykonywana nie tylko w fazie poporodowej (po porodzie), ale także przed urodzeniem (prenatalna).
Do badania poporodowego wystarczy pobranie krwi i późniejsza analiza próbki krwi; z kolei w przypadku badania prenatalnego istnieją dwie możliwości: DNA płodu (o małym marginesie błędu) oraz analiza próbki płynu owodniowego pobranej w drodze amniopunkcji lub CVS (małe ryzyko aborcji).
Fizjoterapia, aktywność ruchowa i pomoce ortopedyczne
Fizjoterapia i regularna aktywność ruchowa są niezbędne do spowolnienia atrofii i osłabienia mięśni.
Zachęcanie pacjenta do poruszania się, oczywiście w miarę możliwości, służy tonizacji mięśni i zapobieganiu (lub przynajmniej odkładaniu) niektórych powikłań; ćwiczenia fizyczne w rzeczywistości przeciwstawiają się osteoporozie, zaparciom i skoliozie.
Stała fizjoterapia, wychowanie postawy i korzystanie z pomocy ortopedycznych pozwalają zachować przynajmniej częściowo ruchomość stawów, ścięgien i mięśni.
Zapamietaj to ...
Gdy funkcja mięśni kończyn dolnych jest całkowicie upośledzona, pacjent z DMD jest przykuty do wózka inwalidzkiego.
W przypadku DMD przyjmowanie kortykosteroidów może pomóc w utrzymaniu masy i siły mięśniowej pacjenta.
Kortykosteroidy powszechnie stosowane u pacjentów z dystrofią mięśniową Duchenne'a obejmują prednizolon i deflazakort.
Leczenie i zapobieganie powikłaniom
Kiedy DMD komplikuje zdrowie serca i mięśni oddechowych, pacjent potrzebuje leków kontrolujących kardiomiopatię rozstrzeniową, przenośnego aparatu oddechowego do wentylacji mechanicznej, a czasem rozrusznika serca.
Co więcej, zawsze, gdy choroba osiągnie ten etap, lekarze zalecają uzyskanie szczepionki przeciw grypie i szczepionki przeciw pneumokokom, aby zapobiec najczęstszym infekcjom dróg oddechowych u pacjentów z DMD.
W przypadku ciężkiej skoliozy wymagana jest operacja; to samo dotyczy sytuacji, gdy funkcja żucia jest całkowicie zaburzona (gastrostomia).
Szczepionki:
- Przeciw grypie
- Przeciwpneumokokowe
Kontrole okresowe:
- Test czynności płuc
- Poziom tlenu we krwi.
Leki stosowane w leczeniu kardiomiopatii:
- beta-blokery;
- Diuretyki;
- Inhibitory ACE.
Kontrole okresowe:
- Elektrokardiogram;
- Echokardiogram;
- Ultradźwięk.
Leki:
- Środki przeczyszczające przeciwko zaparciom.
Chirurgia:
- Gastrostomia, dla pacjentów z trudnościami w żuciu i połykaniu.
Aby twoje kości były „mocniejsze”:
- Podawanie witaminy D i wapnia;
- Ekspozycja na światło słoneczne.
Chirurgia:
- Tenotomia zginaczy biodra;
- W szczególności rozciąganie ścięgien. ten achilleo
Zatwierdzone leki na dystrofię mięśniową Duchenne'a
- W 2014 roku EMA (Europejska Agencja Leków) zatwierdziła Ataluren, lek, który, jak wykazano, łagodzi objawy u pacjentów z mukowiscydozą i dystrofią mięśni Duchenne'a.
Należy zauważyć, że efekty Atalurenu u pacjenta z DMD są zauważalne tylko wtedy, gdy pacjent nadal jest w stanie chodzić.
Ataluren nie jest dokładnie zatwierdzonym lekiem na dystrofię mięśniową Duchenne'a. - W 2016 r. w Stanach Zjednoczonych FDA (Administracja Jedzenia i Leków) zatwierdził pierwszy specyficzny lek przeciwko dystrofii mięśniowej Duchenne'a: jest to Exondys 51, znany również jako eteplirsen.
Wydaje się, że lek ten jest w stanie promować produkcję dystrofiny, przeciwdziałając w ten sposób przebiegowi choroby.
Exondys 51 jest wskazany tylko do stosowania u pacjentów z postacią DMD charakteryzującą się „zmianą” eksonu 51 genu dystrofiny, która dotyczy 13% wszystkich przypadków dystrofii mięśniowej Duchenne'a. - Odpowiednio w 2019 i 2020 roku FDA zatwierdziła Vyondys 53 (golodirsen) i Vilepso (viltolarsen), dwa specyficzne leki do leczenia dystrofii mięśniowej Duchenne'a.
Leki te są wskazane tylko do stosowania u pacjentów z postacią DMD charakteryzującą się „zmianą” egzonu 53 genu dystrofiny, która dotyczy 8% wszystkich przypadków dystrofii mięśniowej Duchenne'a.








-corpi-estranei-e-altre-cause.jpg)