Ogólność
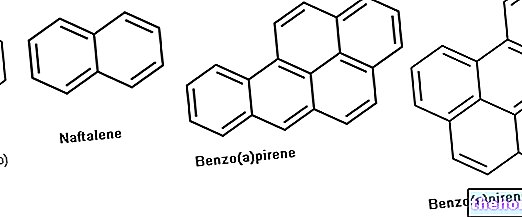
Siarkowodór – inaczej zwany siarkowodorem lub siarkowodorem (H2S) – to cząsteczka rozpuszczalna w wodzie i etanolu, która wydziela bardzo silny zapach „zgniłego jajka”.

Siarkowodór (H2S) jest trujący, a nawet śmiertelny dla człowieka, jego uwalnianie do powietrza następuje głównie w wyniku:
- Bakteryjny lub enzymatyczny rozkład białek zawierających siarkę w wiązaniach stabilizujących, takich jak mostki dwusiarczkowe i aminokwasy siarkowe
- Gotowanie białek i denaturacja struktur drugorzędowych, trzeciorzędowych i czwartorzędowych z rozerwaniem mostków dwusiarczkowych.
Siarkowodór (H2S) jest wysoce obecny w wyziewach pochodzących z: kieszeni powietrznych w podłożu, ropy naftowej i obszarów o wysokiej aktywności gnilnej (takich jak stawy, bagna i bagna); siarkowodór jest jednym z aromatycznych składników najczęściej występujących w kale i gazach jelitowych ale jego uwalnianie w dużych ilościach ma miejsce głównie w cyklach produkcyjnych przemysłu spożywczego, przy oczyszczaniu wody z osadów, w rafinacji ropy naftowej itp.
NB. Siarkowodór (H2S) reaguje ze srebrem i powierzchownie tworzy czarną patynę siarczku srebra, widoczną po kąpielach termalnych na pierścionkach, kolczykach i naszyjnikach.
Toksyczność
Siarkowodór (H2S) to trucizna działająca poprzez hamowanie oddychania mitochondrialnego, dlatego jego toksyczne działanie wpływa na wszystkie komórki organizmu, które wykorzystują metabolizm tlenowy (praktycznie wszystkie, z wyjątkiem czerwonych krwinek), najbardziej niebezpieczna cecha siarkowodoru (H2S) w średnio-wysokich stężeniach jest to jego zdolność do dezaktywacji zmysłowej percepcji węchowej, jako jedynego dzwonka alarmowego dla obecności siarkowodoru (H2S) w powietrzu. Z drugiej strony, w niskich stężeniach siarkowodór (H2S) powoduje podrażnienie błon śluzowych, hiperwentylację i obrzęk płuc, a dłuższa ekspozycja prowadzi do chronicznego zmęczenia, utraty apetytu, bólu głowy, zaburzeń poznawczych i pamięci.
Siarkowodór (H2S) jest już wyczuwalny w stężeniach 0,0047 części na milion (przez 50% ludzi), podczas gdy 10 ppm stanowi dolną granicę toksyczności bez ryzyka uszkodzenia zdrowia po ekspozycji przez 8 kolejnych godzin; przy poziomach równych 1000 ppm siarkowodoru (H2S) następuje natychmiastowe załamanie nawet po jednym oddechu.
Stężenia w częściach na milion (ppm)
Wpływ na organizm człowieka
0,0047ppm
Dolna granica percepcji dla 50% osób
<10ppm
Limit narażenia bez szkody dla zdrowia, przez 8 godzin dziennie
10-20 ppm
Granica, powyżej której oczy są podrażnione gazem
50-100 ppm
Stężenie powodujące uszkodzenie komórek
100-150ppm
Koncentracja paraliżująca nerw węchowy
320-530ppm
Koncentracja powodująca obrzęk płuc
530-1000ppm
Koncentracja, która powoduje hiperwentylację
800ppm
Dolna granica śmiertelności 50% osób po 5" ekspozycji
> 1000 ppm
Minimalne stężenie powodujące zadławienie po 1 oddechu
Siarkowodór w żywności
Siarkowodór (H2S) może być wytwarzany w żywności, z której jest uwalniany w wyniku parowania gazowego; siarkowodór (H2S) jest typową pochodną niektórych przemian chemicznych, takich jak np. zrywanie mostków dwusiarczkowych i agregacja jonów wodorowych ( H +) po „gotowaniu białek" (denaturacja). Reakcja ta jest dobrze wyczuwalna w jajku ugotowanym na twardo, które wytwarza siarkowodór (H2S) z siarki zawartej w białku (która, chociaż lotna, jest zatrzymywana przez powłoki), w momencie łuskania natychmiast uwalnia gaz, dzięki czemu jest wyczuwalny przez nos. Pamiętamy również, że w gotowanym jajku siarkowodór (H2S) uwalniany podczas gotowania białka jaja jest odpowiedzialny za żelazne (powierzchowne) chelatowanie żółtka z produkcją soli zwanej siarczek żelaza (FeS)plus dwa jony wodorowe; reakcja chemiczna jest następująca:
H2S + Fe++ → FeS + H2
NB. Siarczek żelazawy jest związkiem, który chelatując żelazo w żółtku i częściowo zapobiegając jego wykorzystaniu metabolicznemu, jest nieszkodliwy w niskich stężeniach, ALE nie należy go lekceważyć w wysokich dawkach.
Siarkowodór (H2S) jest również związkiem ułatwiającym odróżnienie: żywności zdrowego pochodzenia zwierzęcego od żywności ulegającej rozkładowi – dzieje się tak ze względu na działanie gnilnych bakterii zarówno na mostki siarczkowe białek, jak i na aminokwasy siarkowe, z następczym uwolnieniem siarki przeznaczonej do syntezy siarkowodoru (H2S). NB. Ten proces jest rozpoznawalny szczególnie w degradacji jaj i ryb uszkodzonych przez słabą konserwację.





-cos-dove-si-trova-e-tossicit.jpg)