Składniki aktywne: Etonogestrel / Etynyloestradiol
NuvaRing, 0,120 mg / 0,015 mg co 24 godziny, urządzenie dopochwowe
Wskazania Dlaczego stosuje się Nuvaring? Po co to jest?
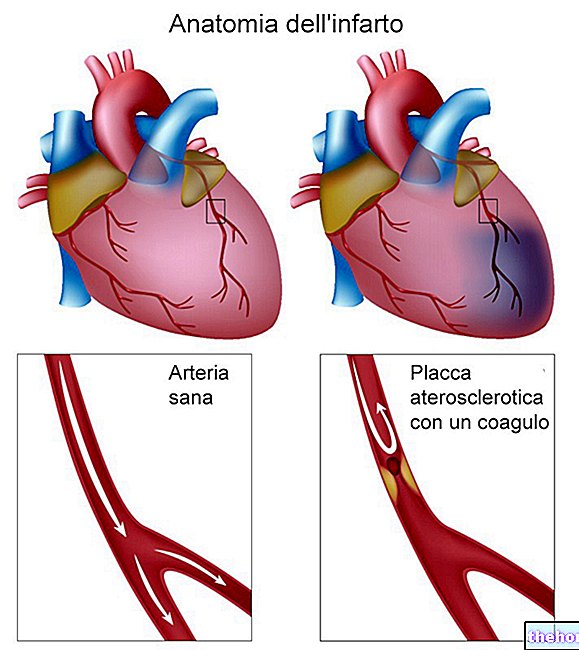
NuvaRing to antykoncepcyjny pierścień dopochwowy stosowany w celu zapobiegania ciąży. Każdy pierścień zawiera niewielką ilość dwóch żeńskich hormonów płciowych: etonogestrelu i etynyloestradiolu. Pierścień powoli uwalnia te hormony do krwioobiegu.Ponieważ ilość uwalnianych hormonów jest niewielka, NuvaRing jest uważany za niskodawkowy środek antykoncepcyjny.Ponieważ NuvaRing uwalnia dwa różne rodzaje hormonów, jest to tak zwany złożony środek antykoncepcyjny.
NuvaRing działa jak złożona pigułka antykoncepcyjna (Pill), ale zamiast jednej pigułki dziennie, pierścień jest stosowany przez trzy tygodnie z rzędu.NuvaRing uwalnia dwa żeńskie hormony płciowe, które zapobiegają uwalnianiu komórki jajowej z jajników. nie ma uwalniania komórek jajowych, nie można zajść w ciążę.
Przeciwwskazania, kiedy nie należy stosować leku Nuvaring
Uwagi ogólne Przed rozpoczęciem stosowania NuvaRing należy zapoznać się z informacjami dotyczącymi zakrzepów krwi. Szczególnie ważne jest zapoznanie się z objawami zakrzepu krwi
W tej ulotce opisano niektóre sytuacje, w których należy przerwać stosowanie NuvaRing lub w przypadku, gdy NuvaRing może być mniej skuteczny.W takich sytuacjach nie należy odbyć stosunków płciowych lub należy zastosować dodatkowe niehormonalne środki antykoncepcyjne, takie jak stosowanie prezerwatywy lub innej metody mechanicznej . Nie używaj metod pomiaru rytmu i temperatury podstawowej, które mogą być zawodne, ponieważ NuvaRing zmienia miesięczne zmiany temperatury ciała i śluzu szyjkowego.
NuvaRing, podobnie jak inne hormonalne środki antykoncepcyjne, nie chroni przed zakażeniem wirusem HIV (AIDS) ani innymi chorobami przenoszonymi drogą płciową.
Nie używaj NuvaRing, jeśli cierpisz na którykolwiek z poniższych stanów. Jeśli cierpisz na którykolwiek z poniższych stanów, skontaktuj się z lekarzem. Twój lekarz omówi z Tobą inne metody kontroli urodzeń, które mogą być dla Ciebie bardziej odpowiednie.
- jeśli masz (lub kiedykolwiek) zakrzep krwi w naczyniu krwionośnym nogi (zakrzepica żył głębokich, DVT), płuc (zator tętnicy płucnej, PE) lub innych narządów; 2 54 mm 4 mm
- jeśli wiesz, że masz zaburzenie, które wpływa na krzepliwość krwi, takie jak niedobór białka C, niedobór białka S, niedobór antytrombiny III, czynnik V Leiden lub przeciwciała antyfosfolipidowe;
- jeśli planujesz „operację” lub będziesz leżeć przez dłuższy czas (patrz rozdział „Zakrzepy krwi”);
- jeśli kiedykolwiek miałeś zawał serca lub udar;
- jeśli pacjent ma (lub kiedykolwiek miał) dusznicę bolesną (stan, który powoduje silny ból w klatce piersiowej i może być pierwszym objawem zawału serca) lub przemijający napad niedokrwienny (TIA – przejściowe objawy udaru);
jeśli u pacjenta występuje którakolwiek z następujących chorób, które mogą zwiększać ryzyko powstania zakrzepów krwi w tętnicach:
- ciężka cukrzyca z uszkodzeniem naczyń krwionośnych
- bardzo wysokie ciśnienie krwi
- bardzo wysoki poziom tłuszczu (cholesterolu lub trójglicerydów) we krwi
- choroba znana jako hiperhomocysteinemia
nie używaj Nuvaring
- jeśli masz (lub kiedykolwiek miałeś) rodzaj migreny zwany „migreną z aurą”;
- jeśli u pacjenta występuje (lub kiedykolwiek) zapalenie trzustki (zapalenie trzustki) związane z wysokim poziomem tłuszczu we krwi.
- jeśli pacjent ma (lub kiedykolwiek miał) ciężką chorobę wątroby, a czynność wątroby nie wróciła jeszcze do normy.
- jeśli masz (lub kiedykolwiek) łagodny lub złośliwy guz wątroby.
- jeśli pacjentka ma (lub kiedykolwiek miała) lub może mieć raka piersi lub narządów płciowych.
- jeśli masz krwawienie z pochwy niewiadomego pochodzenia.
- jeśli pacjent ma uczulenie na etynyloestradiol lub etonogestrel lub którykolwiek z pozostałych składników tego leku;
Jeśli którykolwiek z tych stanów pojawi się po raz pierwszy podczas używania NuvaRing, natychmiast zdejmij pierścień i skonsultuj się z lekarzem. W międzyczasie stosuj niehormonalne metody antykoncepcji.
Środki ostrożności dotyczące stosowania Informacje ważne przed zastosowaniem leku Nuvaring
Kiedy powinieneś iść do lekarza?
Skontaktuj się z lekarzem w trybie pilnym
- jeśli pacjent zauważy możliwe objawy zakrzepu krwi, które mogą wskazywać na zakrzep krwi w nodze (zakrzepicę żył głębokich), zakrzep krwi w płucu (zator tętnicy płucnej), zawał serca lub udar (patrz punkt poniżej "Zakrzepy krwi").
Opis objawów tych poważnych działań niepożądanych znajduje się w rozdziale „Jak rozpoznać zakrzep krwi”.
Należy poinformować lekarza, jeśli którakolwiek z poniższych sytuacji dotyczy Ciebie. Jeśli ten stan pojawi się lub pogorszy podczas stosowania NuvaRing, należy poinformować o tym lekarza.
- jeśli bliski członek rodziny ma lub kiedykolwiek miał raka piersi;
- jeśli pacjent ma padaczkę (patrz punkt „Interakcje”);
- jeśli u pacjenta występuje choroba wątroby (np. żółtaczka) lub choroba pęcherzyka żółciowego (np. kamienie żółciowe);
- jeśli u pacjenta występuje choroba Leśniowskiego-Crohna lub wrzodziejące zapalenie jelita grubego (przewlekła choroba zapalna jelit);
- jeśli u pacjenta występuje toczeń rumieniowaty układowy (SLE, choroba, która atakuje naturalny system obronny);
- jeśli u pacjenta występuje zespół hemolityczno-mocznicowy (HUS, zaburzenie krzepnięcia krwi powodujące niewydolność nerek);
- jeśli u pacjenta występuje niedokrwistość sierpowatokrwinkowa (dziedziczna choroba krwinek czerwonych);
- jeśli u pacjenta występuje wysoki poziom tłuszczu we krwi (hipertriglicerydemia) lub „dodatni wywiad rodzinny dotyczący tej choroby”. Hipertriglicerydemia jest związana ze zwiększonym ryzykiem rozwoju zapalenia trzustki;
- jeśli planujesz „operację” lub będziesz leżeć przez dłuższy czas (patrz rozdział „Zakrzepy krwi”);
- jeśli właśnie urodziłaś, ryzyko powstania zakrzepów krwi jest wyższe.Zapytaj swojego lekarza, jak szybko po porodzie możesz zacząć stosować NuvaRing;
- jeśli masz „zapalenie żył pod skórą (zakrzepowe zapalenie żył powierzchownych);
- jeśli masz żylaki;
- jeśli u pacjentki występuje stan, który wystąpił po raz pierwszy lub pogorszył się podczas ciąży lub podczas wcześniejszego stosowania hormonów płciowych (np. utrata słuchu, porfiria [zaburzenie krwi], opryszczka ciężarnych [wysypka skórna] z pęcherzami podczas ciąży], choroba Sydenhama pląsawica [choroba nerwów, w której mogą wystąpić nagłe ruchy ciała], dziedziczny obrzęk naczynioruchowy [należy natychmiast zgłosić się do lekarza, jeśli wystąpią objawy obrzęku naczynioruchowego, takie jak obrzęk twarzy, języka i (lub) gardła i (lub) trudności w przełykaniu lub pokrzywka związane z trudnościami w oddychaniu]).
- jeśli u pacjentki występuje (lub kiedykolwiek) ostuda (żółtawo-brązowe plamy pigmentacyjne, tak zwane „plamy ciążowe”, zwłaszcza na twarzy). Jeśli tak, unikaj długotrwałej ekspozycji na słońce lub promienie ultrafioletowe.
- jeśli u pacjenta występuje stan chorobowy utrudniający stosowanie leku NuvaRing, taki jak zaparcia, wypadanie szyjki macicy lub ból podczas stosunku.
ZAKRZEPY
Stosowanie złożonych hormonalnych środków antykoncepcyjnych, takich jak NuvaRing, zwiększa ryzyko powstania zakrzepów krwi w porównaniu z ich niestosowaniem. W rzadkich przypadkach zakrzep krwi może blokować naczynia krwionośne i powodować poważne problemy. Mogą powstać zakrzepy krwi.
w żyłach (tzw. „zakrzepica żylna”, „żylna choroba zakrzepowo-zatorowa” lub VTE)
w tętnicach (określanych jako „zakrzepica tętnicza”, „tętnicza choroba zakrzepowo-zatorowa” lub ATE).
Odzyskiwanie zakrzepów krwi nie zawsze jest całkowite. Rzadko mogą wystąpić długotrwałe, poważne skutki lub bardzo rzadko mogą być śmiertelne.
Należy pamiętać, że ogólne ryzyko powstania szkodliwego zakrzepu krwi związanego z NuvaRing jest niskie.
JAK ROZPOZNAĆ ZAKRZECH KRWI?
Natychmiast skontaktuj się z lekarzem, jeśli zauważysz którykolwiek z poniższych objawów.
- obrzęk jednej nogi lub wzdłuż żyły w nodze lub stopie, zwłaszcza w towarzystwie:
- ból lub tkliwość w nodze, która może być odczuwana tylko podczas stania lub chodzenia
- zwiększone czucie ciepła w chorej nodze
- zmiana koloru skóry na nodze, np. bladość, zaczerwienienie lub zasinienie
- nagła i niewyjaśniona duszność lub szybki oddech;
- nagły kaszel bez wyraźnej przyczyny, prawdopodobnie powodujący wydzielanie krwi;
- ostry ból w klatce piersiowej, który może nasilać się przy głębokim oddychaniu;
- silne zawroty głowy lub zawroty głowy;
- szybkie lub nieregularne bicie serca;
- silny ból w żołądku
- natychmiastowa utrata wzroku lub
- bezbolesne niewyraźne widzenie, które może prowadzić do utraty wzroku
- ból w klatce piersiowej, dyskomfort, uczucie ucisku lub ciężkości
- uczucie ściskania lub pełności w klatce piersiowej, ramieniu lub poniżej mostka;
- uczucie pełności, niestrawności lub zadławienia;
- dyskomfort w górnej części ciała promieniujący do pleców, szczęki, gardła, ramion i żołądka;
- pocenie się, nudności, wymioty lub zawroty głowy;
- skrajne osłabienie, niepokój lub duszność;
- szybkie lub nieregularne bicie serca
- nagłe drętwienie lub osłabienie twarzy, ręki lub nogi, zwłaszcza po jednej stronie ciała;
- nagłe splątanie, trudności w mówieniu lub rozumieniu;
- nagła trudność widzenia w jednym lub obu oczach;
- nagłe trudności w chodzeniu, zawroty głowy, utrata równowagi lub koordynacji;
- nagła, ciężka lub przedłużająca się migrena bez znanej przyczyny;
- utrata przytomności lub omdlenia z drgawkami lub bez drgawek.
- obrzęk i bladoniebieskie przebarwienie jednej kończyny;
- silny ból brzucha (ostry brzuch).
ZAKRZEPY KRWI W ŻYLE
Co może się stać, jeśli w żyle powstanie zakrzep krwi?
- Stosowanie złożonych hormonalnych środków antykoncepcyjnych wiąże się ze zwiększonym ryzykiem powstawania zakrzepów krwi w żyłach (zakrzepica żylna), jednak te działania niepożądane występują rzadko i w większości przypadków występują w pierwszym roku stosowania złożonych hormonalnych środków antykoncepcyjnych.
- Jeśli w żyle nogi lub stopy utworzy się zakrzep krwi, może to spowodować zakrzepicę żył głębokich (DVT).
- Jeśli skrzep krwi przemieści się z nogi i ulokuje się w płucu, może spowodować „zator tętnicy płucnej”.
- Bardzo rzadko zakrzep może powstać w innym narządzie, takim jak oko (zakrzepica żył siatkówki).
Kiedy ryzyko powstania zakrzepu krwi w żyle jest największe?
Ryzyko powstania zakrzepu krwi w żyle jest największe w pierwszym roku stosowania złożonego hormonalnego środka antykoncepcyjnego po raz pierwszy. Ryzyko może być jeszcze większe, jeśli wznowisz przyjmowanie złożonych hormonalnych środków antykoncepcyjnych (tego samego lub innego leku) po przerwie trwającej 4 lub więcej tygodni.
Po pierwszym roku ryzyko jest zmniejszone, ale zawsze jest nieco wyższe niż w przypadku, gdy nie stosowałaś złożonych hormonalnych środków antykoncepcyjnych.
Po przerwaniu stosowania leku NuvaRing ryzyko powstania zakrzepów krwi wraca do normy w ciągu kilku tygodni.
Jakie jest ryzyko powstania zakrzepów krwi?
Ryzyko zależy od naturalnego ryzyka wystąpienia ŻChZZ i rodzaju przyjmowanego złożonego hormonalnego środka antykoncepcyjnego.
Ogólne ryzyko powstania zakrzepu krwi w nodze lub płucu (ZŻG lub ZP) przy stosowaniu NuvaRing jest niskie.
- Na 10 000 kobiet, które nie stosują złożonych hormonalnych środków antykoncepcyjnych i nie są w ciąży, u około 2 w ciągu roku powstanie zakrzep krwi.
- Na 10 000 kobiet, które stosują złożone hormonalne środki antykoncepcyjne zawierające lewonorgestrel, noretysteron lub norgestimat, w ciągu roku u około 5-7 wystąpią zakrzepy krwi.
- Na 10 000 kobiet stosujących złożone hormonalne środki antykoncepcyjne zawierające norelgestromin lub etonorgestrel, takie jak NuvaRing, w ciągu roku u około 6-12 wystąpią zakrzepy krwi.
- Ryzyko powstania zakrzepów krwi zależy od historii choroby (patrz „Czynniki zwiększające ryzyko powstania zakrzepów krwi”).
Czynniki zwiększające ryzyko powstania zakrzepów krwi w żyle
Ryzyko powstania zakrzepów krwi z NuvaRing jest niskie, ale niektóre stany zwiększają to ryzyko. Jego ryzyko jest większe:
- jeśli masz znaczną nadwagę (wskaźnik masy ciała lub BMI powyżej 30 kg/m2);
- jeśli bliski krewny miał zakrzep krwi w nodze, płucu lub innym narządzie w młodym wieku (mniej niż około 50 lat). W takim przypadku możesz mieć dziedziczne zaburzenie krzepnięcia krwi;
- w przypadku planowanego zabiegu chirurgicznego, konieczności leżenia przez dłuższy czas z powodu urazu lub choroby lub w przypadku założonej nogi w gipsie.Może być konieczne przerwanie stosowania leku NuvaRing na kilka tygodni przed zabiegiem lub w okres, w którym pacjent jest mniej mobilny.W przypadku konieczności przerwania stosowania leku NuvaRing należy zapytać lekarza, kiedy można ponownie rozpocząć przyjmowanie leku NuvaRing;
- z wiekiem (szczególnie powyżej 35 roku życia);
- jeśli urodziłaś mniej niż kilka tygodni temu.
Ryzyko powstania zakrzepów krwi wzrasta, im więcej masz tego typu schorzeń.
Podróż samolotem (trwająca > 4 godziny) może tymczasowo zwiększyć ryzyko powstania zakrzepów krwi, zwłaszcza jeśli u pacjenta występują inne wymienione czynniki ryzyka
Ważne jest, aby poinformować lekarza, jeśli którekolwiek z powyższych dotyczy Ciebie, nawet jeśli nie masz pewności. Lekarz może zdecydować o zaprzestaniu przyjmowania leku NuvaRing.Jeśli którykolwiek z powyższych stanów ulegnie zmianie podczas stosowania leku NuvaRing, na przykład jeśli u bliskiego krewnego występuje zakrzepica bez znanej przyczyny lub jeśli pacjent przytyje, należy skontaktować się z lekarzem.
ZAKRZEPY KRWI W TĘTNICY
Co może się stać, jeśli w „tętnicy” utworzy się skrzep krwi?
Podobnie jak zakrzepy krwi w żyle, zakrzepy w tętnicy mogą powodować poważne problemy, na przykład mogą powodować zawał serca lub udar.
Czynniki zwiększające ryzyko powstania zakrzepów krwi w tętnicy
Należy zauważyć, że ryzyko zawału serca lub udaru związanego ze stosowaniem NuvaRing jest bardzo niskie, ale może wzrosnąć:
- z wiekiem (powyżej 35 lat);
- jeśli palisz. Podczas stosowania złożonych hormonalnych środków antykoncepcyjnych, takich jak NuvaRing, zaleca się rzucenie palenia. Jeśli nie możesz rzucić palenia i masz więcej niż 35 lat, lekarz może zalecić stosowanie innego rodzaju środka antykoncepcyjnego;
- jeśli masz nadwagę;
- jeśli masz wysokie ciśnienie krwi;
- jeśli członek Twojej najbliższej rodziny miał zawał serca lub udar w młodym wieku (mniej niż około 50 lat). W takim przypadku możesz również być narażony na wysokie ryzyko zawału serca lub udaru mózgu;
- jeśli u pacjenta lub bliskiego krewnego występuje wysoki poziom tłuszczów we krwi (cholesterolu lub trójglicerydów);
- jeśli cierpisz na migreny, zwłaszcza migreny z aurą;
- jeśli u pacjenta występują jakiekolwiek problemy z sercem (wada zastawki, zaburzenie rytmu serca zwane migotaniem przedsionków);
- jeśli masz cukrzycę.
Jeśli masz więcej niż jeden z tych stanów lub jeśli którykolwiek z nich jest szczególnie ciężki, ryzyko powstania zakrzepu krwi może być jeszcze wyższe.
Jeśli którykolwiek z powyższych stanów ulegnie zmianie podczas stosowania NuvaRing, na przykład, jeśli zaczniesz palić, jeśli bliski krewny ma zakrzepicę bez znanej przyczyny lub jeśli znacznie przytyjesz, skontaktuj się z lekarzem.
Guzy
Poniższe informacje zostały uzyskane w badaniach COC i można je również zastosować do NuvaRing.
Brak dostępnych informacji na temat dopochwowego podawania hormonów antykoncepcyjnych (takich jak NuvaRing). Rozpoznanie raka piersi jest nieco częstsze u kobiet stosujących tabletki złożone, ale nie wiadomo, czy jest to spowodowane leczeniem. Na przykład może się zdarzyć, że nowotwory występują częściej u kobiet przyjmujących dwuskładnikową pigułkę, ponieważ są one częściej sprawdzane przez lekarza. Po odstawieniu tabletki złożonej wzrost zachorowalności na raka piersi stopniowo się zmniejsza.
Ważne jest, aby regularnie sprawdzać piersi i skontaktować się z lekarzem, gdy tylko poczujesz guzek. Należy również poinformować lekarza, jeśli bliski krewny ma lub kiedykolwiek miał raka piersi (patrz punkt 2.2 „Ostrzeżenia i środki').
U kobiet przyjmujących pigułki rzadko zgłaszano łagodne guzy wątroby, a w mniejszej liczbie przypadków złośliwe guzy wątroby. Skonsultuj się z lekarzem w przypadku nietypowego silnego bólu brzucha.
U kobiet stosujących tabletki złożone rzadziej występuje rak endometrium (wyściółki macicy) i rak jajników. Może tak być również w przypadku NuvaRing, ale nie zostało to potwierdzone.
Interakcje Jakie leki lub pokarmy mogą zmienić działanie Nuvaring
Zawsze informuj lekarza przepisującego NuvaRing o wszelkich lekach lub produktach ziołowych, które już przyjmujesz, a także informuj innych lekarzy lub dentystów (lub farmaceutę wydającego leki), którzy przepisują inne leki, o stosowaniu leku NuvaRing, aby mogli ustalić, czy i w jakim celu długo konieczne jest stosowanie dodatkowych metod antykoncepcji.
Niektóre leki mogą powodować szczególne problemy podczas stosowania hormonalnych środków antykoncepcyjnych, takich jak NuvaRing.
Istnieją leki, które mogą prowadzić do zmniejszenia skuteczności antykoncepcyjnej NuvaRing lub spowodować nieoczekiwane krwawienie, w tym leki stosowane w leczeniu:
- „padaczka (np. prymidon, fenytoina, barbiturany, karbamazepina, okskarbazepina, topiramat, felbamat);
- gruźlica (np. ryfampicyna);
- zakażenie wirusem HIV (np. rytonawir);
- inne choroby zakaźne (np. gryzeofulwina i antybiotyki, z wyjątkiem amoksycyliny i doksycykliny, co do których wykazano, że nie wpływają na uwalnianie hormonów przez NuvaRing).
- Produkt ziołowy o nazwie ziele dziurawca również może wpływać na skuteczność NuvaRing.Jeśli chcesz stosować produkty zawierające ziele dziurawca podczas stosowania NuvaRing, powinieneś najpierw skonsultować się z lekarzem.
- NuvaRing może również zakłócać działanie innych leków, takich jak cyklosporyna i przeciwpadaczkowa lamotrygina.
Wkładki chłonne mogą być używane podczas korzystania z NuvaRing. Włóż NuvaRing przed włożeniem wkładki. Podczas wyjmowania wkładki należy zachować szczególną ostrożność, aby zapobiec przypadkowemu wyrzuceniu pierścienia. W takim przypadku po prostu umyj pierścień w zimnej lub letniej wodzie i natychmiast załóż go ponownie.
Stosowanie produktów plemnikobójczych lub drożdży dopochwowych nie zmniejsza skuteczności antykoncepcyjnej NuvaRing.
Ostrzeżenia Ważne jest, aby wiedzieć, że:
Dzieci i młodzież
Nie badano bezpieczeństwa i skuteczności produktu NuvaRing u młodzieży w wieku poniżej 18 lat.
Testy laboratoryjne
W przypadku wykonywania badań krwi lub moczu należy poinformować lekarza o stosowaniu NuvaRing, ponieważ może to zmienić wyniki niektórych badań.
Ciąża i karmienie piersią
NuvaRing nie wolno stosować, jeśli pacjentka jest w ciąży lub podejrzewa, że jest w ciąży. Jeśli zajdziesz w ciążę podczas stosowania NuvaRing, musisz zdjąć pierścień i skontaktować się z lekarzem.
Jeśli chcesz przestać używać NuvaRing, ponieważ chcesz zajść w ciążę, zapoznaj się z rozdziałem „Kiedy chcesz przestać używać NuvaRing”.
NuvaRing nie jest zalecany w okresie karmienia piersią.Jeśli pacjentka chce stosować NuvaRing podczas karmienia piersią, powinna zasięgnąć porady lekarza.
Prowadzenie i używanie maszyn
Jest mało prawdopodobne, aby NuvaRing wpływał na zdolność prowadzenia pojazdów i obsługiwania maszyn.
Dawkowanie i sposób użycia Jak stosować Nuvaring: Dawkowanie
NuvaRing włożysz do pochwy i sam go wyjmiesz. Lekarz poinstruuje Cię, kiedy rozpocząć stosowanie NuvaRing po raz pierwszy. Pierścień dopochwowy należy założyć w odpowiednim dniu cyklu miesiączkowego (patrz rozdział „Kiedy zacząć od pierwszego pierścienia”) i pozostawić w pochwie przez 3 tygodnie z rzędu.Dobrą praktyką jest regularne sprawdzanie, czy pierścień nadal znajduje się w pochwie. Po trzecim tygodniu zdejmij NuvaRing i zrób tygodniową przerwę. Zwykle cykl menstruacyjny występuje podczas tego okresu bez pierścienia.
Jak wkładać i wyjmować NuvaRing
- Przed włożeniem pierścienia sprawdź, czy nie wygasł (patrz „Jak przechowywać NuvaRing”).
- Umyj ręce przed włożeniem lub wyjęciem pierścienia.
- Wybierz pozycję, która jest dla Ciebie najwygodniejsza, np. stanie z jedną nogą uniesioną, kucanie lub leżenie.
- Wyjmij NuvaRing z saszetki.
- Trzymaj pierścień między kciukiem a palcem wskazującym, ściśnij go i delikatnie włóż do pochwy. Po włożeniu NuvaRing nie powinno nic słyszeć. Jeśli poczujesz dyskomfort, delikatnie wepchnij NuvaRing głębiej do pochwy. Dokładna pozycja pierścienia w pochwie nie jest ważna.
- Po 3 tygodniach wyjmij NuvaRing z pochwy. NuvaRing można usunąć, zaczepiając palec wskazujący pod przednią krawędzią pierścienia lub chwytając za krawędź pierścienia i pociągając na zewnątrz (patrz Rysunek 5).Jeśli zlokalizujesz pierścień w pochwie, ale nie możesz go usunąć, musisz skontaktować się z Twój doktor.
- Zużyty pierścień należy wyrzucić wraz ze zwykłymi odpadami domowymi, najlepiej w zamykanym worku. Nie wyrzucaj NuvaRing do toalety.
Trzy tygodnie z założonym pierścieniem, tydzień bez
- Od dnia założenia pierścień dopochwowy powinien być trzymany w pochwie bez przerwy przez 3 tygodnie.
- Po 3 tygodniach wyjmij pierścień w tym samym dniu tygodnia, w którym został założony, mniej więcej o tej samej godzinie.Na przykład, jeśli NuvaRing zostanie założony w środę około godziny 22:00, pierścień musi zostać usunięty w środę trzeciego w następnym tygodniu, około godziny 22:00.
- Po usunięciu nie należy używać pierścienia przez 1 tydzień. Krwawienie z pochwy powinno wystąpić w tym tygodniu. Zwykle rozpoczyna się 2-3 dni po usunięciu NuvaRing.
- Zacznij od nowego pierścienia dokładnie po 1 tygodniu przerwy (ponownie tego samego dnia tygodnia i mniej więcej o tej samej porze), nawet jeśli krwawienie z pochwy jeszcze się nie skończyło. Jeśli nowy pierścień zostanie założony ponad 3 godziny później, ochrona przed ciążą może być zmniejszona. W takim przypadku postępuj zgodnie z instrukcjami podanymi w akapicie „Co zrobić, jeśli ... zapomnisz włożyć nowy pierścień po przerwie bez pierścienia ".
Jeśli NuvaRing jest stosowany w sposób opisany powyżej, krwawienie z pochwy będzie pojawiać się co miesiąc mniej więcej w te same dni.
Kiedy zacząć od pierwszego dzwonka?
- Jeśli w ciągu ostatniego miesiąca nie stosowałaś hormonalnych środków antykoncepcyjnych
Pierwszy NuvaRing należy założyć pierwszego dnia naturalnego cyklu (tj. pierwszego dnia cyklu miesiączkowego). NuvaRing zaczyna działać natychmiast. Nie jest konieczne podejmowanie innych środków antykoncepcyjnych.
Rozpoczęcie stosowania NuvaRing między 2 a 5 dniem jest dozwolone, ale jeśli odbyłeś stosunek płciowy w ciągu pierwszych 7 dni stosowania NuvaRing, upewnij się, że stosujesz również dodatkową metodę antykoncepcji (np. prezerwatywę). Tej rady należy przestrzegać tylko przy pierwszym użyciu NuvaRing.
- Jeśli w ostatnim miesiącu stosowałaś złożony doustny środek antykoncepcyjny (pigułkę)
Rozpocznij stosowanie NuvaRing najpóźniej dzień po przerwie w stosowaniu obecnej pigułki.Jeśli opakowanie zawiera również nieaktywne tabletki, zacznij używać NuvaRing najpóźniej dzień po ostatniej nieaktywnej tabletce. Jeśli nie masz pewności, który to jest, skonsultuj się z lekarzem lub farmaceutą. Nigdy nie przedłużaj przerwy w stosowaniu hormonów w obecnym opakowaniu tabletek poza zalecaną długość.
Jeśli regularnie i prawidłowo stosowałaś pigułkę i jeśli masz pewność, że nie jesteś w ciąży, możesz również przerwać przyjmowanie pigułki w dowolnym dniu bieżącego opakowania i natychmiast rozpocząć stosowanie NuvaRing.
- Jeśli pacjent stosował system transdermalny w ciągu ostatniego miesiąca
Rozpocznij stosowanie NuvaRing najpóźniej dzień po zwykłym odstępie czasu bez plastra. Nigdy nie wydłużaj okresu bez plastra poza zalecany czas
Jeśli plastra stosowałaś konsekwentnie i prawidłowo oraz jeśli masz pewność, że nie jesteś w ciąży, możesz również przerwać stosowanie plastra w dowolnym dniu i natychmiast rozpocząć stosowanie NuvaRing.
- Jeśli w ciągu ostatniego miesiąca stosowałaś pigułkę zawierającą tylko progestagen (minipigułkę)
Minipigułkę można przerwać w dowolnym dniu i rozpocząć stosowanie NuvaRing następnego dnia o tej samej porze, o której normalnie przyjmowałbyś pigułkę. Pamiętaj o stosowaniu dodatkowej metody antykoncepcji (np. prezerwatywy) przez pierwsze 7 dni używania pierścienia.
- Jeśli w ciągu ostatniego miesiąca stosowałaś wstrzyknięcie lub implant uwalniający progestagen lub wkładkę domaciczną
Rozpocznij stosowanie NuvaRing w dniu nowego wstrzyknięcia lub w dniu usunięcia implantu lub pierścienia domacicznego uwalniającego progestagen.
- Po porodzie
Jeśli właśnie urodziłaś dziecko, lekarz zaleci Ci poczekać do pierwszego naturalnego cyklu przed rozpoczęciem stosowania NuvaRing. W niektórych przypadkach można zacząć wcześniej. Uzyskaj poradę od swojego lekarza. Nawet jeśli chcesz używać NuvaRing podczas karmienia piersią, najpierw skonsultuj się z lekarzem.
- Po aborcji naturalnej lub chirurgicznej
Skonsultuj się z lekarzem.
Co zrobić, jeśli ...
Pierścień został przypadkowo wyrzucony z pochwy
NuvaRing może przypadkowo wypaść z pochwy, jeśli np. nie został prawidłowo założony, podczas wyjmowania tamponu, podczas stosunku płciowego, w związku z zaparciami lub wypadaniem macicy, dlatego należy regularnie sprawdzać, czy pierścień jest wciąż w pochwie.
Jeśli pierścień zostanie pozostawiony poza pochwą na mniej niż 3 godziny, nadal będzie chronić Cię przed ciążą.Wypłucz pierścień w zimnej lub letniej (nie gorącej) wodzie i załóż go ponownie. Jeśli pierścień jest pozostawiony poza pochwą na dłużej niż 3 godziny, może nie ochronić Cię przed ciążą.Patrz informacje w części „Co zrobić, gdy… pierścień jest chwilowo poza pochwą”.
Pierścień tymczasowo pozostaje poza pochwą
W pochwie NuvaRing powoli uwalnia hormony do organizmu, aby zapobiec ciąży. Jeśli pierścień pozostaje poza pochwą dłużej niż 3 godziny, może nie ochronić Cię przed ciążą, dlatego też pierścień nie powinien pozostawać poza pochwą dłużej niż 3 godziny w ciągu 24 godzin.
- Jeśli pierścień znajdował się poza pochwą przez mniej niż 3 godziny, nadal może chronić Cię przed ciążą. Załóż pierścień ponownie tak szybko, jak to możliwe, ale najpóźniej w ciągu 3 godzin
- Jeśli pierścień pozostaje poza pochwą lub podejrzewasz, że był poza pochwą przez ponad 3 godziny w pierwszym i drugim tygodniu, może to nie ochronić cię przed ciążą. Pamiętaj, aby to zrobić i pozostawić pierścień w pochwie bez przerwa trwająca co najmniej 7 dni Jeśli uprawiasz seks w ciągu tych 7 dni, użyj prezerwatywy Jeśli jesteś w pierwszym tygodniu i uprawiałaś seks w ciągu ostatnich 7 dni, istnieje możliwość, że możesz być w ciąży. Jeśli tak, skontaktuj się z lekarzem.
- Jeśli pierścień pozostaje poza pochwą lub podejrzewasz, że znajdował się poza pochwą przez ponad 3 godziny w trzecim tygodniu, może nie ochronić Cię przed ciążą. Wyrzuć ten pierścień i wybierz jedną z następujących dwóch opcji:
- natychmiast włóż nowy pierścień. Rozpocznie się następny 3-tygodniowy okres użytkowania. Cykl menstruacyjny może się nie pojawić, ale może wystąpić plamienie lub przełomowe krwawienie.
- Nie zakładaj ponownie pierścienia. Poczekaj, aż pojawi się miesiączka i załóż nowy pierścień nie później niż 7 dni po usunięciu lub wyjęciu poprzedniego pierścienia. Tę opcję należy wybrać tylko wtedy, gdy NuvaRing był używany w sposób ciągły w poprzednim 7 dni.
Pierścień pęka NuvaRing bardzo rzadko może pęknąć.
Jeśli zauważysz, że pierścień NuvaRing się zepsuł, wyrzuć ten pierścień i jak najszybciej załóż nowy pierścień.Zastosuj dodatkowe środki antykoncepcyjne (np. prezerwatywę) przez następne 7 dni.Jeśli odbyłaś stosunek seksualny, zanim zauważyłaś pęknięcie pierścienia pierścień, skonsultuj się z lekarzem.
Włożono więcej niż jeden pierścień
Nie zgłoszono żadnych poważnych działań niepożądanych związanych z przedawkowaniem hormonów NuvaRing. Jeśli przypadkowo założyłaś więcej niż jeden pierścień, możesz mieć nudności, wymioty lub krwawienie z pochwy. Usuń nadmiar pierścieni i skonsultuj się z lekarzem, jeśli takie objawy nie ustąpią. Zapomniałeś o założeniu nowego pierścienia po przerwie bez pierścienia Jeśli przerwa bez pierścienia wynosi więcej niż 7 dni, załóż nowy pierścień, gdy tylko sobie o tym przypomnisz.W przypadku stosunku płciowego zastosuj również inną metodę antykoncepcji (np. prezerwatywę). , przez następne 7 dni.Jeśli odbyłaś stosunek płciowy w okresie przerwy, należy rozważyć możliwość zajścia w ciążę. Natychmiast porozmawiaj z lekarzem. Im dłuższa przerwa bez pierścienia, tym większe ryzyko zajścia w ciążę.
Zapomniałeś zdjąć pierścionek
- Jeśli Twój pierścionek jest na miejscu dłużej niż 3, ale nie dłużej niż 4 tygodnie. Nadal może chronić Cię przed ciążą. Wykonaj regularną tygodniową przerwę bez pierścienia, a następnie załóż nowy pierścień.
- Jeśli Twój pierścień był zakładany dłużej niż 4 tygodnie, istnieje możliwość zajścia w ciążę.Skontaktuj się z lekarzem przed założeniem nowego pierścienia.
Nie ma miesiączki
- NuvaRing był używany zgodnie z instrukcjami
Jeśli nie wystąpiła miesiączka, ale NuvaRing był stosowany zgodnie z instrukcją i nie przyjmowała żadnych innych leków, jest bardzo mało prawdopodobne, że zaszła w ciążę. Kontynuuj używanie NuvaRing jak zwykle. Jeśli jednak miesiączka nie wystąpi dwa razy z rzędu, możliwe, że jesteś w ciąży. Natychmiast skonsultuj się z lekarzem. Nie zaczynaj od nowego NuvaRing, dopóki lekarz nie wykluczy ciąży.
- NuvaRing nie był używany zgodnie z zaleceniami
Jeśli przegapiłaś miesiączkę i nie postępowałaś zgodnie z podanymi instrukcjami i nie miałaś oczekiwanej miesiączki podczas następnej przerwy bez pierścienia, możesz być w ciąży. Przed rozpoczęciem stosowania nowego pierścienia NuvaRing należy skontaktować się z lekarzem.
Masz nieoczekiwane krwawienie
Podczas stosowania NuvaRing niektóre kobiety mogą doświadczać nieoczekiwanego krwawienia z pochwy między miesiączkami. Może być konieczne zastosowanie ochrony higienicznej. W każdym razie pozostaw pierścień w pochwie i używaj go normalnie. Skonsultuj się z lekarzem, jeśli nieregularne krwawienie utrzymuje się, nasila się lub nawraca.
Chcesz zmienić pierwszy dzień swojego cyklu miesiączkowego
Jeśli stosujesz NuvaRing zgodnie z zaleceniami, cykl menstruacyjny (krwawienie z odstawienia) rozpocznie się w okresie bez pierścienia.Jeśli chcesz zmienić dzień rozpoczęcia miesiączki, możesz skrócić okres bez pierścienia (nigdy nie wydłużaj tego okresu!)
Na przykład, jeśli twój okres zwykle zaczyna się w piątek, możesz zmienić na wtorek (3 dni wcześniej) od następnego miesiąca. Po prostu załóż następny NuvaRing 3 dni wcześniej niż zwykle.
Jeśli przerwa w stosowaniu pierścienia jest bardzo krótka (np. 3 dni lub krócej), krwawienie może nie występować, ale mogą wystąpić plamienie (krople lub plamki krwi) lub krwawienie podczas stosowania następnego pierścienia.
Jeśli nie masz pewności, jak postępować, skontaktuj się z lekarzem w celu uzyskania wyjaśnień.
Chcesz odłożyć miesiączkę
Chociaż nie jest to zalecane, możliwe jest opóźnienie miesiączki (krwawienie z odstawienia) poprzez założenie nowego pierścienia natychmiast po zdjęciu starego, bez robienia przerwy bez pierścienia. Nowy pierścień może pozostać włożony do 3 tygodni. Podczas używania nowego pierścienia mogą wystąpić plamienie (krople lub plamki krwi) lub przełomowe krwawienie. Zdejmij pierścień, gdy zdecydujesz się na miesiączkę. Przestrzegaj regularnego tygodniowego okresu bezobrączkowego, a następnie załóż nowy pierścień.
Możesz poprosić swojego lekarza o poradę przed podjęciem decyzji o opóźnieniu miesiączki.
Kiedy chcesz przestać używać Nuvaring
Możesz przestać używać NuvaRing, kiedy tylko chcesz.
Jeśli nie chcesz zajść w ciążę, skonsultuj się z lekarzem w sprawie innych metod kontroli urodzeń.
Jeśli przestaniesz stosować NuvaRing, ponieważ chcesz zajść w ciążę, musisz poczekać na swój naturalny cykl przed próbą zajścia w ciążę.Pomoże to obliczyć przewidywaną datę porodu.
Skutki uboczne Jakie są skutki uboczne Nuvaring
Jak każdy lek, NuvaRing może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
W przypadku wystąpienia jakichkolwiek działań niepożądanych, zwłaszcza ciężkich lub uporczywych, lub jakichkolwiek zmian w stanie zdrowia, które mogą być spowodowane stosowaniem leku NuvaRing, należy poinformować o tym lekarza.
U wszystkich kobiet stosujących złożone hormonalne środki antykoncepcyjne występuje zwiększone ryzyko powstania zakrzepów krwi w żyłach (żylna choroba zakrzepowo-zatorowa) lub zakrzepów krwi w tętnicach (tętnicza choroba zakrzepowo-zatorowa). Bardziej szczegółowe informacje na temat różnych zagrożeń związanych z „stosowaniem złożonych hormonalnych środków antykoncepcyjnych” można znaleźć w części „Co należy wiedzieć przed zastosowaniem NuvaRing”.
Jeśli pacjent ma uczulenie na którykolwiek ze składników NuvaRing (nadwrażliwość), mogą wystąpić następujące objawy (częstość nieznana): obrzęk naczynioruchowy [obrzęk twarzy, języka i (lub) gardła i (lub) trudności w połykaniu] lub pokrzywka związana z trudnościami w oddechowy. W takim przypadku należy zdjąć NuvaRing i natychmiast skonsultować się z lekarzem.
Następujące działania niepożądane zostały zgłoszone podczas stosowania NuvaRing:
Często: mogą dotyczyć nie więcej niż 1 na 10 kobiet
- ból brzucha; mdłości (nudności)
- grzybica pochwy (np. „Candida”); dyskomfort pochwy z powodu pierścienia, swędzenie w okolicy narządów płciowych; wydzieliny z pochwy
- ból głowy lub migrena; depresyjny nastrój; obniżone libido
- bóle piersi; ból miednicy; bolesne miesiączki
- trądzik
- przybranie na wadze
- wyrzucenie pierścienia
Niezbyt często: mogą dotyczyć nie więcej niż 1 na 100 kobiet
- zaburzenia widzenia; zawroty głowy
- obrzęk brzucha; wymioty, biegunka lub zaparcia
- uczucie zmęczenia, złe samopoczucie lub rozdrażnienie; zmiany nastroju; wahania nastroju
- nadmiar płynu w tkankach (obrzęk)
- zakażenie dróg moczowych lub pęcherza moczowego
- trudności lub ból w oddawaniu moczu; silna potrzeba oddawania moczu; częstsze oddawanie moczu
- problemy podczas stosunku, w tym ból, krwawienie lub odczuwanie pierścienia przez partnera
- podwyższone ciśnienie krwi
- zwiększony apetyt
- ból pleców; skurcze mięśni; ból w nogach lub ramionach
- zmniejszona wrażliwość skóry
- obolałe lub powiększone piersi; mastopatia włóknisto-torbielowata (torbiele piersi, które mogą puchnąć i powodować ból)
- zapalenie szyjki macicy; polipy szyjki macicy (wzrosty w szyjce macicy); wyrzucenie krawędzi szyjki macicy (ektropium)
- zmiany w cyklu menstruacyjnym (np. miesiączki mogą być obfite, długie, nieregularne lub mogą całkowicie ustać); zaburzenia w okolicy miednicy; zespół napięcia przedmiesiączkowego; skurcze macicy
- infekcje pochwy (grzybicze i bakteryjne); pieczenie, nieprzyjemny zapach, ból, dyskomfort lub suchość pochwy lub sromu
- wypadanie włosów, egzema, swędzenie, wysypka lub uderzenia gorąca
- pęknięcie pierścienia
Rzadko: mogą dotyczyć nie więcej niż 1 na 1000 kobiet
- szkodliwe zakrzepy krwi w żyle lub tętnicy, na przykład: o w nodze lub stopie (ZŻG) lub płucu (ZP), zawał serca, udar lub mini-udar lub przejściowe objawy podobne do objawów „ udaru, znanego jako przemijające niedokrwienie (TIA) lub zakrzepy krwi w wątrobie, żołądku/jelitach, nerkach lub oku Prawdopodobieństwo powstania zakrzepów krwi może być większe, jeśli u pacjenta występują jakiekolwiek inne stany zwiększające to ryzyko (patrz punkt dotyczący stanów zwiększających ryzyko wystąpienia zakrzepy i objawy zakrzepu krwi).
- wydzielina z sutka. Nieznana (częstość nie może być określona na podstawie dostępnych danych)
- ostuda (żółtawo-brązowe plamy na skórze, szczególnie na twarzy)
- dyskomfort w penisie partnera (taki jak podrażnienie, wysypka, swędzenie). W związku ze stosowaniem złożonych hormonalnych środków antykoncepcyjnych zgłaszano występowanie raka piersi i raka wątroby.W celu uzyskania dalszych informacji patrz punkt „Rak”.
Zgłaszanie skutków ubocznych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie możliwe działania niepożądane niewymienione w tej ulotce, należy porozmawiać z lekarzem lub farmaceutą. Możesz również zgłaszać skutki uboczne bezpośrednio za pośrednictwem krajowego systemu zgłaszania na „https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse”. Zgłaszając skutki uboczne, możesz pomóc dostarczyć więcej informacji na temat bezpieczeństwa tego Medycyna
Wygaśnięcie i przechowywanie
Przechowywać w temperaturze poniżej 30°C. Przechowywać w oryginalnym opakowaniu, aby chronić urządzenie przed światłem i wilgocią.
Nie należy stosować NuvaRing, jeśli został wydany ponad 4 miesiące temu. Data wydania jest podana na kartoniku i saszetce.
Nie stosować leku NuvaRing po upływie terminu ważności zamieszczonego na pudełku i saszetce.
Nie używaj NuvaRing, jeśli zauważysz jakiekolwiek zmiany w kolorze pierścienia lub jakiekolwiek inne widoczne oznaki zepsucia.
Zużyty pierścień należy wyrzucić wraz z normalnymi odpadami domowymi, najlepiej w zamykanej saszetce. NuvaRing nie należy wyrzucać do toalety. Podobnie jak w przypadku innych leków, nie należy wyrzucać nieużywanych lub przeterminowanych pierścieni do kanalizacji lub domowych pojemników na odpadki. Należy zapytać farmaceutę, jak usunąć niewykorzystane pierścienie, których się już nie używa. Pomoże to chronić środowisko.
Zawartość opakowania i inne informacje
Co zawiera NuvaRing
- Substancjami czynnymi są: etonogestrel (11,7 mg) i etynyloestradiol (2,7 mg)
- Pozostałe składniki to: kopolimery etylen-octan winylu (28% i 9% octan winylu) (rodzaj plastiku, który nie rozpuszcza się w organizmie) oraz stearynian magnezu.
Etonogestrel i etynyloestradiol są uwalniane z pierścienia w dziennych ilościach odpowiednio 0,120 mg/dzień i 0,015 mg/dzień przez okres 3 tygodni.
Jak wygląda NuvaRing i co zawiera opakowanie
NuvaRing to elastyczny, przezroczysty, bezbarwny lub prawie bezbarwny pierścień o średnicy 54 mm.
Każdy pierścień jest umieszczony w zamykanym woreczku foliowym i zapakowany w pudełko tekturowe wraz z ulotką dla pacjenta. Każde pudełko zawiera 1 lub 3 pierścienie. Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
Ulotka pakietu źródłowego: AIFA (Włoska Agencja Leków). Treść opublikowana w styczniu 2016 r. Przedstawione informacje mogą być nieaktualne.
Aby mieć dostęp do najbardziej aktualnej wersji, warto wejść na stronę AIFA (Włoskiej Agencji Leków). Zastrzeżenie i przydatne informacje.
01.0 NAZWA PRODUKTU LECZNICZEGO
NUVARING 0,120 MG / 0,015 MG CO 24 GODZINY URZĄDZENIE POCHWOWE
02.0 SKŁAD JAKOŚCIOWY I ILOŚCIOWY
NuvaRing zawiera 11,7 mg etonogestrelu i 2,7 mg etynyloestradiolu. Pierścień uwalnia etonogestrel i etynyloestradiol w średnich ilościach odpowiednio 0,120 mg i 0,015 mg co 24 godziny przez okres 3 tygodni.
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
03.0 POSTAĆ FARMACEUTYCZNA
Urządzenie dopochwowe.
NuvaRing to elastyczny, przezroczysty, bezbarwny lub prawie bezbarwny pierścień o średnicy zewnętrznej 54 mm i przekroju 4 mm.
04.0 INFORMACJE KLINICZNE
04.1 Wskazania terapeutyczne
Zapobieganie ciąży.
NuvaRing jest wskazany u kobiet w wieku rozrodczym. Bezpieczeństwo i skuteczność wykazano u kobiet w wieku od 18 do 40 lat.
Decyzję o przepisaniu NuvaRing należy wziąć pod uwagę obecne czynniki ryzyka u poszczególnych kobiet, szczególnie te związane z żylną chorobą zakrzepowo-zatorową (ŻChZZ) oraz porównanie ryzyka ŻChZZ związanego z produktem NuvaRing i tym związanym z innymi złożonymi hormonalnymi środkami antykoncepcyjnymi (patrz punkty 4.3 i 4.4).
04.2 Dawkowanie i sposób podawania
Dawkowanie
Aby osiągnąć skuteczność antykoncepcji, NuvaRing należy stosować zgodnie z zaleceniami (patrz „Jak stosować NuvaRing” i „Jak rozpocząć stosowanie NuvaRing”).
Populacja pediatryczna
Nie badano bezpieczeństwa i skuteczności produktu NuvaRing u młodzieży w wieku poniżej 18 lat.
Sposób podawania
JAK UŻYWAĆ NUVARING
NuvaRing może być wprowadzony do pochwy bezpośrednio przez kobietę. Lekarz powinien poinformować kobietę o sposobie zakładania i wyjmowania pierścienia NuvaRing. Podczas zakładania, kobieta powinna wybrać pozycję, która jest dla niej najwygodniejsza, na przykład stanie z jedną nogą uniesioną, kucanie lub leżenie.NuvaRing należy ścisnąć dwoma palcami i włożyć do pochwy, aż osiągnie wygodną pozycję. Dokładna pozycja NuvaRing w pochwie nie wpływa na działanie antykoncepcyjne pierścienia (patrz Rysunki 1-4).
Po założeniu NuvaRing (patrz „Jak zacząć używać NuvaRing”) pozostaje on w pochwie nieprzerwanie przez 3 tygodnie. Kobieta powinna mieć dobry nawyk regularnego sprawdzania obecności NuvaRing. W przypadku przypadkowego wyrzucenia pierścienia NuvaRing, kobieta powinna postępować zgodnie z instrukcjami podanymi w punkcie 4.2 „Co zrobić, jeśli pierścień zostanie tymczasowo wyrzucony z pochwy” (więcej informacji, patrz również punkt 4.4 „Wyrzucenie”).
NuvaRing należy usunąć po 3 tygodniach stosowania, w tym samym dniu tygodnia, w którym został założony. Po tygodniowej przerwie bez pierścienia można założyć nowy pierścień (na przykład jeśli NuvaRing zostanie założony w środę około godziny 22.00, pierścień musi zostać ponownie usunięty w środę trzeciego tygodnia następującego po nim, około godziny 22.00. Nowy pierścień musi zostać założony w następną środę). NuvaRing można usunąć, zaczepiając palec wskazujący pod pierścieniem lub chwytając pierścień między palcem wskazującym i środkowym i pociągając na zewnątrz (Rysunek 5). Zużyty pierścień należy umieścić w saszetce (przechowywać w miejscu niedostępnym dla dzieci i zwierząt) i wyrzucić zgodnie z opisem w punkcie 6.6 Krwawienie z odstawienia zwykle rozpoczyna się 2-3 dni po usunięciu NuvaRing i może nie być całkowicie zakończone po założeniu nowego pierścienia. do włożenia.
JAK ROZPOCZĄĆ KORZYSTANIE Z NUVARING
Brak antykoncepcji hormonalnej w poprzednim cyklu
NuvaRing należy założyć pierwszego dnia naturalnego cyklu kobiety (tj. pierwszego dnia krwawienia miesiączkowego). Możliwe jest również rozpoczęcie od 2 do 5 dnia cyklu, ale podczas pierwszego cyklu, w pierwszych 7 dniach stosowania NuvaRing, zaleca się dodatkowo zastosowanie metody barierowej.
Zmiana ze złożonego hormonalnego środka antykoncepcyjnego
Kobieta powinna założyć NuvaRing najpóźniej w dniu następującym po zwykłej przerwie w przyjmowaniu tabletek lub plastra lub po ostatniej tabletce placebo poprzedniego złożonego hormonalnego środka antykoncepcyjnego.
Jeśli kobieta konsekwentnie i prawidłowo stosowała poprzednią metodę i ma wystarczającą pewność, że nie jest w ciąży, może również zmienić dotychczasowy złożony hormonalny środek antykoncepcyjny w dowolnym dniu cyklu.
Okres wolny od hormonów poprzedniej metody nigdy nie powinien być przedłużony poza zalecany okres.
Zmiana z metody zawierającej wyłącznie progestagen (minipigułka, implant lub wstrzyknięcie) lub z systemu domacicznego (IUS) uwalniającego progestagen
Kobieta może przestawić się z minitabletki w dowolnym dniu (z implantu lub systemu domacicznego, w dniu usunięcia, z zastrzyku antykoncepcyjnego, gdy nadejdzie nowy zastrzyk), ale w każdym przypadku musi zastosować dodatkową metodę bariery w pierwszej kolejności. 7 dni stosowania NuvaRing.
Po aborcji w pierwszym trymestrze
Kobieta może zacząć natychmiast. W ten sposób nie są konieczne żadne dodatkowe środki antykoncepcyjne. Jeśli pacjentka nie chce rozpocząć natychmiastowego leczenia, powinna postępować zgodnie z instrukcjami zawartymi w części „Brak hormonalnej antykoncepcji w poprzednim cyklu”. W międzyczasie należy zalecić stosowanie alternatywnej metody antykoncepcji.
Po porodzie lub aborcji w drugim trymestrze
Karmienie piersią, patrz punkt 4.6.
Należy zalecić kobiecie rozpoczęcie leczenia w czwartym tygodniu po porodzie lub poronieniu w drugim trymestrze ciąży.W przypadku rozpoczęcia później należy zalecić kobiecie stosowanie dodatkowej metody mechanicznej przez pierwsze 7 dni stosowania. wystąpiła ciąża, należy wykluczyć ciążę lub kobieta musi poczekać na pierwszą miesiączkę przed rozpoczęciem leczenia lekiem NuvaRing.
ODCHYLENIA OD ZALECANEGO DAWKOWANIA
Skuteczność antykoncepcji i kontrola cyklu mogą być zagrożone, jeśli kobieta nie przestrzega zalecanego dawkowania.W przypadku odstępstwa, należy udzielić następujących porad, aby uniknąć utraty skuteczności antykoncepcji:
• Co zrobić, jeśli przerwa bez dzwonka zostanie wydłużona?
Kobieta musi założyć nowy pierścień, gdy tylko sobie o tym przypomni. Przez następne 7 dni należy również stosować metodę mechaniczną, taką jak prezerwatywa. Jeśli stosunek odbył się w okresie bez pierścienia, należy rozważyć możliwość zajścia w ciążę.Im dłuższa przerwa bez pierścienia, tym większe ryzyko zajścia w ciążę.
• Co zrobić, jeśli pierścień zostanie tymczasowo wyrzucony z pochwy?
NuvaRing należy pozostawić w pochwie nieprzerwanie przez 3 tygodnie. Jeśli pierścień zostanie przypadkowo wyrzucony, można go umyć zimną lub letnią (nie gorącą) wodą i należy go natychmiast ponownie założyć.
Jeśli NuvaRing jest pozostawiony poza pochwą na mniej niż 3 godziny, skuteczność antykoncepcji nie zmniejsza się.Kobieta powinna jak najszybciej ponownie założyć pierścień, ale nie później niż w ciągu 3 godzin.
Jeśli NuvaRing pozostaje poza pochwą lub istnieje podejrzenie, że pozostawał poza pochwą przez ponad 3 godziny w 1. lub 2. tygodniu stosowania, skuteczność antykoncepcji może być zmniejszona.Kobieta powinna ponownie założyć pierścień, gdy tylko sobie przypomni. to. Należy stosować metodę barierową, taką jak prezerwatywa, dopóki NuvaRing nie będzie znajdować się w pochwie nieprzerwanie przez 7 dni. Im dłuższy czas przebywania NuvaRing poza pochwą i im bliżej tego okresu jest okres bez pierścienia, tym większe jest ryzyko zajścia w ciążę.
Jeśli pierścień NuvaRing znajdował się poza pochwą lub istnieje podejrzenie, że był poza pochwą przez ponad 3 godziny w trzecim tygodniu trzytygodniowego okresu stosowania, skuteczność antykoncepcji może być zmniejszona.Kobieta powinna wyrzucić ten pierścień i wybrać jeden z następujących dwóch możliwości:
1. Natychmiast włóż nowy pierścień
Uwaga: Założenie nowego pierścienia rozpocznie następny trzytygodniowy okres użytkowania. Kobieta może nie mieć krwawienia z odstawienia w poprzednim cyklu. Może jednak wystąpić plamienie lub krwawienie śródcykliczne.
2. Zrób krwawienie z odstawienia i załóż nowy pierścień nie później niż 7 dni (7 x 24 godziny) od momentu usunięcia lub wyrzucenia poprzedniego pierścienia.
Uwaga: tę opcję należy wybrać tylko wtedy, gdy pierścień był używany nieprzerwanie przez ostatnie 7 dni.
• Co zrobić w przypadku dłuższego używania pierścionka?
Chociaż nie jest to zalecane dawkowanie, skuteczność antykoncepcji jest nadal zadowalająca, o ile NuvaRing był stosowany przez okres do 4 tygodni.Kobieta może zachować tygodniową przerwę w stosowaniu pierścienia, a następnie założyć nowy pierścień.NuvaRing był zakładany dłużej niż Po 4 tygodniach skuteczność antykoncepcji może być zmniejszona, a przed założeniem nowego pierścienia NuvaRing należy wykluczyć możliwość zajścia w ciążę.
Jeśli kobieta nie przestrzegała zalecanego schematu leczenia, a następnie nie wystąpiło krwawienie z odstawienia w następnym okresie bez pierścienia, przed założeniem nowego pierścienia NuvaRing należy wykluczyć możliwość zajścia w ciążę.
JAK PORUSZAĆ LUB Opóźnić cykl menstruacyjny?
Jeśli w wyjątkowych przypadkach konieczne jest opóźnienie cyklu miesiączkowego, kobieta może założyć nowy pierścień bez przestrzegania przerwy bez pierścienia. Następny pierścień może być używany przez kolejne 3 tygodnie.Kobieta może mieć krwawienie lub plamienie z pochwy.Po tym czasie wznowione jest regularne stosowanie NuvaRing po zwyczajowej tygodniowej przerwie bez pierścienia.
Aby przesunąć miesiączkę na inny dzień tygodnia niż ten stosowany w jej obecnym harmonogramie, kobiecie można zalecić skrócenie następnej przerwy bez pierścienia o preferowaną liczbę dni. Im krótsza przerwa bez pierścienia, tym większe ryzyko, że kobieta nie będzie miała krwawienia z odstawienia i może mieć przełomowe krwawienie i plamienie podczas stosowania kolejnego pierścienia.
04.3 Przeciwwskazania
Złożonych hormonalnych środków antykoncepcyjnych (COC) nie należy stosować w następujących stanach.
Jeśli którykolwiek z tych stanów pojawi się po raz pierwszy podczas korzystania z NuvaRing, należy go natychmiast usunąć.
• Występowanie lub ryzyko żylnej choroby zakrzepowo-zatorowej (ŻChZZ) lub żylnej choroby zakrzepowo-zatorowej – obecna (z lekiem przeciwzakrzepowym) lub przebyta ŻChZZ (np. zakrzepica żył głębokich [ZŻG] lub zatorowość płucna [ZP])
• Rozpoznana dziedziczna lub nabyta predyspozycja do żylnej choroby zakrzepowo-zatorowej, taka jak oporność na aktywowane białko C (w tym czynnik V Leiden), niedobór antytrombiny III, niedobór białka C, niedobór białka S
• Duży zabieg chirurgiczny z przedłużonym unieruchomieniem (patrz punkt 4.4)
• Wysokie ryzyko żylnej choroby zakrzepowo-zatorowej ze względu na obecność wielu czynników ryzyka (patrz punkt 4.4).
• Obecność lub ryzyko tętniczej choroby zakrzepowo-zatorowej (ATE) lub tętniczej choroby zakrzepowo-zatorowej – obecna lub przebyta tętnicza choroba zakrzepowo-zatorowa (np. zawał mięśnia sercowego) lub stany zwiastujące (np. dusznica bolesna)
• Choroba naczyń mózgowych – obecny lub przebyty udar lub stany zwiastujące (np. przemijający atak niedokrwienny (Przejściowy atak niedokrwienny, TIA))
• Znana dziedziczna lub nabyta predyspozycja do tętniczej choroby zakrzepowo-zatorowej, taka jak hiperhomocysteinemia i przeciwciała antyfosfolipidowe (przeciwciała antykardiolipinowe, antykoagulant toczniowy)
• Historia migreny z ogniskowymi objawami neurologicznymi
• Wysokie ryzyko tętniczej choroby zakrzepowo-zatorowej z powodu obecności wielu czynników ryzyka (patrz punkt 4.4) lub obecności poważnego czynnika ryzyka, takiego jak:
• cukrzyca z objawami naczyniowymi
• ciężkie nadciśnienie
• ciężka dyslipoproteinemia.
• Zapalenie trzustki lub ta choroba w wywiadzie, jeśli jest związana z ciężką hipertriglicerydemią.
• Przebyta lub obecna ciężka choroba wątroby do czasu powrotu wartości czynności wątroby do normy.
• Guzy wątroby (łagodne lub złośliwe), obecne lub przeszłe.
• Rozpoznanie lub podejrzenie złośliwych chorób narządów płciowych lub piersi, jeśli są zależne od hormonów.
• Krwawienie z pochwy o nieznanym charakterze.
• Nadwrażliwość na substancje czynne lub na którąkolwiek substancję pomocniczą wymienioną w punkcie 6.1 NuvaRing.
04.4 Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania
OSTRZEŻENIA
W przypadku wystąpienia któregokolwiek z wymienionych poniżej warunków lub czynników ryzyka, należy omówić z kobietą zastosowanie NuvaRing.
W przypadku pogorszenia się lub pierwszego pojawienia się któregokolwiek z tych czynników ryzyka lub stanów, kobieta powinna skontaktować się ze swoim lekarzem w celu ustalenia, czy należy przerwać stosowanie NuvaRing.
1. Zaburzenia krążenia
Ryzyko żylnej choroby zakrzepowo-zatorowej (ŻChZZ)
Stosowanie jakichkolwiek złożonych hormonalnych środków antykoncepcyjnych (COC) powoduje zwiększone ryzyko żylnej choroby zakrzepowo-zatorowej (ŻChZZ) w porównaniu z niestosowaniem. Produkty zawierające lewonorgestrel, norgestymat lub noretysteron są związane z niższym ryzykiem VTE. Ryzyko związane z innymi produktami. taki jak NuvaRing może być dwojaki.Decyzja o zastosowaniu produktu innego niż ten, który wiąże się z niższym ryzykiem VTE, powinna być podejmowana wyłącznie po rozmowie z kobietą, aby upewnić się, że rozumie ona ryzyko VTE związane z NuvaRing, sposób, w jaki pacjent obecne czynniki ryzyka wpływają na to ryzyko oraz fakt, że ryzyko rozwoju ŻChZZ jest największe w pierwszym roku stosowania.Istnieją również dowody na to, że ryzyko wzrasta, gdy przyjmowanie COC zostanie wznowione po przerwie 4 lub więcej tygodni.
Około 2 na 10 000 kobiet, które nie stosują CHC i nie są w ciąży, rozwinie ŻChZZ w okresie jednego roku. Jednak u jednej kobiety ryzyko może być znacznie wyższe, w zależności od jej podstawowych czynników ryzyka (patrz poniżej).
Szacuje się, że na 10 000 kobiet stosujących niskodawkowe CHC zawierające lewonorgestrel około 61 rozwinie żylną chorobę zakrzepowo-zatorową w ciągu roku. Uzyskano niespójne wyniki dotyczące ryzyka ŻChZZ związanego z NuvaRing w porównaniu z złożonymi doustnymi środkami antykoncepcyjnymi zawierającymi lewonorgestrel (oszacowane ryzyko względne wahało się od braku wzrostu, RR = 0,96 do prawie 2-krotnego wzrostu, RR = 1,90). Wartości te odpowiadają około 6-12 VTE rocznie u 10 000 kobiet stosujących NuvaRing.
W obu przypadkach liczba ŻChZZ rocznie jest niższa niż przewidywana u kobiet w ciąży lub po porodzie.
ŻChZZ może być śmiertelna w 1-2% przypadków.
Bardzo rzadko u osób stosujących złożone hormonalne środki antykoncepcyjne zgłaszano zakrzepicę innych naczyń krwionośnych, np. żył i tętnic wątrobowych, krezkowych, nerkowych lub siatkówki.
Czynniki ryzyka ŻChZZ
Ryzyko żylnych powikłań zakrzepowo-zatorowych u osób stosujących złożone hormonalne środki antykoncepcyjne może znacznie wzrosnąć, jeśli występują dodatkowe czynniki ryzyka, zwłaszcza jeśli występuje więcej niż jeden czynnik ryzyka (patrz tabela).
NuvaRing jest przeciwwskazany, jeśli u kobiety występuje wiele czynników ryzyka, które zwiększają jej ryzyko zakrzepicy żylnej (patrz punkt 4.3). Jeśli u kobiety występuje więcej niż jeden czynnik ryzyka, możliwe jest, że zwiększone ryzyko jest większe niż suma poszczególnych czynników; w takim przypadku należy wziąć pod uwagę całkowite ryzyko ŻChZZ. , nie należy przepisywać COC (patrz punkt 4.3).
Tabela: Czynniki ryzyka ŻChZZ
Nie ma zgody co do możliwej roli żylaków i zakrzepowego zapalenia żył powierzchownych w powstawaniu i progresji zakrzepicy żylnej.
Należy wziąć pod uwagę zwiększone ryzyko wystąpienia choroby zakrzepowo-zatorowej w ciąży, szczególnie w 6-tygodniowym okresie połogu (informacje dotyczące „Ciąża i laktacja”, patrz punkt 4.6).
Objawy ŻChZZ (zakrzepica żył głębokich i zatorowość płucna)
Jeśli wystąpią tego typu objawy, kobiety powinny natychmiast zwrócić się o pomoc lekarską i poinformować je, że przyjmują CHC.
Objawy zakrzepicy żył głębokich (DVT) mogą obejmować:
• jednostronny obrzęk nogi i/lub stopy lub wzdłuż żyły w nodze;
• ból lub tkliwość w nodze, która może być odczuwana tylko podczas stania lub chodzenia;
• zwiększone czucie ciepła w chorej nodze; czerwona lub przebarwiona skóra na nodze.
Objawy zatorowości płucnej (PE) mogą obejmować:
• nagłe i niewyjaśnione wystąpienie duszności i szybkiego oddechu;
• nagły kaszel, który może być związany z krwiopluciem;
• ostry ból w klatce piersiowej;
• silne uczucie pustki w głowie lub zawroty głowy;
• szybkie lub nieregularne bicie serca.
Niektóre z tych objawów (takie jak „duszność” i „kaszel”) są niespecyficzne i mogą być błędnie interpretowane jako częstsze lub mniej poważne zdarzenia (np. infekcje dróg oddechowych).
Inne objawy niedrożności naczyń mogą obejmować: nagły ból, obrzęk lub bladoniebieskie przebarwienie jednej „kończyny”.
Jeśli okluzja ma miejsce w oku, objawy mogą obejmować bezbolesne niewyraźne widzenie lub utratę wzroku. Czasami utrata wzroku następuje niemal natychmiast.
Ryzyko tętniczej choroby zakrzepowo-zatorowej (ATE)
Badania epidemiologiczne wiążą stosowanie złożonych hormonalnych środków antykoncepcyjnych ze zwiększonym ryzykiem tętniczej choroby zakrzepowo-zatorowej (zawału mięśnia sercowego) lub incydentów naczyniowo-mózgowych (np. przemijający napad niedokrwienny, udar).Tętnicze zdarzenia zakrzepowo-zatorowe mogą być śmiertelne.
Czynniki ryzyka ATE
Ryzyko wystąpienia tętniczych powikłań zakrzepowo-zatorowych lub incydentów naczyniowo-mózgowych u osób stosujących złożone hormonalne środki antykoncepcyjne wzrasta w obecności czynników ryzyka (patrz tabela). NuvaRing jest przeciwwskazany, jeśli kobieta ma jeden poważny czynnik lub wiele czynników ryzyka ATE, które zwiększają jej ryzyko zakrzepicy tętniczej (patrz punkt 4.3). Jeśli u kobiety występuje więcej niż jeden czynnik ryzyka, możliwe jest, że wzrost ryzyka jest większy niż suma poszczególnych czynników; w takim przypadku należy wziąć pod uwagę całkowite ryzyko. nie należy przepisywać CHC (patrz punkt 4.3).
Tabela: Czynniki ryzyka ATE
Objawy ATE
Jeśli wystąpią tego typu objawy, kobiety muszą: natychmiast skontaktuj się z pracownikiem służby zdrowia i poinformuj go, że przyjmuje CHC.
Objawy udaru naczyniowo-mózgowego mogą obejmować:
• nagłe drętwienie lub osłabienie twarzy, ręki lub nogi, zwłaszcza po jednej stronie ciała;
• nagłe trudności w chodzeniu, zawroty głowy, utrata równowagi lub koordynacji;
• nagłe splątanie, trudności w mówieniu lub rozumieniu;
• nagłe trudności z widzeniem w jednym lub obu oczach;
• nagła, ciężka lub przedłużająca się migrena bez znanej przyczyny;
• utrata przytomności lub omdlenia z drgawkami lub bez drgawek.
Tymczasowe objawy sugerują, że jest to przejściowy atak niedokrwienny (TIA).
Objawy zawału mięśnia sercowego (MI) mogą obejmować:
• ból, dyskomfort, ucisk, ciężkość, uczucie ściskania lub pełności w klatce piersiowej, ramieniu lub poniżej mostka;
• dyskomfort promieniujący do pleców, szczęki, gardła, ramion, żołądka;
• uczucie pełności, niestrawności lub zadławienia;
• pocenie się, nudności, wymioty lub zawroty głowy;
• skrajne osłabienie, niepokój lub duszność;
• szybkie lub nieregularne bicie serca.
W przypadku podejrzenia lub potwierdzenia VTE lub ATE CHC powinien zostać zawieszony. Należy zastosować odpowiednią antykoncepcję ze względu na teratogenność leczenia przeciwzakrzepowego (kumaryny).
2. Guzy
• Badania epidemiologiczne wskazują, że długotrwałe stosowanie doustnych środków antykoncepcyjnych jest czynnikiem ryzyka rozwoju raka szyjki macicy u kobiet zakażonych wirusem brodawczaka ludzkiego (HPV).Nie ma jednak pewności, jak duży wpływ na to odkrycie mają czynniki zakłócające (np. różnice). liczby partnerów seksualnych lub stosowania barier antykoncepcyjnych.) Brak danych epidemiologicznych dotyczących ryzyka raka szyjki macicy u kobiet stosujących NuvaRing (patrz „Badania / wizyty lekarskie”).
• Metaanaliza 54 badań epidemiologicznych wykazała, że kobiety stosujące złożone hormonalne środki antykoncepcyjne mają nieznacznie zwiększone ryzyko względne (RR = 1,24) rozpoznania raka piersi. Nadmierne ryzyko stopniowo zanika w ciągu 10 lat od przerwania leczenia. Ponieważ rak piersi występuje rzadko u kobiet poniżej 40 roku życia, liczba dodatkowych przypadków raka piersi zdiagnozowanych u kobiet przyjmujących lub niedawno przyjmujących złożone hormonalne środki antykoncepcyjne jest niska w porównaniu z ogólnym ryzykiem raka piersi. Rak piersi zdiagnozowany u kobiet stosujących doustne środki antykoncepcyjne jest zwykle mniej zaawansowany klinicznie niż rak zdiagnozowany u kobiet, które nigdy nie stosowały doustnego środka antykoncepcyjnego. Obserwacje dotyczące zwiększonego ryzyka mogą wynikać z wczesnego rozpoznania raka piersi u kobiet stosujących złożone doustne środki antykoncepcyjne, biologicznego wpływu tych samych lub kombinacji obu czynników.
• U kobiet przyjmujących złożone hormonalne środki antykoncepcyjne rzadko zgłaszano łagodne guzy wątroby, a jeszcze rzadziej złośliwe guzy wątroby. W pojedynczych przypadkach nowotwory te powodowały zagrażające życiu krwotoki w jamie brzusznej. Dlatego też, jeśli kobieta stosująca NuvaRing odczuwa silny ból w nadbrzuszu, powiększenie wątroby lub objawy wskazujące na krwotok śródbrzuszny, w diagnostyce różnicowej należy wziąć pod uwagę możliwość raka wątroby.
3. Inne warunki
• Kobiety z hipertriglicerydemią lub z tą chorobą w wywiadzie rodzinnym mogą być narażone na zwiększone ryzyko zapalenia trzustki podczas przyjmowania hormonalnych środków antykoncepcyjnych.
• Chociaż u wielu kobiet stosujących hormonalne środki antykoncepcyjne odnotowano niewielkie wzrosty ciśnienia krwi, klinicznie istotne wzrosty są rzadkimi zdarzeniami. Nie ustalono wyraźnej korelacji pomiędzy stosowaniem hormonalnych środków antykoncepcyjnych a nadciśnieniem klinicznym, jednak jeśli podczas stosowania NuvaRing wystąpi przedłużone klinicznie istotne nadciśnienie, lekarz powinien, jako środek ostrożności, przerwać stosowanie pierścienia i zastosować leczenie. NuvaRing można wznowić, jeśli po leczeniu przeciwnadciśnieniowym osiągnięto prawidłowe wartości ciśnienia krwi.
• Początek lub pogorszenie wymienionych poniżej stanów odnotowano zarówno w czasie ciąży, jak i podczas przyjmowania hormonalnych środków antykoncepcyjnych, ale nie ma jednoznacznych dowodów na związek między tymi stanami a hormonalnymi środkami antykoncepcyjnymi: żółtaczka i/lub swędzenie spowodowane cholestazą, tworzeniem się kamieni żółciowych, porfiria, toczeń rumieniowaty układowy, zespół hemolityczno-mocznicowy, pląsawica Sydenhama, opryszczka ciężarnych, utrata słuchu spowodowana otosklerozą, obrzęk naczynioruchowy (dziedziczny).
• Ostre lub przewlekłe zaburzenia czynności wątroby mogą wymagać przerwania stosowania NuvaRing do czasu powrotu parametrów czynności wątroby do normy Powrót żółtaczki cholestatycznej i (lub) świądu cholestatycznego, które wystąpiły w czasie ciąży lub podczas wcześniejszego leczenia steroidami płciowymi, wymaga przerwania korzystania z pierścienia.
• Chociaż estrogeny i progestageny mogą wpływać na obwodową oporność na insulinę i tolerancję glukozy, nie ma dowodów na potrzebę dostosowania schematu leczenia u chorych na cukrzycę stosujących hormonalne środki antykoncepcyjne.
• W związku ze stosowaniem hormonalnych środków antykoncepcyjnych zgłaszano pogorszenie choroby Leśniowskiego-Crohna i wrzodziejące zapalenie jelita grubego.
• Od czasu do czasu może pojawić się ostuda, zwłaszcza u kobiet z historią ostudy ciężką. Kobiety ze skłonnością do ostudy powinny unikać ekspozycji na słońce lub promieniowanie ultrafioletowe podczas stosowania NuvaRing.
• Jeśli kobieta cierpi na którykolwiek z poniższych stanów, może nie być w stanie prawidłowo założyć NuvaRing lub może zgubić pierścień: wypadnięcie szyjki macicy, pęcherz moczowy i/lub odbytnica, ciężkie lub przewlekłe zaparcia.
Bardzo rzadko donoszono o nieumyślnym włożeniu NuvaRing do cewki moczowej, co może doprowadzić do pęcherza moczowego, dlatego w diagnostyce różnicowej należy rozważyć nieprawidłowe umieszczenie leku w przypadku wystąpienia objawów zapalenia pęcherza moczowego.
• Sporadycznie podczas stosowania NuvaRing mogą wystąpić przypadki zapalenia pochwy.Nie ma dowodów na to, że leczenie zapalenia pochwy będzie miało wpływ na skuteczność działania NuvaRing, ani że stosowanie NuvaRing wpłynie na leczenie zapalenia pochwy (patrz punkt 4.5).
• Bardzo rzadko zgłaszano, że pierścień przywarł do tkanki pochwy, co wymagało jego usunięcia przez przeszkolonego pracownika służby zdrowia.
BADANIA / WIZYTY LEKARSKIE
Przed rozpoczęciem lub wznowieniem stosowania NuvaRing należy zebrać pełny wywiad chorobowy (w tym wywiad rodzinny) i wykluczyć ciążę, zmierzyć ciśnienie krwi i przeprowadzić badanie kliniczne, kierując się przeciwwskazaniami (patrz punkt 4.3). ostrzeżenia (patrz punkt 4.4) Ważne jest zwrócenie uwagi kobiety na informacje dotyczące zakrzepicy żylnej lub tętniczej, w tym ryzyko związane ze stosowaniem leku NuvaRing w porównaniu z innymi złożonymi hormonalnymi środkami antykoncepcyjnymi, objawy żylnej choroby zakrzepowo-zatorowej i zakrzepicy tętnicy zakrzepowo-zatorowej, znane czynniki ryzyka oraz postępowanie w przypadku podejrzenia zakrzepicy.
Należy również poinformować kobietę o konieczności uważnego przeczytania ulotki dołączonej do opakowania i zastosowania się do jej zaleceń. Częstotliwość i rodzaj badań powinna opierać się na ustalonych wytycznych i powinna być dostosowana do indywidualnej kobiety.
Należy poinformować kobiety, że hormonalne środki antykoncepcyjne nie chronią przed zakażeniem wirusem HIV (AIDS) i innymi chorobami przenoszonymi drogą płciową.
REDUKCJA EFEKTYWNOŚCI
Skuteczność NuvaRing może być zmniejszona w przypadku nieprzestrzegania dostarczonych informacji (punkt 4.2) lub w przypadku jednoczesnego przyjmowania innych produktów leczniczych (punkt 4.5).
ZMNIEJSZENIE KONTROLI CYKLU
Podczas stosowania NuvaRing może wystąpić nieregularne krwawienie (plamienie lub krwawienie śródcykliczne. Jeśli nieregularne krwawienie występuje po wcześniej regularnych cyklach, podczas gdy NuvaRing jest stosowany w zalecanym dawkowaniu, należy rozważyć przyczynę niehormonalną i, aby wykluczyć nowotwory złośliwe lub ciążę, odpowiednie należy wdrożyć środki diagnostyczne, które mogą obejmować łyżeczkowanie.
U niektórych kobiet krwawienie z odstawienia może nie wystąpić w okresie bez pierścienia.Jeśli NuvaRing był stosowany zgodnie z instrukcjami opisanymi w punkcie 4.2, jest mało prawdopodobne, że jest w ciąży. Przed dalszym stosowaniem NuvaRing należy wykluczyć ciążę.
EKSPOZYCJA „MAN ALL” ETINILESTRADIOLO I WSZYSTKIE „ETONOGESTREL
Nie badano stopnia i możliwej roli farmakologicznej ekspozycji męskiego partnera seksualnego na etynyloestradiol i etonogestrel poprzez wchłanianie z penisa.
ZŁAMANIE PIERŚCIENIA
Zgłaszano, że pierścień NuvaRing otwierał się podczas używania w bardzo rzadkich przypadkach (patrz punkt 4.5). Należy doradzić kobiecie jak najszybsze usunięcie złamanego pierścienia i ponowne założenie nowego oraz dodatkowo stosowanie przez kolejne 7 dni metody mechanicznej, np. prezerwatywy.Należy rozważyć możliwość zajścia w ciążę, a kobieta powinna skontaktować się z lekarzem.
WYDALENIE
Istnieją doniesienia, że NuvaRing może zostać usunięty, na przykład jeśli pierścień nie został prawidłowo założony, podczas usuwania tamponu, podczas stosunku lub w przypadku ciężkich lub przewlekłych zaparć.Przedłużone wydalenie może prowadzić do niepowodzenia antykoncepcji i / lub przełomowe krwawienie.
Dlatego, aby zapewnić skuteczność, należy zalecić kobiecie regularne sprawdzanie obecności NuvaRing.
Jeśli NuvaRing zostanie przypadkowo wyrzucony i pozostawiony z pochwy na mniej niż 3 godziny, skuteczność antykoncepcyjna nie jest zmniejszona.Kobieta powinna umyć pierścień zimną lub ciepłą (nie gorącą) wodą i założyć go ponownie tak szybko, jak to możliwe, ale nie później niż o 3 godziny.
Jeśli pierścień NuvaRing znajdował się poza pochwą lub istnieje podejrzenie, że znajdował się poza pochwą przez ponad 3 godziny, skuteczność antykoncepcyjna może być zmniejszona. tymczasowo wydalony z pochwy ”.
04.5 Interakcje z innymi produktami leczniczymi i inne formy interakcji
INTERAKCJE Z INNYMI LEKAMI
Interakcje między hormonalnymi środkami antykoncepcyjnymi a innymi produktami leczniczymi mogą prowadzić do krwawienia międzymiesiączkowego i (lub) niepowodzenia antykoncepcji.W piśmiennictwie opisano następujące interakcje.
Metabolizm wątrobowy: Mogą wystąpić interakcje z produktami leczniczymi, które indukują enzymy mikrosomalne, powodując zwiększony klirens hormonów płciowych (np. fenytoina, fenobarbital, prymidon, karbamazepina, ryfampicyna i prawdopodobnie również okskarbazepina, topiramat, felbamat, rytonawir, gryzeofulwina i produkty zawierające stieofulwinę brzeczka).
Kobiety leczone którymkolwiek z tych leków powinny tymczasowo stosować oprócz NuvaRing metodę mechaniczną lub wybrać inną metodę antykoncepcji. W przypadku produktów leczniczych indukujących wątrobowe enzymy mikrosomalne, metodę barierową należy stosować przez cały okres jednoczesnego podawania leku i przez 28 dni po ich odstawieniu.
Jeśli jednoczesne podawanie leku trwa dłużej niż 3 tygodnie cyklu pierścienia, następny pierścień należy założyć natychmiast, bez zachowania zwykłego odstępu czasu bez pierścienia.
Odnotowano również utratę skuteczności antykoncepcji w przypadku antybiotyków, takich jak penicyliny i tetracykliny.Mechanizm tego działania nie został dobrze poznany. W badaniu farmakokinetyki interakcji doustne podawanie amoksycyliny (875 mg, dwa razy na dobę) lub doksycykliny (200 mg w dniu 1., a następnie 100 mg na dobę) przez 10 dni podczas stosowania NuvaRing nie miało istotnego wpływu na farmakokinetykę etonogestrelu i EE. Kobiety leczone antybiotykami (z wyjątkiem amoksycyliny i doksycykliny) powinny stosować metodę mechaniczną przez okres do 7 dni po odstawieniu.Jeżeli jednoczesne podawanie leku trwa dłużej niż 3 tygodnie cyklu pierścienia, należy natychmiast założyć następny pierścień, nie obserwując zwykłego pierścienia -wolny interwał.
Na podstawie danych farmakokinetycznych przewiduje się, że środki przeciwgrzybicze dopochwowe i środki plemnikobójcze nie będą miały wpływu na skuteczność antykoncepcyjną i bezpieczeństwo NuvaRing.Podczas równoczesnego stosowania pessarów przeciwgrzybiczych ryzyko pęknięcia pierścienia może być nieco większe (patrz punkt 4.4 „Pęknięcie pierścienia”). .
Hormonalne środki antykoncepcyjne mogą wpływać na metabolizm innych leków. W konsekwencji stężenie w osoczu i tkankach może albo wzrosnąć (np. cyklosporyna), albo zmniejszyć (np. lamotrygina).
Należy zapoznać się z informacjami dotyczącymi jednocześnie stosowanych leków, aby zidentyfikować potencjalne interakcje.
EGZAMINY LABORATORYJNE
Stosowanie steroidów antykoncepcyjnych może wpływać na wyniki niektórych badań laboratoryjnych, w tym parametrów biochemicznych czynności wątroby, tarczycy, nadnerczy i nerek, stężenia białek transportowych w osoczu (np. globuliny wiążącej kortykosteroidy i globuliny wiążącej hormony płciowe), lipidów/ frakcje lipoproteinowe, parametry metabolizmu węglowodanów, koagulacji i fibrynolizy. Odchylenia mieszczą się na ogół w granicach normalnych wartości laboratoryjnych.
INTERAKCJE Z PODKŁADKAMI CHŁONNYMI
Dane farmakokinetyczne pokazują, że stosowanie tamponów nie ma wpływu na ogólnoustrojową absorpcję hormonów uwalnianych przez NuvaRing. W rzadkich przypadkach NuvaRing może zostać wyrzucony podczas wyjmowania tamponu (patrz wskazówki w części „Co zrobić, jeśli pierścień zostanie tymczasowo wyrzucony z pochwy”).
04.6 Ciąża i laktacja
Płodność
NuvaRing jest wskazany w zapobieganiu ciąży. Jeśli kobieta chce przestać stosować NuvaRing, ponieważ chce zajść w ciążę, zaleca się odczekać przed próbą zajścia w ciążę do momentu, w którym wystąpi naturalna miesiączka, ponieważ pomoże to jej obliczyć, kiedy dziecko ma urodzić.
Ciąża
NuvaRing nie jest wskazany w okresie ciąży. Jeśli zajdziesz w ciążę z NuvaRing na miejscu, pierścień musi zostać usunięty. Obszerne badania epidemiologiczne nie wykazały zwiększonego ryzyka wad wrodzonych u dzieci urodzonych przez kobiety, które stosowały złożone doustne środki antykoncepcyjne przed ciążą, ani nie stwierdzono działania teratogennego w przypadku nieumyślnego zastosowania COC we wczesnej ciąży .
Badanie kliniczne przeprowadzone na niewielkiej liczbie kobiet wykazało, że pomimo podania dopochwowego, wewnątrzmaciczne stężenia steroidów antykoncepcyjnych z NuvaRing są podobne do stężeń obserwowanych u kobiet stosujących COC (patrz punkt 5.2).
Nie zgłoszono żadnych doświadczeń klinicznych dotyczących wyników ciąży narażonych na NuvaRing.
Przy ponownym rozpoczynaniu leczenia produktem NuvaRing należy wziąć pod uwagę zwiększone ryzyko wystąpienia choroby zakrzepowo-zatorowej w okresie poporodowym (patrz punkty 4.2 i 4.4).
Czas karmienia
Estrogen może mieć wpływ na karmienie piersią, ponieważ może zmniejszyć ilość i zmienić skład mleka kobiecego.W związku z tym należy odradzać stosowanie NuvaRing do czasu zakończenia przez matkę odstawienia od piersi. Niewielkie ilości steroidów antykoncepcyjnych i/lub ich metabolitów mogą przenikać do mleka, ale nie ma dowodów na to, że wpływa to niekorzystnie na zdrowie dziecka.
04.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
W oparciu o profil farmakodynamiczny, NuvaRing nie ma wpływu lub ma nieistotny wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn.
04.8 Działania niepożądane
Najczęściej zgłaszanymi działaniami niepożądanymi w badaniach klinicznych z NuvaRing były bóle głowy, infekcje pochwy i upławy, każde zgłaszane przez 5-6% kobiet.
Opis niektórych działań niepożądanych
U osób stosujących złożone hormonalne środki antykoncepcyjne obserwowano zwiększone ryzyko wystąpienia tętniczych i żylnych zdarzeń zakrzepowych i zakrzepowo-zatorowych, w tym zawału mięśnia sercowego, udaru mózgu, przemijających napadów niedokrwiennych, zakrzepicy żylnej i zatorowości płucnej. Ryzyko to omówiono bardziej szczegółowo w punkcie 4.4.
U osób stosujących złożone hormonalne środki antykoncepcyjne zgłaszano również inne działania niepożądane: działania te omówiono bardziej szczegółowo w punkcie 4.4.
W poniższej tabeli wymieniono działania niepożądane leku zgłaszane w badaniach klinicznych, badaniach obserwacyjnych lub podczas stosowania produktu NuvaRing po wprowadzeniu do obrotu.Najbardziej odpowiedni termin MedDRA jest wymieniony w celu opisania określonego zdarzenia niepożądanego.
Wszystkie działania niepożądane wymieniono według klasyfikacji układów i narządów oraz częstości; często (≥ 1/100,
1) Lista zdarzeń niepożądanych na podstawie zgłoszeń spontanicznych.
W związku ze stosowaniem COC zgłaszano występowanie guzów hormonozależnych (np. guzów wątroby, raka piersi).W celu uzyskania dalszych informacji patrz punkt 4.4.
W rzadkich przypadkach partnerzy kobiet stosujących NuvaRing zgłaszali chorobę prącia podczas nadzoru po wprowadzeniu do obrotu.
U kobiet stosujących złożone hormonalne środki antykoncepcyjne szereg działań niepożądanych opisano bardziej szczegółowo w punkcie 4.4. Efekty te obejmują:
- żylne zaburzenia zakrzepowo-zatorowe;
- tętnicze zaburzenia zakrzepowo-zatorowe;
- nadciśnienie;
- nowotwory zależne od hormonów (np. nowotwory wątroby, rak piersi);
- ostuda
Zgłaszanie podejrzewanych działań niepożądanych
Zgłaszanie podejrzewanych działań niepożądanych występujących po dopuszczeniu produktu leczniczego do obrotu jest ważne, ponieważ umożliwia ciągłe monitorowanie stosunku korzyści do ryzyka produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem krajowego systemu zgłaszania. www.agenziafarmaco.gov.it/it/responsabili ”.
04.9 Przedawkowanie
Nie zgłoszono żadnych poważnych działań niepożądanych przedawkowania hormonalnych środków antykoncepcyjnych. W takiej sytuacji mogą wystąpić takie objawy, jak nudności, wymioty, a u dziewcząt łagodne krwawienie z pochwy. Nie ma odtrutek i każde leczenie musi być objawowe.
05.0 WŁAŚCIWOŚCI FARMAKOLOGICZNE
05.1 Właściwości farmakodynamiczne
Grupa farmakoterapeutyczna: inne produkty ginekologiczne, dopochwowe środki antykoncepcyjne, pierścień dopochwowy z progestagenem i estrogenem, kod ATC: G02BB01.
Mechanizm akcji
NuvaRing zawiera etonogestrel i etynyloestradiol. Etonogestrel jest progestyną pochodną 19-nortestosteronu i wiąże się z wysokim powinowactwem z receptorami progesteronu w narządach docelowych.Etynyloestradiol jest estrogenem szeroko stosowanym w środkach antykoncepcyjnych. Działanie antykoncepcyjne NuvaRing opiera się na różnych mechanizmach, z których najważniejszym jest hamowanie owulacji.
Skuteczność kliniczna i bezpieczeństwo
Badania kliniczne przeprowadzono na całym świecie (USA, Europa i Brazylia) na kobietach w wieku od 18 do 40. Skuteczność antykoncepcji okazała się co najmniej porównywalna do tej znanej dla złożonych doustnych środków antykoncepcyjnych. Poniższa tabela przedstawia wskaźniki Pearl (liczba ciąż na lata użytkowania przez 100 kobiet) znalezione w badaniach klinicznych z NuvaRing.
Stosowanie dużych dawek COC (0,05 mg etynyloestradiolu) zmniejsza ryzyko raka endometrium i jajnika.Należy ustalić, czy dotyczy to również niższych dawek środków antykoncepcyjnych, takich jak NuvaRing.
PROFIL KRWI
Duże badanie porównawcze z doustnym środkiem antykoncepcyjnym zawierającym lewonorgestrel/etynyloestradiol 150/30?G (n = 512 w porównaniu z n = 518), w którym oceniano charakterystykę krwawienia z pochwy w ciągu 13 cykli, wykazało niską częstość występowania plamienia lub krwawienia międzymiesiączkowego w grupie NuvaRing ( 2,0-6,4%). Ponadto krwawienie z pochwy ograniczało się wyłącznie do okresu bez pierścienia u większości pacjentek (58,8-72,8%).
WPŁYW NA GĘSTOŚĆ KOŚCI MINERALNE
Wpływ NuvaRing (n = 76) na gęstość mineralną kości badano w porównaniu z niehormonalną wkładką domaciczną (IUD) (n = 31) przez okres dwóch lat. Nie zaobserwowano niekorzystnego wpływu na masę kostną.
Populacja pediatryczna
Nie badano bezpieczeństwa i skuteczności produktu NuvaRing u młodzieży w wieku poniżej 18 lat.
05.2 Właściwości farmakokinetyczne
Etonogestrel
Wchłanianie
Etonogestrel uwalniany przez NuvaRing jest szybko wchłaniany przez błonę śluzową pochwy.Maksymalne stężenie etonogestrelu w surowicy, około 1700 pg/ml, osiągane jest po około tygodniu od założenia. Stężenia w surowicy wykazują niewielkie wahania i powoli spadają do około 1600 pg/ml po tygodniu, 1500 pg/ml po 2 tygodniach i 1400 pg/ml po 3 tygodniach stosowania. Całkowita biodostępność wynosi około 100% i jest większa niż po podaniu doustnym. U niewielkiej liczby kobiet stosujących NuvaRing lub doustny środek antykoncepcyjny zawierający 0,150 mg dezogestrelu i 0,020 mg etynyloestradiolu zmierzono stężenie etonogestrelu w szyjce macicy i w macicy. Zaobserwowane poziomy były porównywalne.
Dystrybucja
Etonogestrel wiąże się z albuminą surowicy i globuliną wiążącą hormony płciowe (SHBG). Pozorna objętość dystrybucji etonogestrelu wynosi 2,3 l/kg.
Biotransformacja
Etonogestrel jest metabolizowany przez znane szlaki metabolizmu steroidów.Pozorny klirens w surowicy wynosi około 3,5 l / h. Nie stwierdzono bezpośredniej interakcji z jednocześnie podawanym etynyloestradiolem.
Eliminacja
Stężenie etonogestrelu w surowicy zmniejsza się dwufazowo. Faza eliminacji końcowej charakteryzuje się okresem półtrwania wynoszącym około 29 godzin. Etonogestrel i jego metabolity są wydalane w stosunku mocz/żółć wynoszącym około 1,7:1. Okres półtrwania wydalanego metabolitu wynosi około 6 dni.
Etynyloestradiol
Wchłanianie
Etynyloestradiol uwalniany przez NuvaRing jest szybko wchłaniany przez błonę śluzową pochwy.Maksymalne stężenia w surowicy, około 35 pg/ml, osiągane są 3 dni po założeniu i zmniejszają się do 19 pg/ml po 1 tygodniu, 18 pg/ml po 2 tygodniach i 18 pg / ml po 3 tygodniach stosowania. Miesięczna ogólnoustrojowa ekspozycja na etynyloestradiol (AUC0-∞) z NuvaRing wynosi 10,9 ng • h / ml. Całkowita biodostępność wynosi około 56%, porównywalna z przyjmowaniem doustnym etynyloestradiolu. U niewielkiej liczby kobiet stosujących NuvaRing lub doustne środki antykoncepcyjne zawierające 0,150 mg dezogestrelu i 0,020 mg etynyloestradiolu zmierzono stężenie etynyloestradiolu w szyjce macicy i w macicy. Zaobserwowane poziomy były porównywalne.
Dystrybucja
Etynyloestradiol jest w dużej mierze, ale nie konkretnie, związany z albuminą surowicy. Określono pozorną objętość dystrybucji około 15 l/kg.
Biotransformacja
Głównym szlakiem metabolicznym etynyloestradiolu jest hydroksylacja aromatyczna, ale powstaje również wiele różnych hydroksylowanych i metylowanych metabolitów, obecnych jako wolne metabolity oraz jako koniugaty siarczanowe i glukuronianowe. Pozorny klirens to około 35 l/h.
Eliminacja
Stężenie etynyloestradiolu w surowicy zmniejsza się dwufazowo.Końcowa faza eliminacji charakteryzuje się dużą indywidualną zmiennością okresu półtrwania, czego średni okres półtrwania wynosi około 34 h. Niezmieniony etynyloestradiol nie jest wydalany; metabolity etynyloestradiolu są wydalane w stosunku mocz/żółć 1,3:1. Okres półtrwania wydalania metabolitów wynosi około 1,5 dnia.
Populacje specjalne
Populacja pediatryczna
Nie badano farmakokinetyki produktu NuvaRing u zdrowych dziewcząt w wieku poniżej 18 lat po pierwszej miesiączce.
Wpływ uszkodzenia nerek
Nie przeprowadzono badań oceniających wpływ choroby nerek na farmakokinetykę NuvaRing.
Wpływ zaburzeń czynności wątroby
Nie przeprowadzono badań oceniających wpływ chorób wątroby na farmakokinetykę NuvaRing, jednak hormony steroidowe mogą być słabo metabolizowane u kobiet z zaburzeniami czynności wątroby.
Grupy etniczne
Nie przeprowadzono formalnych badań oceniających farmakokinetykę w grupach etnicznych.
05.3 Przedkliniczne dane o bezpieczeństwie
Dane niekliniczne dotyczące etynyloestradiolu i etonogestrelu, wynikające z konwencjonalnych badań farmakologicznych dotyczących bezpieczeństwa, toksyczności po podaniu wielokrotnym, genotoksyczności, potencjalnego działania rakotwórczego i toksycznego wpływu na reprodukcję, oprócz dotychczasowych badań u ludzi, nie ujawniają szczególnych zagrożeń dla ludzi.
06.0 INFORMACJE FARMACEUTYCZNE
06.1 Zaróbki
Kopolimer etylen-octan winylu, 28% octan winylu;
kopolimer etylen-octan winylu, 9% octan winylu;
stearynian magnezu.
06.2 Niekompatybilność
Nieistotne.
06.3 Okres ważności
40 miesięcy.
06.4 Specjalne środki ostrożności przy przechowywaniu
Przed wydaniem:
3 lata przechowywać w lodówce (2°C - 8°C).
W momencie dyspensy:
Farmaceuta zapisuje na opakowaniu datę sprzedaży. Produkt należy włożyć nie później niż 4 miesiące od daty sprzedaży, ale w każdym przypadku przed datą ważności, jeśli przypada ona wcześniej.
Po wydaniu:
4 miesiące przechowywać w temperaturze poniżej 30°C.
Przechowywać w oryginalnym opakowaniu, aby chronić urządzenie przed światłem i wilgocią.
06.5 Rodzaj opakowania bezpośredniego i zawartość opakowania
Saszetka zawierająca pojedynczy NuvaRing. Saszetka wykonana jest z folii aluminiowej, której warstwa wewnętrzna to polietylen o niskiej gęstości, natomiast warstwa zewnętrzna to politereftalan etylenu (PET). Saszetka jest zamykana i wodoodporna i jest pakowana w pudełko tekturowe z nadrukiem wraz z ulotką dla pacjenta. Każde pudełko zawiera 1 lub 3 pierścienie.
Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
06.6 Instrukcje użytkowania i obsługi
Patrz rozdział 4.2. Farmaceuta musi podać na opakowaniu datę sprzedaży. W przypadku opakowania zawierającego 3 pierścienie zaleca się umieszczenie tej daty na zewnętrznym opakowaniu i na saszetkach NuvaRing należy założyć nie później niż 4 miesiące od daty sprzedaży, ale w każdym przypadku przed upływem terminu ważności w przypadku wcześniejszego W celu uniknięcia przypadkowego kontaktu, NuvaRing należy umieścić z powrotem w zamykanej saszetce i wyrzucić wraz ze zwykłymi odpadami domowymi. NuvaRing nie wolno wyrzucać do toalety. Wszelkie niewykorzystane (przeterminowane) pierścienie należy usunąć zgodnie z lokalnymi przepisami.
07.0 PODMIOT POZWOLENIA NA DOPUSZCZENIE DO OBROTU
N.V. Organon
Kloosterstraat 6
5349 AB Obs
Holandia
08.0 NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
1 saszetka zawierająca 1 urządzenie dopochwowe
AIC nr 035584010
3 saszetki, z których każda zawiera 1 urządzenie dopochwowe
AIC nr 035584022
09.0 DATA PIERWSZEGO ZEZWOLENIA LUB PRZEDŁUŻENIA ZEZWOLENIA
28 maja 2002 / 1 marca 2012
10.0 DATA ZMIAN TEKSTU
Lipiec 2014




















fortuna-di-halloween.jpg)