Składniki aktywne: Doksorubicyna
Caelyx 2 mg/ml koncentrat do sporządzania roztworu do infuzji
Wskazania Dlaczego stosuje się Caelyx? Po co to jest?
Caelyx jest środkiem przeciwnowotworowym.
Caelyx stosuje się w leczeniu raka piersi u pacjentek z ryzykiem wystąpienia problemów z sercem. Caelyx jest również stosowany w leczeniu raka jajnika.Stosuje się go do zabijania komórek nowotworowych, zmniejszania wielkości guza, opóźniania wzrostu guza i przedłużania jego przeżycia.
Preparat Caelyx stosuje się również w skojarzeniu z innym lekiem, bortezomibem, w leczeniu szpiczaka mnogiego, nowotworu krwi, u pacjentów, którzy otrzymali co najmniej jedną wcześniejszą terapię.
Caelyx jest również stosowany w leczeniu mięsaka Kaposiego, w tym spłaszczaniu, blednięciu, a nawet zmniejszaniu rozmiaru guza. Inne objawy mięsaka Kaposiego, takie jak obrzęk wokół guza, również mogą ulec poprawie lub zniknąć.
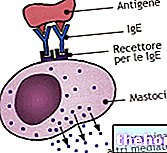
Caelyx zawiera substancję zdolną do interakcji z komórkami w celu selektywnego zabijania komórek nowotworowych. Chlorowodorek doksorubicyny zawarty w Caelyx jest zamknięty w bardzo małych kuleczkach, zwanych pegylowanymi liposomami, które ułatwiają transport leku z krwi do tkanki nowotworowej, unikając jego rozproszenia w zdrowej tkance.
Przeciwwskazania Kiedy nie należy stosować preparatu Caelyx
Nie przyjmować leku Caelyx
- jeśli pacjent ma uczulenie na chlorowodorek doksorubicyny lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6).
Środki ostrożności dotyczące stosowania Informacje ważne przed zastosowaniem leku Caelyx
Powiedz swojemu lekarzowi o następujących warunkach:
- jeśli pacjent jest leczony z powodu problemów z sercem lub wątrobą;
- jeśli pacjent ma cukrzycę, ponieważ lek Caelyx zawiera cukier i może być konieczne odpowiednie dostosowanie leczenia cukrzycy;
- jeśli masz mięsaka Kaposiego i twoja śledziona została usunięta;
- jeśli zauważysz owrzodzenia, przebarwienia lub jakikolwiek dyskomfort w jamie ustnej.
Dzieci i młodzież
Preparatu Caelyx nie należy stosować u dzieci i młodzieży, ponieważ nie wiadomo, w jaki sposób lek na nich wpływa.
Interakcje Jakie leki lub pokarmy mogą zmienić działanie leku Caelyx
Należy poinformować lekarza lub farmaceutę
- jeśli pacjent przyjmuje lub ostatnio przyjmował jakiekolwiek inne leki, w tym te wydawane bez recepty,
- o wszystkich metodach leczenia raka, które obserwuje lub stosował w przeszłości, ponieważ „wymagana jest szczególna uwaga w przypadku leczenia, które zmniejsza liczbę białych krwinek, ponieważ może to prowadzić do„ dalszego zmniejszenia liczby krwinek upławy. Jeśli nie masz pewności co do leczenia, które otrzymałeś lub przebytych chorób, porozmawiaj ze swoim lekarzem
Ostrzeżenia Ważne jest, aby wiedzieć, że:
Ciąża i karmienie piersią
Przed zażyciem jakiegokolwiek leku należy zasięgnąć porady lekarza lub farmaceuty.
Ponieważ substancja czynna leku Caelyx, chlorowodorek doksorubicyny, może powodować zmiany u nienarodzonego dziecka, ważne jest, aby poinformować lekarza o podejrzeniu ciąży. Kobiety powinny unikać zajścia w ciążę, jeśli one lub ich partner są leczeni preparatem Caelyx i przez sześć miesięcy po zaprzestaniu leczenia.
Ponieważ chlorowodorek doksorubicyny może być szkodliwy dla niemowląt, kobiety muszą przerwać karmienie piersią przed rozpoczęciem leczenia preparatem Caelyx.Eksperci zalecają kobietom zakażonym wirusem HIV, aby w żadnych okolicznościach nie karmiły piersią, aby zapobiec przeniesieniu wirusa HIV.
Prowadzenie i używanie maszyn
W przypadku uczucia zmęczenia lub senności po leczeniu lekiem Caelyx nie należy prowadzić pojazdów ani obsługiwać żadnych narzędzi ani maszyn.
Dawka, sposób i czas podawania Jak stosować Caelyx: Dawkowanie
Caelyx to wyjątkowy preparat. Nie wolno go stosować zamiennie z innymi preparatami chlorowodorku doksorubicyny.
Ile podaje się Caelyx
Jeśli pacjentka jest leczona z powodu raka piersi lub jajnika, Caelyx będzie podawany w dawce 50 mg na każdy metr kwadratowy powierzchni ciała (na podstawie wzrostu i masy ciała). Dawkę powtarza się co 4 tygodnie, aż do progresji choroby i zdolności tolerowania leczenia.
Jeśli pacjent jest leczony z powodu szpiczaka mnogiego i otrzymał już co najmniej jedną wcześniejszą terapię, Caelyx zostanie podany dożylnie w dawce 30 mg na metr kwadratowy powierzchni ciała (w zależności od wzrostu i masy ciała). 1 godzina podawana bezpośrednio po wlewie bortezomibem w dniu 4. 3-tygodniowego schematu leczenia bortezomibem Dawka będzie powtarzana do momentu uzyskania zadowalającej odpowiedzi i tolerancji leczenia.
W przypadku leczenia mięsaka Kaposiego lek Caelyx zostanie podany w dawce 20 mg na każdy metr kwadratowy powierzchni ciała (na podstawie wzrostu i masy ciała). Dawkę powtarza się co 2 lub 3 tygodnie przez 2 lub 3 miesiące; następnie zostanie powtórzony, gdy konieczne będzie utrzymanie poprawy jego stanu.
Jak podaje się Caelyx
Caelyx zostanie podany przez lekarza w kroplówce (infuzji) do żyły. W zależności od dawki i wskazania będzie to trwało od 30 minut do ponad godziny (tj. 90 minut).
Przedawkowanie Co zrobić w przypadku przyjęcia zbyt dużej dawki leku Caelyx
Ostre przedawkowanie nasila działania niepożądane, takie jak rany w jamie ustnej lub spadek liczby białych krwinek i płytek krwi.Leczenie będzie polegało na podawaniu antybiotyków, przetaczaniu płytek krwi, stosowaniu czynników stymulujących produkcję białych krwinek oraz objawowym leczeniu owrzodzeń w jamie ustnej.
W przypadku dalszych pytań dotyczących stosowania leku Caelyx należy zwrócić się do lekarza lub farmaceuty.
Skutki uboczne Jakie są skutki uboczne Caelyx
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Podczas infuzji leku Caelyx mogą wystąpić następujące reakcje: zaczerwienienie twarzy, duszność, ból głowy, dreszcze, ból pleców, ucisk w klatce piersiowej i (lub) gardle, ból gardła, wysokie lub niskie ciśnienie krwi, przyspieszona choroba serca, obrzęk twarzy, gorączka, zawroty głowy, nudności, zaburzenia trawienia, świąd, nagłe zaczerwienienie skóry i pocenie się, w bardzo rzadkich przypadkach, wystąpiły drgawki, może również wystąpić kłujący ból lub obrzęk w miejscu wstrzyknięcia, niepokój lub ból podczas przyjmowania dawki leku Caelyx należy natychmiast powiadomić lekarza.
Należy natychmiast skontaktować się z lekarzem, jeśli:
- na dłoniach i stopach pojawia się bolesne zaczerwienienie,
- odczuwać ból na skórze i (lub) pęcherze na ciele lub w jamie ustnej,
- masz problemy z sercem,
- ma rany w ustach,
- gorączka lub inne oznaki infekcji,
- masz „nagłą duszność lub ostry ból w klatce piersiowej, który może się nasilić przy głębokim oddychaniu lub kaszlu”,
- masz obrzęk, ciepło lub wrażliwość tkanek miękkich w nogach, czasami z bólem, który nasila się podczas stania lub chodzenia.
Inne skutki uboczne
W okresie między infuzjami mogą wystąpić następujące efekty:
Bardzo często (może dotyczyć więcej niż 1 na 10 pacjentów):
- zaczerwienienie, obrzęk i rany na dłoniach i podeszwach stóp. Efekty te były często obserwowane i czasami są poważne. W ciężkich przypadkach efekty te mogą zakłócać niektóre codzienne czynności i mogą trwać do 4 tygodni lub dłużej, zanim całkowicie ustąpią. Lekarz może według własnego uznania opóźnić rozpoczęcie i/lub zmniejszyć dawkę kolejnego leczenia (patrz poniżej: Techniki zapobiegania i leczenia zespołu dłoni i stóp);
- ból lub rany w jamie ustnej lub gardle, nudności, wymioty, biegunka, zaparcia, utrata apetytu, utrata masy ciała;
- zmniejszenie liczby białych krwinek, co może zwiększyć ryzyko infekcji. Niedokrwistość (zmniejszenie liczby czerwonych krwinek) może powodować uczucie zmęczenia, a zmniejszenie liczby płytek krwi może zwiększać ryzyko krwawienia.W rzadkich przypadkach mała liczba białych krwinek może prowadzić do poważnych infekcji.Z powodu możliwych zmian w krwinek, wymagane jest regularne monitorowanie krwi W badaniu klinicznym z udziałem pacjentów z AIDS-KS porównującym preparat Caelyx z innym lekiem (bleomycyna/winkrystyna) stwierdzono, że może występować zwiększone ryzyko niektórych zakażeń preparatem Caelyx. Zgodnie z doświadczeniem pacjentów z AIDS-KS, gdy preparat Caelyx porównywano ze standardowym leczeniem zaawansowanego raka jajnika (topotekan), ryzyko infekcji było znacznie niższe w grupie pacjentek leczonych preparatem Caelyx. Ryzyko niskiej liczby krwinek i infekcji było podobnie niskie w badaniach nad rakiem piersi. Niektóre z tych efektów mogą być związane z chorobą, a nie z Caelyxem;
- ogólne uczucie zmęczenia, osłabienia, uczucie mrowienia lub bólu rąk i stóp;
- wypadanie włosów.
Często (mogą dotyczyć do 1 na 10 pacjentów):
- ból brzucha;
- pleśniawki (grzybicze zakażenie jamy ustnej), owrzodzenia nosa, krwawienia z nosa, opryszczka wargowa i zapalenie języka;
- wyniki testów czynności wątroby mogą wzrosnąć lub spaść podczas leczenia preparatem Caelyx;
- senność, zawroty głowy, omdlenia, ból kości, ból w klatce piersiowej, nieprawidłowe napięcie mięśni, ból mięśni, skurcze lub obrzęk kończyn dolnych, ogólny obrzęk, zapalenie siatkówki (błony oka stymulowanej światłem), nasilone łzawienie, niewyraźne widzenie uczucie mrowienia lub bólu rąk i stóp;
- zapalenie mieszków włosowych, łuszczenie się skóry, zapalenie lub wysypka, nieprawidłowa pigmentacja (przebarwienia) skóry i paznokci;
- problemy z sercem, np. nieregularne bicie serca, rozszerzone naczynia krwionośne;
- gorączka, podwyższona temperatura lub inne oznaki infekcji, które mogą być związane z chorobą;
- problemy z oddychaniem, tj. trudności w oddychaniu lub kaszlu, które mogą być związane z infekcjami nabytymi w wyniku choroby;
- niedostateczna ilość wody w organizmie (odwodnienie), znaczna utrata masy ciała i zanik mięśni, niski poziom wapnia, magnezu, potasu lub sodu we krwi, wysoki poziom potasu we krwi;
- zapalenie przełyku, zapalenie błony śluzowej żołądka, trudności w połykaniu, suchość w ustach, wzdęcia, zapalenie dziąseł, zaburzenia smaku;
- zapalenie pochwy;
- ból podczas oddawania moczu;
- jeśli u pacjenta wystąpiły wcześniej reakcje skórne, tj. ból, zaczerwienienie i suchość skóry podczas radioterapii, mogą one nadal występować podczas leczenia lekiem Caelyx;
- Podczas jednoczesnego stosowania leku Caelyx i bortezomibu mogą wystąpić bóle stawów, zmniejszone lub nieprawidłowe czucie podczas stymulacji, zapalenie rogówki, zaczerwienienie oka, zaczerwienienie moszny. wszystko.
Niezbyt często (dotyczy do 1 na 100 pacjentów)
- dezorientacja;
- zapalenie żył i tworzenie się w żyłach zakrzepów krwi, które mogą blokować dopływ krwi do płuc i powodować trudności w oddychaniu, ból w klatce piersiowej i kołatanie serca.
Bardzo rzadko (dotyczy nie więcej niż 1 na 10 000 pacjentów)
- ciężka reakcja skórna, taka jak rozległe złuszczanie się skóry, powstawanie pęcherzy i nadżerka (wrzody) błon śluzowych (zespół Stevensa-Johnsona/toksyczna nekroliza naskórka);
- Rak jamy ustnej może wystąpić, jeśli Caelyx jest przyjmowany przez dłuższy czas (ponad rok).
Zgłaszanie skutków ubocznych
Jeśli wystąpią jakiekolwiek objawy niepożądane, porozmawiaj ze swoim lekarzem lub pielęgniarką, w tym wszelkie możliwe działania niepożądane niewymienione w tej ulotce.Możesz również zgłaszać działania niepożądane bezpośrednio za pośrednictwem krajowego systemu zgłaszania wymienionego w załączniku V. Zgłaszając działania niepożądane, możesz pomóc dostarczyć więcej informacji na temat bezpieczeństwa tego leku.
Techniki zapobiegania i leczenia zespołu dłoni i stóp obejmują:
- w miarę możliwości zanurzaj ręce i/lub stopy w misce z zimną wodą (np. podczas oglądania telewizji, czytania lub słuchania radia);
- trzymaj ręce i stopy odkryte (bez rękawiczek, skarpet itp.)
- pozostań w chłodnych miejscach;
- brać zimne kąpiele w gorących okresach;
- unikaj energicznych ćwiczeń, które mogą spowodować uraz stopy (np. jogging);
- unikać ekspozycji skóry na bardzo gorącą wodę (np. hydromasaż, sauna);
- unikaj ciasnych butów lub butów na wysokim obcasie.
Pirydoksyna (witamina B6):
- witaminę B6 można kupić bez recepty;
- weź 50-150 mg dziennie, zaczynając od pierwszych oznak zaczerwienienia lub mrowienia.
Wygaśnięcie i przechowywanie
Przechowuj Caelyx w miejscu niewidocznym i niedostępnym dla dzieci.
Przechowywać w lodówce (2°C - 8°C). Nie zamrażać.
Po rozcieńczeniu:
- Wykazano chemiczną i fizyczną stabilność użytkową przez 24 godziny w temperaturach od 2°C do 8°C.
- Z mikrobiologicznego punktu widzenia produkt należy zużyć natychmiast. Jeśli rozcieńczony roztwór nie zostanie zużyty natychmiast, odpowiedzialność spoczywa na użytkowniku i nie powinien przekraczać 24 godzin w przypadku przechowywania w temperaturze od 2°C do 8°C. Częściowo zużyte fiolki należy usunąć.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na etykiecie i pudełku.
Nie stosować tego leku, jeśli zauważy się osad lub inne rodzaje cząstek.
Nie należy wyrzucać żadnych leków do kanalizacji ani domowych pojemników na odpadki. Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa.Pomoże to chronić środowisko.
Inne informacje
Co zawiera lek Caelyx
- Substancją czynną jest chlorowodorek doksorubicyny. Jeden ml preparatu Caelyx zawiera 2 mg chlorowodorku doksorubicyny w postaci pegylowanych liposomów.
- Pozostałe składniki to: sól sodowa: ?-(2-[1,2-distearoilo-sn-glicerofosfoksy]etylokarbamoil)-omega-metoksypoli(oksyetyleno)-40 (MPEG-DSPE), całkowicie uwodorniona fosfatydylocholina sojowa (HSPC), cholesterol, siarczan amonu, sacharoza, histydyna, woda do wstrzykiwań, kwas solny i wodorotlenek sodu.
Caelyx 2 mg/ml koncentrat do sporządzania roztworu do infuzji: fiolki o objętości 10 ml (20 mg) lub 25 ml (50 mg).
Jak wygląda lek Caelyx i co zawiera opakowanie
Roztwór do infuzji jest sterylny, przezroczysty i czerwony. Caelyx jest dostępny w szklanych ampułkach w pojedynczych opakowaniach lub zawierających 10 fiolek.
Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
Poniższe informacje są przeznaczone wyłącznie dla personelu medycznego i pracowników służby zdrowia:
Z roztworem Caelyx należy obchodzić się ostrożnie. Wymagane jest używanie rękawiczek.W przypadku kontaktu Caelyx ze skórą lub błonami śluzowymi, należy natychmiast dokładnie przemyć wodą z mydłem.Z preparatem Caelyx należy obchodzić się i usuwać zgodnie ze środkami ostrożności wskazanymi dla innych leków przeciwnowotworowych.
Określ dawkę preparatu Caelyx do podania (w zależności od zalecanej dawki i powierzchni ciała pacjenta). Pobrać odpowiednią objętość preparatu Caelyx za pomocą sterylnej strzykawki. Konieczna jest praca w ściśle aseptycznych warunkach, ponieważ Caelyx nie zawiera konserwantów ani środków bakteriostatycznych. Przed podaniem właściwą dawkę preparatu Caelyx należy rozcieńczyć w 5% roztworze glukozy (50 mg/ml) do infuzji dożylnej. Do dawek <90 mg Caelyx rozcieńczyć w 250 ml i do dawek? 90 mg rozcieńczonego Caelyx w 500 ml.
Aby zmniejszyć ryzyko wystąpienia reakcji na wlew, dawkę początkową należy podawać z szybkością nieprzekraczającą 1 mg / min. Jeśli nie obserwuje się reakcji na wlew, kolejne wlewy preparatu Caelyx można podawać przez 60 minut.
W programie badań klinicznych dotyczących raka piersi dozwolona była modyfikacja wlewu u pacjentek, u których wystąpiła reakcja po podaniu, taka jak: 5% całkowitej dawki podano powoli w ciągu pierwszych 15 minut, tolerowany bez reakcji, wlew szybkość była podwojona przez następne 15 minut. Jeśli tolerowana, infuzja została zakończona w ciągu następnej godziny, co dało całkowity czas wstrzyknięcia 90 minut.
Jeśli u pacjenta wystąpią wczesne objawy lub oznaki reakcji na infuzję, należy natychmiast przerwać infuzję, podać odpowiednie premedykacje (leki przeciwhistaminowe i/lub krótkodziałające kortykosteroidy) i wznowić infuzję z mniejszą szybkością.
Stosowanie do infuzji dożylnych innych niż 5% roztworu glukozy (50 mg/ml) rozcieńczalników lub obecność jakiegokolwiek środka bakteriostatycznego, takiego jak alkohol benzylowy, może powodować precypitację preparatu Caelyx.
Zaleca się podłączenie linii infuzyjnej zawierającej preparat Caelyx do bocznego wlotu wlewu 5% glukozy (50 mg/ml). Infuzję można podawać przez żyłę obwodową. Nie stosować z filtrami wbudowanymi.
Ulotka pakietu źródłowego: AIFA (Włoska Agencja Leków). Treść opublikowana w styczniu 2016 r. Przedstawione informacje mogą być nieaktualne.
Aby mieć dostęp do najbardziej aktualnej wersji, warto wejść na stronę AIFA (Włoskiej Agencji Leków). Zastrzeżenie i przydatne informacje.
01.0 NAZWA PRODUKTU LECZNICZEGO
CAELYX 2 MG/ML KONCENTRAT DO SPORZĄDZANIA ROZTWORU DO INFUZJI
02.0 SKŁAD JAKOŚCIOWY I ILOŚCIOWY
Jeden ml preparatu Caelyx zawiera 2 mg chlorowodorku doksorubicyny w postaci pegylowanych liposomów.
Caelyx składa się z preparatu liposomalnego, w którym chlorowodorek doksorubicyny jest zamknięty w liposomach, na których powierzchni jest związany glikol metoksypolietylenowy (MPEG). Proces ten, zwany pegylacją, chroni liposomy przed rozpoznaniem przez fagocytarny układ jednojądrzasty (MPS), wydłużając czas ich krążenia we krwi.
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
03.0 POSTAĆ FARMACEUTYCZNA
Koncentrat do sporządzania roztworu do infuzji
Zawiesina jest sterylna, przezroczysta i czerwona.
04.0 INFORMACJE KLINICZNE
04.1 Wskazania terapeutyczne
Caelyx jest wskazany:
- W monoterapii u pacjentów z rakiem piersi z przerzutami, w przypadku zwiększonego ryzyka sercowego.
- W leczeniu zaawansowanego raka jajnika u kobiet, u których chemioterapia pierwszego rzutu oparta na platynie zakończyła się niepowodzeniem.
- W skojarzeniu z bortezomibem w leczeniu postępującego szpiczaka mnogiego u pacjentów, którzy otrzymali wcześniej co najmniej jedno leczenie i którzy przeszli lub nie mogą przejść przeszczepu szpiku kostnego.
- Do leczenia mięsaka Kaposi'ego związanego z AIDS (KS-AIDS), u pacjentów z małą liczbą komórek CD4 (limfocyty CD4 3) i rozlaną chorobą śluzówkowo-skórną lub trzewną.
Caelyx może być stosowany jako chemioterapia systemowa pierwszego lub drugiego rzutu u pacjentów z AIDS-KS z zaawansowaną chorobą lub u pacjentów nietolerujących wcześniejszego leczenia systemową chemioterapią skojarzoną z użyciem co najmniej dwóch z następujących substancji: alkaloidu barwinka, bleomycyny i standardowej doksorubicyny ( lub „inną antracyklinę”).
04.2 Dawkowanie i sposób podawania
Caelyx powinien być podawany wyłącznie pod nadzorem onkologa specjalizującego się w podawaniu środków cytotoksycznych.
Caelyx posiada unikalne właściwości farmakokinetyczne; dlatego nie należy go stosować zamiennie z innymi preparatami chlorowodorku doksorubicyny.
Rak piersi / Rak jajnika :
Preparat Caelyx należy podawać dożylnie w dawce 50 mg/m2 raz na 4 tygodnie do progresji choroby i tolerancji leczenia przez pacjenta.
Szpiczak mnogi : Preparat Caelyx podaje się w dawce 30 mg/m2 w 4. dniu 3-tygodniowego schematu bortezomibu w postaci 1-godzinnego wlewu dożylnego bezpośrednio po infuzji bortezomibu.Schemat bortezomibu obejmuje dawkę 1,3 mg/m2 w dniach 1, 4, 8 i 11 co 3 tygodnie Terapię należy powtarzać tak długo, jak pacjent wykazuje zadowalającą odpowiedź i jest w stanie tolerować leczenie Dawka w 4. dniu obu leków może być opóźniona do 48 godzin, jeśli jest to konieczne ze względów medycznych Dawki bortezomibu powinny być oddzielone co najmniej 72 godzinami.
Do dawek dożylnych.
W przypadku dawek ≥ 90 mg: rozcieńczyć preparat Caelyx w 500 ml 5% roztworu glukozy (50 mg/ml) do infuzji dożylnej.
Aby zminimalizować ryzyko wystąpienia reakcji związanych z infuzją, dawkę początkową należy podawać z szybkością nieprzekraczającą 1 mg/minutę.Jeśli nie obserwuje się reakcji, kolejne infuzje preparatu Caelyx można podawać przez 60 minut.
U tych pacjentów, u których wystąpiła reakcja po podaniu, zezwolono na modyfikację wlewu, na przykład:
5% całkowitej dawki należy podawać powoli przez pierwsze 15 minut. Jeśli jest tolerowane bez reakcji, szybkość wlewu można podwoić przez następne 15 minut. Jeśli jest tolerowane, infuzję można zakończyć w ciągu następnej godziny, co daje całkowity czas wstrzyknięcia 90 minut.
Mięsak Kaposiego związany z AIDS :
Caelyx podaje się dożylnie w dawkach 20 mg/m2 co dwa do trzech tygodni. Unikać przerw krótszych niż 10 dni, ponieważ nie można wykluczyć nagromadzenia produktu i wzrostu toksyczności. Aby uzyskać odpowiedź terapeutyczną, zaleca się leczenie pacjentów przez okres od dwóch do trzech miesięcy. Kontynuuj leczenie w razie potrzeby, aby utrzymać odpowiedź terapeutyczną.
Dawkę preparatu Caelyx rozcieńcza się w 250 ml 5% roztworu glukozy (50 mg/ml) do infuzji dożylnej i podaje w infuzji dożylnej przez 30 minut.
Dla wszystkich pacjentów :
Jeśli u pacjenta wystąpią wczesne oznaki lub objawy reakcji na infuzję (patrz punkty 4.4 i 4.8), należy natychmiast przerwać infuzję, podać odpowiednią premedykację (leki przeciwhistaminowe i (lub) krótko działające kortykosteroidy) i wznowić infuzję w późniejszym czasie.
Nie podawać leku Caelyx w postaci bolusa lub nierozcieńczonego roztworu. Zaleca się podłączenie linii infuzyjnej zawierającej preparat Caelyx do bocznego wlotu dożylnego wlewu 5% glukozy (50 mg/ml) w celu dalszego rozcieńczenia roztworu i zminimalizowania ryzyka zakrzepicy i wynaczynienia. Wlew można podawać do żyły obwodowej Nie stosować z filtrami wbudowanymi Caelyx nie wolno podawać domięśniowo ani podskórnie (patrz punkt 6.6).
W przypadku działań niepożądanych, takich jak erytrodyzestezja dłoniowo-podeszwowa (PPE), zapalenie jamy ustnej lub toksyczność hematologiczna, dawkę można zmniejszyć lub odroczyć podanie. W poniższych tabelach przedstawiono wytyczne dotyczące dostosowywania dawki preparatu Caelyx po tych działaniach niepożądanych Klasyfikacja toksyczności w tych tabelach opiera się na wspólnych kryteriach toksyczności National Cancer Institute (NCI-CTC).
Tabele dotyczące PPE (tabela 1) i zapalenia jamy ustnej (tabela 2) przedstawiają schemat dostosowywania dawki podczas badań klinicznych w leczeniu raka piersi lub raka jajnika (modyfikacja zalecanego 4-tygodniowego przebiegu leczenia): jeśli te objawy wystąpią u pacjentów w przypadku KS-AIDS w podobny sposób można zmodyfikować zalecany cykl leczenia 2-3 tygodnie.
Tabela toksyczności hematologicznej (Tabela 3) przedstawia schemat zastosowany do modyfikacji dawki podczas badań klinicznych prowadzonych wyłącznie u pacjentek z rakiem piersi lub jajnika. Dostosowanie dawki u pacjentów z AIDS-KS, patrz punkt 4.8.
Wskazówki dotyczące dostosowania dawki leku Caelyx
U pacjentów ze szpiczakiem mnogim leczonych preparatem Caelyx w skojarzeniu z bortezomibem, u których wystąpił zespół PPE lub zapalenie jamy ustnej, dawkę preparatu Caelyx należy dostosować zgodnie z opisem w Tabelach 1 i 2 powyżej. Poniższa tabela 4 przedstawia schemat zastosowany w przypadku innych modyfikacji dawki podczas badania klinicznego w leczeniu pacjentów ze szpiczakiem mnogim, którzy otrzymywali preparat Caelyx i bortezomib w terapii skojarzonej. Więcej informacji na temat dawkowania i dostosowywania dawki bortezomibu można znaleźć w Charakterystyce Produktu Leczniczego bortezomibu (ChPL).
* więcej informacji na temat dawkowania bortezomibu i dostosowywania dawki znajduje się w ChPL bortezomibu
Pacjenci z niewydolnością wątroby : farmakokinetyka preparatu Caelyx, określona u niewielkiej liczby pacjentów z podwyższonym poziomem bilirubiny całkowitej, nie różni się od farmakokinetyki pacjentów z prawidłową bilirubiną całkowitą; jednak do czasu uzyskania dodatkowych informacji dawkę preparatu Caelyx u pacjentów z niewydolnością wątroby należy zmniejszyć na podstawie doświadczeń z badań klinicznych dotyczących raka piersi i jajnika, w następujący sposób: na początku leczenia, jeśli stężenie bilirubiny wynosi od 1,2 do 3,0 mg/dl , pierwsza dawka zostaje zmniejszona o 25%. Jeśli stężenie bilirubiny wynosi >3,0 mg/dl, pierwsza dawka zostaje zmniejszona o 50%. Jeśli pacjent toleruje pierwszą dawkę bez wzrostu stężenia bilirubiny w surowicy lub enzymów wątrobowych, dawkę drugiego cyklu można zwiększyć do następnego poziomu, to znaczy, jeśli pierwsza dawka została zmniejszona o 25%, doprowadzić pełną dawkę do drugi cykl; jeśli pierwsza dawka została zmniejszona o 50%, zwiększyć do 75% pełnej dawki w drugim cyklu. Jeśli tolerowane, dawkowanie można zwiększyć do pełnej dawki w kolejnych cyklach. Preparat Caelyx można podawać pacjentom z przerzutami do wątroby i współistniejącym wzrostem stężenia bilirubiny i enzymów wątrobowych do 4 razy powyżej górnej granicy normy.Przed podaniem preparatu Caelyx należy ocenić czynność wątroby za pomocą konwencjonalnych klinicznych testów laboratoryjnych, takich jak ALT/AST, zasadowe fosfataza i bilirubina.
Pacjenci z niewydolnością nerek : Ponieważ doksorubicyna jest metabolizowana przez wątrobę i wydalana z żółcią, nie jest wymagane dostosowanie dawki. Populacyjne dane farmakokinetyczne (w badanym zakresie klirensu kreatyniny 30-156 ml/min) wykazują, że wydalanie preparatu Caelyx nie jest zależne od czynności nerek Brak danych farmakokinetycznych u pacjentów z klirensem kreatyniny mniejszym niż 30 ml/min.
Pacjenci z KS-AIDS po splenektomii : Ponieważ nie ma doświadczenia w stosowaniu preparatu Caelyx u pacjentów poddawanych splenektomii, jego stosowanie nie jest zalecane.
Pacjenci pediatryczni Doświadczenie u dzieci jest ograniczone Nie zaleca się stosowania preparatu Caelyx u pacjentów w wieku poniżej 18 lat.
Starsi pacjenci : Analiza populacji pokazuje, że wiek w badanym zakresie (21-75 lat) nie zmienia znacząco farmakokinetyki preparatu Caelyx.
04.3 Przeciwwskazania
• Nadwrażliwość na substancję czynną lub na którąkolwiek substancję pomocniczą.
Preparatu Caelyx nie należy stosować w leczeniu AIDS-KS, które można skutecznie leczyć za pomocą terapii miejscowej lub ogólnoustrojowego alfa-interferonu.
04.4 Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania
Toksyczność sercowa : Zaleca się, aby wszyscy pacjenci leczeni preparatem Caelyx byli rutynowo poddawani częstym elektrokardiogramom (EKG). Przejściowe zmiany w zapisie EKG, takie jak spłaszczenie załamka T, podpoziomowanie odcinka ST i łagodne zaburzenia rytmu serca, nie są uważane za wiążące sygnały do przerwania leczenia preparatem Caelyx.Jednak zmniejszenie zespołu QRS jest uważane za najbardziej wskazujący objaw sercowy Jeśli wystąpi taka zmiana, należy rozważyć decydujące badanie toksyczności antracyklin w mięśniu sercowym, tj. biopsję mięśnia sercowego.
Bardziej specyficznymi metodami elektrokardiogramu do oceny i kontroli czynności serca są pomiar frakcji wyrzutowej lewej komory za pomocą echokardiografii lub, najlepiej, za pomocą arteriografii wieloportowej (MUGA).Metody te muszą być rutynowo stosowane przed rozpoczęcia leczenia preparatem Caelyx i należy je powtarzać okresowo w trakcie leczenia. Ocena funkcji lewej komory serca jest uważana za niezbędną przed każdym dodatkowym podaniem preparatu Caelyx, które przekracza dozwoloną skumulowaną dawkę antracykliny w ciągu życia 450 mg/m2.
Opisane powyżej testy i metody oceny dotyczące monitorowania pracy serca podczas leczenia antracyklinami powinny być stosowane w następującej kolejności: monitorowanie EKG, pomiar frakcji wyrzutowej lewej komory, biopsja endomiokardialna Jeśli wynik badania wskazuje na możliwość urazu związanego z leczeniem preparatem Caelyx, korzyści z kontynuacji Terapię należy dokładnie rozważyć pod kątem ryzyka uszkodzenia mięśnia sercowego.
Pacjentów z chorobami serca, którzy wymagają leczenia preparatem Caelyx, należy leczyć tylko wtedy, gdy korzyści przewyższają ryzyko.
Należy zachować ostrożność u pacjentów z zaburzeniami czynności serca leczonych preparatem Caelyx.
W przypadku podejrzenia kardiomiopatii, tj. gdy frakcja wyrzutowa lewej komory znacznie się zmniejszyła w stosunku do wartości sprzed leczenia i/lub frakcja wyrzutowa lewej komory jest niższa od wartości odpowiedniej z punktu widzenia prognostycznego (np.
Zastoinowa niewydolność serca spowodowana kardiomiopatią może wystąpić nagle, nawet kilka tygodni po odstawieniu leczenia, bez poprzedzonej zmianami w elektrokardiogramie.
Należy zachować ostrożność u pacjentów leczonych innymi antracyklinami. Całkowita dawka chlorowodorku doksorubicyny musi również uwzględniać wcześniejsze (lub jednoczesne) leczenie związkami kardiotoksycznymi, takimi jak inne antracykliny/antrachinony lub np. 5-fluorouracyl. Kardiotoksyczność może również wystąpić w przypadku skumulowanych dawek antracyklin poniżej 450 mg/m2 u pacjentów po wcześniejszym napromienianiu śródpiersia lub u pacjentów leczonych jednocześnie cyklofosfamidem.
Na poziomie serca profil bezpieczeństwa zalecanego dawkowania zarówno w przypadku raka piersi, jak i raka jajnika (50 mg/m2) jest porównywalny z profilem 20 mg/m2 u pacjentów z AIDS-KS (patrz punkt 4.8).
Mielosupresja : Wielu pacjentów leczonych preparatem Caelyx cierpi na mielosupresję z powodu różnych czynników, takich jak istniejące wcześniej zakażenie wirusem HIV lub liczne współistniejące lub wcześniejsze terapie lub nowotwory obejmujące szpik kostny. W głównym badaniu z udziałem pacjentek z rakiem jajnika leczonych dawką 50 mg/m2 mielosupresja była na ogół łagodna do umiarkowanej, odwracalna i nie była związana z epizodami zakażenia neutropenicznego lub posocznicy. Ponadto w kontrolowanym badaniu klinicznym preparatu Caelyx w porównaniu z topotekanem częstość występowania sepsy związanej z leczeniem była znacznie mniejsza w grupie leczonej preparatem Caelyx niż w grupie leczonej topotekanem. z przerzutowym rakiem piersi leczonym preparatem Caelyx w badaniu klinicznym pierwszego rzutu.W przeciwieństwie do doświadczeń u pacjentek z rakiem piersi lub jajnika, mielosupresja wydaje się być działaniem niepożądanym ograniczającym dawkę u pacjentek z AIDS-KS (patrz punkt 4.8). możliwość mieloablacji, okresowe badania krwi należy wykonywać często podczas leczenia preparatem Caelyx, a przynajmniej przed każdą dawką preparatu Caelyx.
Ciężka i uporczywa mielosupresja może prowadzić do nadkażenia lub krwotoku.
W kontrolowanych badaniach klinicznych przeprowadzonych u pacjentów z AIDS-KS w porównaniu ze schematem leczenia bleomycyną/winkrystyną, zakażenia oportunistyczne były najwyraźniej częstsze podczas leczenia preparatem Caelyx. Pacjenci i lekarze muszą być świadomi tej zwiększonej zachorowalności i odpowiednio postępować.
Podobnie jak w przypadku innych leków przeciwnowotworowych uszkadzających DNA, u pacjentów otrzymujących leczenie skojarzone z doksorubicyną zgłaszano wtórną ostrą białaczkę szpikową i mielodysplazję. W związku z tym każdy pacjent leczony doksorubicyną musi być pod kontrolą hematologiczną.
Ze względu na różnice w profilu farmakokinetycznym i schematach dawkowania preparatu Caelyx nie należy stosować zamiennie z innymi postaciami chlorowodorku doksorubicyny.
Reakcje związane z infuzją : W ciągu kilku minut od rozpoczęcia wlewu preparatu Caelyx mogą wystąpić ciężkie i czasami zagrażające życiu reakcje na wlew, które charakteryzują się reakcjami alergicznymi lub anafilaktoidalnymi, których objawami są astma, zaczerwienienie skóry, swędzenie wysypki, ból w klatce piersiowej, gorączka, nadciśnienie, tachykardia, swędzenie, pocenie się. , duszność, obrzęk twarzy, dreszcze, ból pleców, ucisk w klatce piersiowej i gardle i (lub) niedociśnienie Bardzo rzadko obserwowano drgawki jako reakcję podczas wlewu (patrz punkt 4.8). Zwykle tymczasowe wstrzymanie infuzji usuwa te objawy bez dalszej interwencji terapeutycznej. Jednak leki stosowane w leczeniu tych objawów (na przykład leki przeciwhistaminowe, kortykosteroidy, adrenalina i leki przeciwdrgawkowe) oraz sprzęt ratunkowy muszą być dostępne do natychmiastowego użycia. pacjentów, leczenie można wznowić po ustąpieniu wszystkich objawów, bez nawrotu.Reakcje związane z infuzją rzadko powracają po pierwszym cyklu leczenia. Aby zminimalizować ryzyko wystąpienia reakcji związanych z infuzją, początkową dawkę należy podawać z szybkością infuzji nieprzekraczającą 1 mg/minutę (patrz punkt 4.2).
Pacjenci z cukrzycą Należy wziąć pod uwagę, że każda fiolka leku Caelyx zawiera sacharozę i jest podawana w postaci 5% roztworu glukozy (50 mg/ml) do infuzji dożylnej.
Często występujące zdarzenia niepożądane wymagające modyfikacji dawki lub przerwania, patrz punkt 4.8.
04.5 Interakcje z innymi produktami leczniczymi i inne formy interakcji
Nie przeprowadzono formalnych badań interakcji między innymi produktami leczniczymi a preparatem Caelyx, chociaż badania skojarzone fazy II z konwencjonalnymi środkami chemioterapeutycznymi przeprowadzono u pacjentów z nowotworami ginekologicznymi. Należy zachować ostrożność podczas jednoczesnego stosowania leków, o których wiadomo, że wchodzą w interakcje ze standardowym chlorowodorkiem doksorubicyny Caelyx, podobnie jak inne preparaty chlorowodorku doksorubicyny, może nasilać toksyczność innych leków przeciwnowotworowych W badaniach klinicznych u pacjentów z guzami litymi (w tym rakiem piersi i jajnika) leczonych jednocześnie z cyklofosfamidem lub taksanami nie stwierdzono nowych skumulowanych działań toksycznych.U pacjentów z AIDS po podaniu standardowego chlorowodorku doksorubicyny wystąpiły przypadki zaostrzenia krwotocznego zapalenia pęcherza moczowego wywołanego przez cyklofosfamid i nasilonej hepatotoksyczności 6-merkaptopuryny. Ostrożność jest również wymagana, gdy wymagane jest jednoczesne podawanie innych środków cytotoksycznych, w szczególności środków mielotoksycznych.
04.6 Ciąża i laktacja
Ciąża : Uważa się, że chlorowodorek doksorubicyny podawany w okresie ciąży powoduje poważne wady wrodzone. Dlatego preparatu Caelyx nie należy stosować w okresie ciąży, chyba że jest to bezwzględnie konieczne.
Kobietom w wieku rozrodczym należy doradzić, aby unikały ciąży, niezależnie od tego, czy one same lub ich partner są leczeni preparatem Caelyx, czy w ciągu sześciu miesięcy po zakończeniu leczenia preparatem Caelyx (patrz punkt 5.3).
Czas karmienia : Nie wiadomo, czy Caelyx przenika do mleka ludzkiego. Ponieważ wiele leków, w tym antracykliny, przenika do mleka ludzkiego oraz ze względu na możliwość wystąpienia poważnych działań niepożądanych u dziecka, matka musi przerwać karmienie piersią przed rozpoczęciem leczenia preparatem Caelyx. Eksperci ds. zdrowia zalecają kobietom zakażonym wirusem HIV, aby w żadnych okolicznościach nie karmiły piersią swoich dzieci, aby zapobiec przeniesieniu wirusa HIV.
04.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Caelyx nie ma wpływu lub wywiera nieistotny wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn. Jednak badania kliniczne przeprowadzone do tej pory wskazują, że senność i senność nie są często powiązane (
04.8 Działania niepożądane
Najczęstszym działaniem niepożądanym zgłaszanym w badaniach klinicznych raka piersi/jajnika (50 mg/m2 co 4 tygodnie) była erytrodyzestezja dłoniowo-podeszwowa (PPE).Całkowita częstość występowania PPE wynosiła 44,0% - 46,1%. Działania te były w większości łagodne, z ciężkimi (stopień III) przypadkami zgłoszonymi w 17% - 19,5%. Częstość występowania zgłoszonych przypadków zagrażających życiu (stopień IV) obejmowała dłonie i stopy w niskich temperaturach, trzymanie ich w zimnej wodzie (moczenie, kąpiel lub pływanie), unikanie nadmiernych źródeł ciepła / gorącej wody i brak ucisków (bez skarpet, rękawiczek lub ciasne obuwie) PPE wydaje się być związane głównie ze schematem dawkowania i można je zmniejszyć, zwiększając odstęp między dawkami do 1-2 tygodni (patrz punkt 4.2). Jednak u niektórych pacjentów reakcja ta może być ciężka i wyniszczająca i wymagać przerwania leczenia Zapalenie jamy ustnej/błon śluzowych i nudności były również często zgłaszane u pacjentów leczonych z powodu raka piersi/jajnika, podczas gdy u pacjentów z AIDS-KS (20 mg/m2 pc.) co 2 tygodnie) najczęstszym działaniem niepożądanym była mielosupresja (głównie leukopenia) (patrz KS-AIDS). Przypadki PPE zgłoszono u 16% pacjentów ze szpiczakiem mnogim leczonych preparatem Caelyx w skojarzeniu z bortezomibem. Stopień 3. zgłoszono u 5% Nie zgłoszono żadnego przypadku PPE stopnia 4. Najczęściej zgłaszanymi zdarzeniami niepożądanymi (związanymi z leczeniem lub pojawiającymi się podczas leczenia) podczas leczenia skojarzonego (Caelyx + bortezomib) były (40%), biegunka (35%), neutropenia (33%). , małopłytkowość (29%), wymioty (28%), zmęczenie (27%) i zaparcia (22%).
Rak piersi : W badaniu klinicznym III fazy (I97-328), 509 pacjentek z zaawansowanym rakiem piersi, które nie otrzymywały wcześniej chemioterapii z powodu choroby przerzutowej, leczono preparatem Caelyx (n = 254) w dawce 50 mg/m2 co 4 tygodnie lub doksorubicyną (n = 255) w dawce 60 mg/m2 co 3 tygodnie. Następujące częste działania niepożądane były zgłaszane częściej podczas stosowania doksorubicyny niż preparatu Caelyx: nudności (53% vs 37%; stopień III/IV 5% vs 3%), wymioty (31% vs 19%; stopień III/IV 4 % vs mniej niż 1%), różne objawy łysienia (66% vs 20%), wyraźne łysienie (54% vs 7%) i neutropenia (10% vs 4%; stopień III/IV 8% vs. 2%).
Zapalenie błony śluzowej (23% vs. 13%; stopień III/IV 4% vs. 2%) i zapalenie jamy ustnej (22% vs. 15%; stopień III/IV 5% vs. 2%) były zgłaszane częściej po zastosowaniu preparatu Caelyx niż po doksorubicynie . Średni czas trwania najczęstszych poważnych zdarzeń (stopień III/IV) w obu grupach wynosił 30 dni lub mniej. W Tabeli 5 znajduje się pełna lista działań niepożądanych zgłaszanych u pacjentów leczonych preparatem Caelyx.
Częstość występowania zagrażających życiu (stopień IV) skutków hematologicznych wynosiła
Klinicznie istotne nieprawidłowości laboratoryjne (stopień III i IV) były nieliczne w tej grupie, z podwyższonymi poziomami bilirubiny całkowitej, AST i ALT zgłoszonymi u 2,4%, 1,6% i
* erytrodyzestezja dłoniowo-podeszwowa (zespół ręka-stopa).
Rak jajnika : 512 pacjentek z rakiem jajnika (subpopulacja 876 pacjentek z guzami litymi) było leczonych w badaniach klinicznych preparatem Caelyx w dawce 50 mg/m2. W tabeli 6 przedstawiono działania niepożądane zgłaszane u pacjentów leczonych preparatem Caelyx.
* erytrodyzestezja dłoniowo-podeszwowa (zespół ręka-stopa).
Mielosupresja była w większości łagodna do umiarkowanej i możliwa do opanowania. Posocznica związana z leukopenią nie była często obserwowana (
W subpopulacji 410 pacjentek z rakiem jajnika klinicznie istotne zmiany parametrów laboratoryjnych podczas badań klinicznych preparatu Caelyx obejmowały zwiększenie stężenia bilirubiny całkowitej (zwykle u pacjentek z przerzutami do wątroby) (5%) i stężenia kreatyniny w surowicy (5%). Rzadziej zgłaszano wzrost poziomu AST (
Pacjenci z guzami litymi: W większym badaniu kohortowym obejmującym 929 pacjentów z guzami litymi (w tym raka piersi i jajnika) leczonych głównie dawką 50 mg/m2 co 4 tygodnie, profil bezpieczeństwa i częstość występowania zdarzeń niepożądanych były porównywalne z tymi u pacjentów leczonych w pilotażowych badaniach nad rakiem piersi i jajnika.
Szpiczak mnogi: W badaniu III fazy z 646 pacjentów ze szpiczakiem mnogim, którzy otrzymali wcześniej co najmniej jedno leczenie, 318 było leczonych preparatem Caelyx 30 mg/m2 podawanym w postaci 1-godzinnego wlewu dożylnego w 4. dniu leczenia bortezomibem. Bortezomib podawano w dawce 1,3 mg/m2 w dniach 1, 4, 8 i 11 co trzy tygodnie w skojarzeniu z preparatem Caelyx lub w monoterapii. W tabeli 7 przedstawiono działania niepożądane zgłoszone u ≥ 5% pacjentów leczonych preparatem Caelyx i bortezomibem w leczeniu skojarzonym.
Neutropenia, trombocytopenia i niedokrwistość były najczęściej zgłaszanymi hematologicznymi działaniami niepożądanymi w przypadku skojarzenia preparatu Caelyx i bortezomibu oraz samego bortezomibu.Częstość neutropenii stopnia 3 i 4 była wyższa w grupie terapii skojarzonej niż w grupie leczonej. w monoterapii (28% vs 14%). Częstość występowania małopłytkowości stopnia 3 i 4 była wyższa w przypadku terapii skojarzonej niż w monoterapii (22% vs 14%), częstość występowania niedokrwistości była porównywalna w obu grupach (7% vs 5%).
Przypadki zapalenia jamy ustnej zgłaszano częściej w grupie skojarzonej (16%) niż w grupie monoterapii (3%) i wiele z nich miało stopień 2. lub niższy. zgłoszono zapalenie jamy ustnej.
Nudności i wymioty były zgłaszane częściej w grupie skojarzonej (40% i 28%), niż w grupie monoterapii (32% i 15%), większość miała nasilenie 1. i 2. stopnia.
Przerwanie leczenia jednym lub obydwoma lekami z powodu działań niepożądanych wystąpiło u 38% pacjentów. Najczęstsze działania niepożądane prowadzące do przerwania leczenia bortezomibem i preparatem Caelyx obejmowały PPE, nerwobóle, neuropatię obwodową, obwodową neuropatię czuciową, małopłytkowość, zmniejszoną frakcję wyrzutową i zmęczenie.
* erytrodyzestezja dłoniowo-podeszwowa (zespół ręka-stopa).
** Działania niepożądane stopnia 3 i 4 oparte są na zdarzeniach niepożądanych o każdym nasileniu z „całkowitą częstością ≥ 5% (patrz działania niepożądane wymienione w pierwszej kolumnie)
KS-AIDS : Badania kliniczne u pacjentów z AIDS-KS leczonych preparatem Caelyx w dawce 20 mg/m2 wskazują, że najczęstszym działaniem niepożądanym związanym z podawaniem preparatu Caelyx jest mielosupresja, która również występuje bardzo często (u około połowy pacjentów).
Leukopenia jest najczęściej zgłaszanym działaniem niepożądanym związanym ze stosowaniem preparatu Caelyx w tej populacji; zgłaszano neutropenię, niedokrwistość i trombocytopenię, które mogą wystąpić na wczesnym etapie leczenia. Toksyczność hematologiczna może wymagać zmniejszenia dawki, przerwania lub odroczenia leczenia. Tymczasowo wstrzymaj leczenie preparatem Caelyx u pacjentów, u których bezwzględna liczba neutrofili wynosi 3 i/lub liczba płytek krwi wynosi 3. G-CSF (lub GM-CSF) można podawać jako terapię wspomagającą w kolejnych cyklach, gdy bezwzględna liczba neutrofili wynosi 3 Toksyczność hematologiczna u pacjentek z rakiem jajnika jest mniej ciężka niż u pacjentek z AIDS-KS (patrz punkt dotyczący pacjentek z rakiem jajnika powyżej).
Działania niepożądane dotyczące układu oddechowego były często obserwowane w badaniach klinicznych preparatu Caelyx i mogą być związane z zakażeniami oportunistycznymi u pacjentów z AIDS. Zakażenia oportunistyczne występowały u pacjentów z mięsakiem Kaposiego po podaniu preparatu Caelyx; takie infekcje są częste u pacjentów z niedoborem odporności wywołanym przez HIV. Najczęstszymi zakażeniami oportunistycznymi obserwowanymi w badaniach klinicznych były kandydoza, wirus cytomegalii, opryszczka zwykła, zapalenie płuc Pneumocystis carinii oraz kompleks Mycobacterium avium.
Działania niepożądane obserwowane u pacjentów z KS-AIDS według kategorii częstości CIOMS III (bardzo często (>1/10); często (>1/100, 1/1000,
Infekcje i infestacje:
Często: drożdżyca jamy ustnej
Zaburzenia układu krwionośnego i limfatycznego:
Bardzo często: neutropenia, niedokrwistość, leukopenia
Często: małopłytkowość
Zaburzenia metabolizmu i odżywiania:
Często: anoreksja
Zaburzenia psychiczne:
Niezbyt często: zamieszanie
Zaburzenia układu nerwowego:
Często: zawroty głowy
Niezbyt często: parestezje
Zaburzenia oka:
Często: zapalenie siatkówki
Zaburzenia naczyniowe:
Często: rozszerzenie naczyń
Zaburzenia układu oddechowego, klatki piersiowej i śródpiersia:
Często: duszność
Zaburzenia żołądkowo-jelitowe:
Bardzo często: nudności
Często: biegunka, zapalenie jamy ustnej, wymioty, owrzodzenie jamy ustnej, ból brzucha, zapalenie języka, zaparcia, nudności i wymioty
Zaburzenia skóry i tkanki podskórnej:
Często: łysienie, wysypka
Niezbyt często: erytrodyzestezja dłoniowo-podeszwowa (PPE)
Zaburzenia ogólne i stany w miejscu podania:
Często: astenia, gorączka, ostre reakcje związane z infuzją
Testy diagnostyczne:
Często: utrata masy ciała
Inne rzadziej spotykane działania niepożądane (reakcje anafilaktyczne. Po wprowadzeniu produktu do obrotu w tej populacji rzadko zgłaszano wysypkę pęcherzową).
Klinicznie istotne nieprawidłowości laboratoryjne pojawiały się często (≥ 5%) i obejmowały podwyższenie poziomu fosfatazy alkalicznej, AspAT i bilirubiny, które uznano za związane z chorobą, a nie z Caelyx. Zmniejszenie stężenia hemoglobiny i płytek krwi stwierdzano rzadziej (wirus HIV, a nie w Caelyx.
Wszyscy pacjenci U 100 z 929 pacjentów (10,8%) z guzami litymi zgłoszono reakcje związane z infuzją preparatu Caelyx określone następującymi wskaźnikami Costart: reakcja alergiczna, reakcja anafilaktoidalna, astma, obrzęk twarzy, niedociśnienie, rozszerzenie naczyń krwionośnych, pokrzywka, ból pleców, ból w klatce piersiowej, dreszcze, gorączka, nadciśnienie, tachykardia, niestrawność, nudności, zawroty głowy, duszność, zapalenie gardła, wysypka, świąd, pocenie się, reakcje w miejscu wstrzyknięcia i interakcje między lekami Rzadko (2%) zgłaszane jest trwałe przerwanie leczenia. Reakcje na wlew (12,4%) i przypadki przerwania leczenia (1,5%) zgłaszano w programie leczenia raka piersi z podobną częstością.U pacjentów ze szpiczakiem mnogim leczonych preparatem Caelyx i bortezomibem, związane z wlewem reakcje zgłaszano z częstością 3%. U pacjentów z AIDS-KS reakcje związane z infuzją charakteryzują się zaczerwienieniem, dusznością, obrzękiem twarzy, bólem głowy, dreszczami, bólem pleców, uciskiem w klatce piersiowej i gardle i (lub) niedociśnieniem. - 10%. Bardzo rzadko obserwowano drgawki jako reakcję na infuzję U wszystkich pacjentów reakcje związane z infuzją występowały głównie podczas pierwszej infuzji. Tymczasowe wstrzymanie infuzji zwykle usuwa te objawy bez konieczności dalszego leczenia. U prawie wszystkich pacjentów leczenie preparatem Caelyx można wznowić po ustąpieniu wszystkich objawów bez nawrotu. Reakcje na wlew rzadko występują po pierwszym cyklu leczenia preparatem Caelyx (patrz punkt 4.2).
U pacjentów leczonych preparatem Caelyx zgłaszano mielosupresję związaną z niedokrwistością, trombocytopenią, leukopenią i neutropenią, a rzadko neutropenią typu gorączkowego.
Zapalenie jamy ustnej występowało u pacjentów leczonych ciągłymi wlewami konwencjonalnego chlorowodorku doksorubicyny i często u pacjentów leczonych preparatem Caelyx. Zapalenie jamy ustnej nie przeszkadzało pacjentom w zakończeniu leczenia i generalnie nie wymagało dostosowania dawki, chyba że miało to wpływ na zdolność pacjenta do odżywiania się. W takim przypadku odstęp między dawkami można wydłużyć o 1-2 tygodnie lub dawkę zmniejszyć (patrz punkt 4.2).
Terapia doksorubicyną w dopuszczalnych dawkach skumulowanych w całym okresie życia > 450 mg/m2 lub niższych dawkach u pacjentów z kardiologicznymi czynnikami ryzyka wiąże się z większą częstością występowania zastoinowej niewydolności serca. dawki preparatu Caelyx większe niż 460 mg/m2 nie wykazały kardiomiopatii wywołanej przez antracykliny.Zalecana dawka preparatu Caelyx dla pacjentów z AIDS-KS wynosi 20 mg/m2 co dwa do trzech tygodni.Skumulowana dawka, przy której kardiotoksyczność może stać się ryzykiem dla tych pacjentów z AIDS-KS (> 400 mg/m2) wymagałoby to ponad 20 cykli terapii Caelyx, której podanie trwa 40-60 tygodni.
Ośmiu pacjentów z guzami litymi leczonych skumulowanymi dawkami antracyklin od 509 mg/m2 do 1680 mg/m2 poddano biopsji endomiokardialnej. Skala kardiotoksyczności według Billinghama wynosiła 0 - 1,5. Wyniki te odpowiadają brakowi lub łagodnej kardiotoksyczności.
W dużym badaniu fazy III w porównaniu z doksorubicyną, 58/509 (11,4%) zrandomizowanych pacjentów (10 leczonych preparatem Caelyx w dawce 50 mg/m2 / co 4 tygodnie w porównaniu z 48 pacjentami leczonymi doksorubicyną w dawce 60 mg/m2 / co 3 tygodnie) spełniły zdefiniowane w protokole kryteria kardiotoksyczności podczas leczenia i (lub) obserwacji. Kardiotoksyczność została zdefiniowana jako zmniejszenie o co najmniej 20 punktów od wartości, jeśli spoczynkowa LVEF pozostała w normie lub jako zmniejszenie o co najmniej 10 punktów, jeśli LVEF stała się nieprawidłowa (mniej niż dolna granica normalna). U żadnego z 10 pacjentów leczonych preparatem Caelyx, u których stwierdzono kardiotoksyczność na podstawie wartości LVEF, nie wystąpiły charakterystyczne oznaki i objawy CHF. Z kolei u 10 z 48 pacjentów leczonych doksorubicyną, u których stwierdzono kardiotoksyczność na podstawie wartości LVEF, wystąpiły również objawy przedmiotowe i podmiotowe CHF.
U pacjentek z guzami litymi, w tym w subpopulacji chorych na raka piersi i jajnika, leczonych dawką 50 mg/m2/cykl skumulowanymi dawkami antracykliny przez cały okres życia, tj. do 1532 mg/m2, klinicznie znaczna dysfunkcja serca była niska. Spośród 418 pacjentów leczonych preparatem Caelyx w dawce 50 mg/m2/cykl i monitorowanych pod kątem frakcji wyrzutowej lewej komory (LVEF) przed leczeniem i co najmniej raz podczas obserwacji za pomocą badania MUGA, 88 pacjentów otrzymało skumulowaną dawkę antracyklin > 400 mg/ m2, poziom ekspozycji związany ze zwiększonym ryzykiem toksyczności sercowo-naczyniowej w przypadku konwencjonalnej doksorubicyny. Spośród tych 88 pacjentów tylko 13 (15%) zgłosiło co najmniej jedną „istotną klinicznie zmianę LVEF, zdefiniowaną jako wartość LVEF mniejsza niż 45% lub spadek o co najmniej 20 punktów w stosunku do wartości wyjściowych. Ponadto tylko 1 pacjent (leczeni skumulowaną dawką antracyklin 944 mg/m2) przerwali leczenie z powodu klinicznych objawów zastoinowej niewydolności serca.
Podobnie jak w przypadku innych leków przeciwnowotworowych uszkadzających DNA, u pacjentów otrzymujących leczenie skojarzone z doksorubicyną zgłaszano wtórną ostrą białaczkę szpikową i mielodysplazję. W związku z tym każdy pacjent leczony doksorubicyną musi być pod kontrolą hematologiczną.
Caelyx jest uważany za środek drażniący, chociaż do tej pory bardzo rzadko obserwowano miejscową martwicę po wynaczynieniu. Badania na zwierzętach wskazują, że podawanie chlorowodorku doksorubicyny w postaci liposomalnej zmniejsza ryzyko uszkodzenia wynaczynienia. W przypadku wystąpienia oznak i objawów wynaczynienia (np. kłujący ból, rumień) należy natychmiast przerwać infuzję i wznowić ją do innej żyły.Przyłożenie lodu do miejsca wynaczynienia na około 30 minut może pomóc złagodzić reakcję. Preparatu Caelyx nie wolno podawać domięśniowo ani podskórnie.
Rzadko po podaniu preparatu Caelyx mogą wystąpić nawroty reakcji skórnych po wcześniejszej radioterapii.
Od czasu wprowadzenia preparatu Caelyx do obrotu rzadko zgłaszano występowanie poważnych chorób skóry, takich jak rumień wielopostaciowy, zespół Stevensa-Johnsona i toksyczne martwicze oddzielanie się naskórka.
U pacjentów leczonych preparatem Caelyx niezbyt często obserwowano przypadki żylnej choroby zakrzepowo-zatorowej, w tym zakrzepowe zapalenie żył, zakrzepicę żylną i zatorowość płucną. Ponieważ jednak pacjenci z nowotworami są narażeni na zwiększone ryzyko rozwoju choroby zakrzepowo-zatorowej, nie można ustalić związku przyczynowego.
04.9 Przedawkowanie
Ostre przedawkowanie chlorowodorku doksorubicyny pogarsza toksyczne działanie zapalenia błon śluzowych, leukopenii i małopłytkowości. Leczenie ostrego przedawkowania u pacjentów z ciężką mielosupresją wymaga hospitalizacji, podawania antybiotyków, przetoczenia płytek krwi i granulocytów oraz leczenia objawowego zapalenia błony śluzowej.
05.0 WŁAŚCIWOŚCI FARMAKOLOGICZNE
05.1 Właściwości farmakodynamiczne
Grupa farmakoterapeutyczna: Leki cytotoksyczne (antracykliny i substancje pokrewne), kod ATC: L01DB.
Substancją czynną preparatu Caelyx jest chlorowodorek doksorubicyny, cytotoksyczny antybiotyk z grupy antracyklin otrzymywany z Streptomyces peucetius zm. Cezjusz. Dokładny mechanizm działania przeciwnowotworowego doksorubicyny nie jest znany. Powszechnie uważa się, że hamowanie syntezy DNA, RNA i białek jest główną przyczyną efektu cytotoksycznego, prawdopodobnie ze względu na interkalację antracykliny między sąsiednimi parami zasad podwójnej helisy DNA, uniemożliwiając jej rozwinięcie się do replikacji.
Randomizowane badanie III fazy porównujące Caelyx z doksorubicyną objęło 509 pacjentów z przerzutowym rakiem piersi. Określony w protokole cel wykazania równoważności preparatu Caelyx w stosunku do doksorubicyny został osiągnięty; względny współczynnik ryzyka (HR) do przeżycia bez progresji choroby (PFS) wyniósł 1,00 (95% CI dla HR = 0,82-1,22) HR leczenie dla PFS po skorygowaniu dla zmiennych prognostycznych odpowiadał PFS dla populacji ITT.
Pierwotna analiza kardiotoksyczności wykazała, że ryzyko wystąpienia incydentu sercowego jako funkcja skumulowanej dawki antracyklin było znacznie niższe w przypadku preparatu Caelyx niż w przypadku doksorubicyny (HR = 3,16, p 2, w przypadku preparatu Caelyx nie wystąpiły żadne zdarzenia sercowe).
Badanie porównawcze III fazy preparatu Caelyx z topotekanem zostało zakończone u 474 pacjentek z nabłonkowym rakiem jajnika, u których nie powiodła się chemioterapia pierwszego rzutu oparta na platynie. C „było korzyścią dla całkowitego przeżycia (OS) pacjentów leczonych preparatem Caelyx w porównaniu z pacjentami leczonymi topotekanem, na co wskazuje względny współczynnik ryzyka (HR) wynoszący 1,216 (95% CI; 1000; 1,478), p = 0,050. , 2 i 3-letnie przeżycia wyniosły odpowiednio 56,3%, 34,7% i 20,2% dla Caelyx w porównaniu do 54,0%, 23,6% i 13,2% dla Topotekanu.
W podgrupie pacjentów z chorobą platynowrażliwą różnica była większa: HR 1,432 (95% CI; 1,066, 1,923), p = 0,017. Wskaźniki przeżycia 1, 2 i 3-letniego wynosiły odpowiednio 74,1%, 51,2% i 28,4% dla Caelyx w porównaniu z 66,2%, 31,0% i 17,5% dla Topotekanu.
Leczenie było podobne w podgrupie pacjentów z chorobą niewrażliwą na platynę: HR 1,069 (95% CI; 0,823; 1,387), p = 0,618. Wskaźniki przeżycia 1, 2 i 3-letniego wynosiły odpowiednio 41,5%, 21,1% i 13,8% dla Caelyx w porównaniu z 43,2%, 17,2% i 9,5% dla Topotekanu.
U 646 pacjentów ze szpiczakiem mnogim, którzy otrzymali wcześniej co najmniej jedną terapię i u których nie doszło do progresji po leczeniu opartym na antracyklinach, przeprowadzono otwarte, wieloośrodkowe, randomizowane badanie kliniczne III fazy w grupach równoległych w celu porównania tolerancji i „Skuteczności Terapia skojarzona Caelyx + bortezomib w porównaniu z bortezomibem w monoterapii Wystąpiła znacząca poprawa w zakresie pierwszorzędowego punktu końcowego, czasu do progresji (TTP), u pacjentów leczonych preparatem Caelyx + bortezomib w porównaniu z pacjentami leczonymi samym bortezomibem, na co wskazuje zmniejszenie ryzyka (RR ) 35% (95% CI; 21-47%), p
05.2 Właściwości farmakokinetyczne
Caelyx to długo krążąca, pegylowana liposomalna postać chlorowodorku doksorubicyny. Pegylowane liposomy zawierają związane z powierzchnią segmenty hydrofilowego polimeru glikolu metoksypolietylenowego (MPEG). Te liniowe grupy rozciągają się od powierzchni liposomów tworząc powłokę ochronną, która zmniejsza interakcje między dwuwarstwową błoną lipidową a składnikami osocza. Dzięki temu liposomy Caelyx mogą krążyć we krwi przez dłuższy czas. Pegylowane liposomy są wystarczająco małe (średnia średnica około 100 nm), aby przejść w stanie nienaruszonym (przez wynaczynienie) przez naczynia włosowate z okienkami, które zaopatrują guzy. Dowody przenikania pegylowanych liposomów z naczyń krwionośnych oraz wnikania i akumulacji do guzów stwierdzono u myszy z rakiem okrężnicy C-26 oraz u myszy transgenicznych ze zmianami podobnymi do KS. Pegylowane liposomy charakteryzują się również niską przepuszczalnością matrycy lipidowej i wewnętrznym wodnym układem buforowym, który pomaga utrzymać kapsułkowany chlorowodorek doksorubicyny, podczas gdy liposom pozostaje w krążeniu.
Farmakokinetyka preparatu Caelyx w osoczu u ludzi różni się znacznie od tych opisywanych w literaturze dla standardowych preparatów chlorowodorku doksorubicyny.W najniższych dawkach (10 mg/m2 - 20 mg/m2) Caelyx charakteryzuje się farmakokinetyką liniową między 10 mg/m2 a 60 mg/m2 Caelyx charakteryzuje się nieliniową farmakokinetyką. Standardowy chlorowodorek doksorubicyny wykazuje znaczną dystrybucję tkankową (objętość dystrybucji od 700 do 1100 l/m2) i szybki klirens eliminacji (24 do 73 l/h/m2). Z kolei profil farmakokinetyczny preparatu Caelyx wskazuje, że produkt ten pozostaje głównie zamknięty w objętości osocza, a klirens doksorubicyny z krwi zależy od transportera liposomalnego.Dostępność doksorubicyny rozpoczyna się po wynaczynieniu liposomów i ich wejście do przedziału tkanek.
Dla dawek równoważnych stężenie preparatu Caelyx w osoczu i wartości AUC reprezentujące głównie chlorowodorek doksorubicyny w pegylowanych liposomach (zawierających 90% - 95% mierzonej doksorubicyny) są znacznie wyższe niż wartości uzyskiwane przy standardowych preparatach chlorowodorku doksorubicyny.
Preparatu Caelyx nie wolno stosować zamiennie z innymi postaciami chlorowodorku doksorubicyny.
Farmakokinetyka populacyjna
Farmakokinetykę preparatu Caelyx oceniano na 120 pacjentach w 10 różnych badaniach klinicznych z zastosowaniem populacyjnego podejścia farmakokinetycznego.Parakokinetykę preparatu Caelyx w zakresie dawek od 10 mg/m2 do 60 mg/m2 najlepiej opisuje dwukompartmentowy, nieliniowy model z danymi wejściowymi rzędu zerowego i eliminacją Michaelisa-Mentena. Średni klirens wewnętrzny preparatu Caelyx wynosił 0,030 l/h/m2 (zakres od 0,008 do 0,152 l/h/m2), a średnia centralna objętość dystrybucji wynosiła 1,93 l/m2 (zakres 0,96 do 3,85 l/m2) w przybliżeniu dla objętości osocza. Pozorny okres półtrwania wynosił od 24 do 231 godzin, ze średnią 73,9 godzin.
Pacjentki z rakiem piersi
Farmakokinetyka preparatu Caelyx oznaczona u 18 pacjentek z rakiem piersi była podobna do farmakokinetyki określonej w większej populacji 120 pacjentek z różnymi nowotworami. Średni klirens wewnętrzny wynosił 0,016 l/h/m2 (zakres 0,008-0,027 l/h/m2), średnia objętość dystrybucji wynosiła 1,46 l/m2 (zakres 1,10-1,64 l/m2). Średni pozorny okres półtrwania wynosił 71,5 godziny (zakres 45,2-98,5 godziny).
Pacjenci z rakiem jajnika
Farmakokinetyka preparatu Caelyx oceniana u 11 pacjentek z rakiem jajnika była podobna do tej określonej w większej populacji 120 pacjentek z różnymi nowotworami. Średni klirens wewnętrzny wynosił 0,021 l/h/m2 (zakres od 0,009 do 0,041 l/h/m2), a średnia centralna objętość dystrybucji wynosiła 1,95 l/m2 (zakres 1,67 do 2, 40 l/m2). Średni pozorny okres półtrwania wynosił 75,0 godzin (zakres 36,1 do 125 godzin).
Pacjenci z KS-AIDS
Farmakokinetykę preparatu Caelyx w osoczu oceniano u 23 pacjentów z KS, którym podawano pojedyncze dawki 20 mg/m2 we wlewie trwającym 30 minut. Parametry farmakokinetyczne preparatu Caelyx (przedstawiające głównie chlorowodorek doksorubicyny w pegylowanych liposomach i niski poziom niekapsułkowanego chlorowodorku doksorubicyny) zmierzono po podaniu 20 mg/m2 i przedstawiono w Tabeli 8.
Tabela 8. Parametry farmakokinetyczne u pacjentów z AIDS-KS leczonych preparatem Caelyx
* Mierzone pod koniec 30-minutowej infuzji
05.3 Przedkliniczne dane o bezpieczeństwie
Profil toksykologiczny preparatu Caelyx w badaniach wielokrotnego podawania na zwierzętach jest bardzo podobny do obserwowanego w przypadku długotrwałych wlewów standardowego chlorowodorku doksorubicyny u ludzi.W przypadku preparatu Caelyx kapsułkowanie chlorowodorku doksorubicyny w pegylowanych liposomach daje następujące efekty: różna intensywność.
Kardiotoksyczność : Badania przeprowadzone na królikach wykazały, że kardiotoksyczność preparatu Caelyx jest zmniejszona w porównaniu z wywoływaną przez konwencjonalne preparaty chlorowodorku doksorubicyny.
Toksyczność skórna : W badaniach przeprowadzonych z wielokrotnym podawaniem preparatu Caelyx szczurom i psom po klinicznie istotnych dawkach obserwowano ciężkie zapalenie skóry właściwej i powstawanie owrzodzeń. W badaniu na psach częstość i nasilenie tych zmian zmniejszono poprzez zmniejszenie dawki lub wydłużenie odstępów między dawkami.Podobne zmiany skórne, określane jako erytrodyzestezja dłoniowo-podeszwowa, obserwowano również u pacjentów po długotrwałym wlewie dożylnym ( patrz punkt 4.8).
Odpowiedź rzekomoanafilaktyczna : Po podaniu pegylowanych liposomów (placebo) w badaniach toksykologicznych u psów obserwowano ostrą odpowiedź charakteryzującą się niedociśnieniem, bladością błon śluzowych, ślinotok, wymiotami i okresami nadpobudliwości, po których następowała niedoczynność i letarg. Podobną, ale mniej ciężką odpowiedź zaobserwowano u psów leczonych preparatem Caelyx i standardową doksorubicyną.
Intensywność odpowiedzi hipotensyjnej była zmniejszona w przypadku wstępnego leczenia opartego na lekach przeciwhistaminowych. Jednak odpowiedź nie zagroziła psom, które szybko wyzdrowiały po zaprzestaniu leczenia.
Toksyczność lokalna : Badania tolerancji podskórnej pokazują, że Caelyx, w porównaniu ze standardowym chlorowodorkiem doksorubicyny, powoduje miejscowe podrażnienie lub łagodniejsze uszkodzenie tkanek po możliwym wynaczynieniu.
Mutagenność i rakotwórczość : chociaż nie przeprowadzono żadnych badań w tym zakresie, chlorowodorek doksorubicyny, farmakologicznie czynny składnik preparatu Caelyx, jest mutagenny i rakotwórczy. Pegylowane liposomy placebo nie są ani mutagenne, ani genotoksyczne.
Toksyczność reprodukcyjna : Caelyx powoduje łagodny do umiarkowanego zanik jajników i jąder po podaniu pojedynczej dawki 36 mg/kg u myszy. U szczurów leczonych wielokrotnymi dawkami ≥ 0,25 mg/kg mc./dobę oraz u psów obserwowano zmniejszenie masy jąder i hipospermię, rozległe zwyrodnienie kanalików nasiennych i znaczny spadek spermatogenezy (patrz punkt 4.6).
Nefrotoksyczność : Badanie wykazało, że „pojedyncze dożylne podanie preparatu Caelyx w ilości ponad dwukrotnie większej niż dawka kliniczna powoduje toksyczność nerkową u małp. Toksyczność nerkową zaobserwowano nawet przy pojedynczych niższych dawkach chlorowodorku doksorubicyny u szczurów i królików. Od czasu oceny. dane dotyczące bezpieczeństwa po wprowadzeniu preparatu Caelyx do obrotu nie sugerowały znaczącej tendencji preparatu Caelyx pod względem nefrotoksyczności, dane obserwowane u małp mogą nie mieć znaczenia dla oceny ryzyka dla pacjenta.
06.0 INFORMACJE FARMACEUTYCZNE
06.1 Zaróbki
?- (2-[1,2-distearoilo-sn-glicerofosfoksy]etylokarbamoilo) -a - metoksypoli(oksyetyleno)-40 sól sodowa (MPEG-DSPE)
całkowicie uwodorniona fosfatydylocholina sojowa (HSPC)
cholesterol
siarczan amonu
sacharoza
histydyna
woda do wstrzykiwań
kwas chlorowodorowy
wodorotlenek sodu
06.2 Niekompatybilność
Tego produktu leczniczego nie wolno mieszać z innymi produktami oprócz wymienionych w punkcie 6.6.
06.3 Okres ważności
20 miesięcy
Po rozcieńczeniu:
- Wykazano chemiczną i fizyczną stabilność użytkową przez 24 godziny w temperaturach od 2°C do 8°C.
- Z mikrobiologicznego punktu widzenia produkt należy zużyć natychmiast. Jeśli rozcieńczony roztwór nie zostanie natychmiast zużyty, odpowiedzialność spoczywa na użytkowniku i nie powinien przekraczać 24 godzin w przypadku przechowywania w temperaturze od 2°C do 8°C.
- Częściowo zużyte fiolki należy wyrzucić.
06.4 Specjalne środki ostrożności przy przechowywaniu
Przechowywać w lodówce (2°C-8°C). Nie zamrażać.
Warunki przechowywania rozcieńczonego produktu leczniczego, patrz punkt 6.3.
06.5 Rodzaj opakowania bezpośredniego i zawartość opakowania
Fiolka ze szkła typu I z silikonowanym szarym korkiem z bromobutylu i aluminiowym uszczelnieniem, zawierająca objętość pozwalającą na dostarczenie 10 ml (20 mg) lub 25 ml (50 mg).
Caelyx jest dostarczany w pojedynczych opakowaniach lub opakowaniach po dziesięć fiolek.
Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
06.6 Instrukcje użytkowania i obsługi
Nie używać produktu, jeśli obecne są osady lub inne rodzaje cząstek.
Z roztworem Caelyx należy obchodzić się ostrożnie. Wymagane jest użycie rękawic. Jeśli Caelyx wejdzie w kontakt ze skórą lub błonami śluzowymi, należy natychmiast dokładnie przemyć wodą z mydłem. Z preparatem Caelyx należy obchodzić się i usuwać go zgodnie z normalnymi środkami ostrożności stosowanymi w przypadku innych leków przeciwnowotworowych, zgodnie z lokalnymi przepisami.
Określ dawkę preparatu Caelyx do podania (w zależności od zalecanej dawki i powierzchni ciała pacjenta). Pobrać odpowiednią objętość preparatu Caelyx za pomocą sterylnej strzykawki. Konieczna jest praca w ściśle aseptycznych warunkach, ponieważ Caelyx nie zawiera konserwantów ani środków bakteriostatycznych. Przed podaniem właściwą dawkę preparatu Caelyx należy rozcieńczyć w 5% roztworze glukozy (50 mg/ml) do infuzji dożylnej. Do dawek
Stosowanie do infuzji dożylnych innych niż 5% roztworu glukozy (50 mg/ml) rozcieńczalników lub obecność jakiegokolwiek środka bakteriostatycznego, takiego jak alkohol benzylowy, może powodować precypitację preparatu Caelyx.
Zaleca się podłączenie linii infuzyjnej zawierającej preparat Caelyx do bocznego wlotu wlewu 5% glukozy (50 mg/ml). Infuzję można podawać do żyły obwodowej Nie stosować z filtrami wbudowanymi.
07.0 PODMIOT POZWOLENIA NA DOPUSZCZENIE DO OBROTU
Janssen Cilag International NV
Turnhoutseweg 30
B-2340 Piwo
Belgia
08.0 NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
UE / 1/96/011/001
033308014
UE / 1/96/011/002
033308026
UE / 1/96/011/003
033308038
UE / 1/96/011/004
033308040
09.0 DATA PIERWSZEGO ZEZWOLENIA LUB PRZEDŁUŻENIA ZEZWOLENIA
Data pierwszego zezwolenia: 21 czerwca 1996 r.
Data ostatniego przedłużenia: 19 maja 2006 r.
10.0 DATA ZMIAN TEKSTU
Listopad 2010