Co to jest Zontivity i w jakim celu się go stosuje - worapaksar?
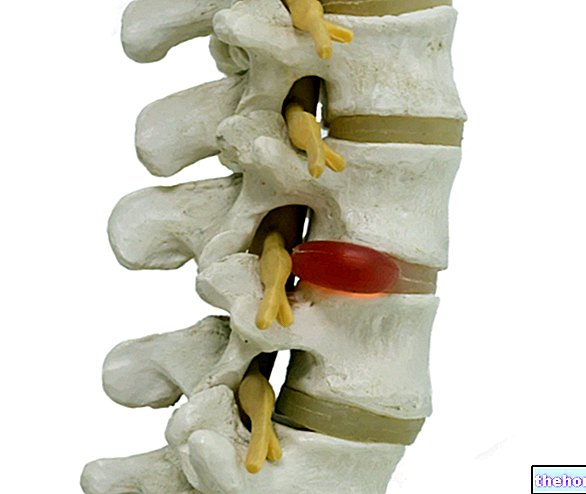
Zontivity jest lekiem stosowanym w celu zmniejszenia występowania zdarzeń miażdżycowych (problemy spowodowane zakrzepami krwi i pogrubieniem tętnic), w tym nowych zawałów mięśnia sercowego lub udaru mózgu u dorosłych pacjentów po przebytym zawale mięśnia sercowego. Zontivity zawiera substancję czynną worapaksar.
Jak stosuje się Zontivity - worapaksar?
Zontivity jest dostępny w postaci tabletek (2 mg) i jest dostępny wyłącznie na receptę. Zalecana dawka to jedna tabletka raz dziennie. Leczenie produktem Zontivity należy rozpocząć co najmniej 2 tygodnie po zawale mięśnia sercowego, najlepiej w ciągu pierwszych 12 miesięcy po zdarzeniu Dane dotyczące stosowania produktu Zontivity przez okres dłuższy niż 2 lata są ograniczone; dlatego po 2 latach leczenia lekarz prowadzący powinien ponownie ocenić korzyści i ryzyko związane ze stosowaniem produktu Zontivity u poszczególnych pacjentów.
Jak działa Zontivity - vorapaxar?
Substancja czynna leku Zontivity, worapaksar, jest inhibitorem agregacji płytek krwi, co oznacza, że pomaga zapobiegać tworzeniu się zakrzepów krwi, skrzepy krwi, gdy pewne komórki krwi, zwane płytkami krwi, sklejają się ze sobą, worapaksar je blokuje, receptory PAR-1 (znane jako „receptory trombiny”) obecne na powierzchni płytek krwi. Trombina jest jedną z substancji biorących udział w procesie krzepnięcia: wiążąc się z receptorem PAR-1, powoduje „lepkość” płytek krwi, a tym samym , promuje tworzenie skrzepów. Blokując receptor PAR-1, lek zapobiega lepkości płytek krwi, zmniejszając ryzyko powstawania skrzepów i pomagając zapobiegać udarowi lub nowemu zawałowi mięśnia sercowego.
Jakie korzyści wykazał Zontivity - worapaksar podczas badań?
Lek Zontivity porównywano z placebo (leczenie pozorowane) w jednym badaniu głównym z udziałem ponad 26 000 osób dorosłych z zawałem mięśnia sercowego lub innymi zdarzeniami zakrzepowymi w przebiegu miażdżycy. leczonych przez co najmniej rok.Główną miarą skuteczności była liczba pacjentów, którzy zgłosili „zdarzenie”, w tym nowy zawał mięśnia sercowego lub udar, lub którzy zmarli z powodu choroby sercowo-naczyniowej (problemy dotyczące serca i naczyń krwionośnych). Zontivity był skuteczniejszy niż placebo w zmniejszaniu częstości występowania incydentów zakrzepowych w miażdżycy.Ogólnie incydenty zakrzepowe w miażdżycy obserwowano u 9,5% pacjentów (1 259 z 13 225 pacjentów), którzy przyjmowali Zontivity, w porównaniu do 10,7% (1 417 z 13 224). pacjentów) pacjentów leczonych placebo. W tej grupie incydent miażdżycowy zaobserwowano u „8,5% pacjentów (719 z 8 458 pacjentów), którzy przyjmowali lek Zontivity w porównaniu z 10,3% (867 z 8 439 pacjentów) pacjentów otrzymujących placebo.
Jakie jest ryzyko związane ze stosowaniem leku Zontivity - worapaksar?
Najczęstszym działaniem niepożądanym związanym ze stosowaniem leku Zontivity (które może dotyczyć nie więcej niż 1 na 10 osób) jest krwawienie, zwłaszcza krwawienie z nosa (krwawienie z nosa).Pełny wykaz działań niepożądanych zgłaszanych podczas stosowania leku Zontivity znajduje się w ulotce dla pacjenta. Leku Zontivity nie należy stosować u pacjentów po udarze lub minizawale serca. Nie wolno go również stosować u pacjentów, u których wystąpił „krwotok śródczaszkowy (krwotok mózgowy) lub z czynnym krwawieniem, ani u pacjentów z ciężkimi zaburzeniami czynności wątroby. Zontivity nie może być stosowany w skojarzeniu z prasugrelem lub tikagrelorem, dwoma innymi lekami, które przyczyniają się do zapobiegać agregacji płytek krwi. Pełna lista ograniczeń znajduje się w ulotce dołączonej do opakowania.
Dlaczego Zontivity - vorapaxar został zatwierdzony?
Komitet ds. Produktów Leczniczych Stosowanych u Ludzi (CHMP) Agencji uznał, że korzyści płynące ze stosowania leku Zontivity przewyższają ryzyko, i zalecił jego dopuszczenie do stosowania w UE. Jeśli chodzi o profil bezpieczeństwa produktu Zontivity, CHMP wyraził obawy dotyczące ryzyka krwotoku u pacjentów przyjmujących Zontivity jako dodatek do standardowego leczenia, w szczególności ryzyko ciężkiego krwotoku, który występuje częściej u pacjentów z udarem mózgu w wywiadzie .
Dlatego uznał za właściwe ograniczenie jego stosowania do pacjentów, którzy nigdy wcześniej nie mieli udaru.
Jakie środki podejmuje się w celu zapewnienia bezpiecznego i skutecznego stosowania leku Zontivity - vorapaxar?
Opracowano plan zarządzania ryzykiem, aby zapewnić, że Zontivity jest używane tak bezpiecznie, jak to możliwe. W oparciu o ten plan do charakterystyki produktu leczniczego i ulotki dołączonej do opakowania produktu Zontivity dodano informacje dotyczące bezpieczeństwa, w tym odpowiednie środki ostrożności, których powinni przestrzegać pracownicy służby zdrowia i pacjenci. Więcej informacji można znaleźć w podsumowaniu planu zarządzania ryzykiem.
Więcej informacji o Zontivity - vorapaxar
W dniu 19 stycznia 2015 r. Komisja Europejska wydała „Zezwolenie na dopuszczenie do obrotu” dla Zontivity, ważne w całej Unii Europejskiej.Pełną wersję EPAR i podsumowanie Planu Zarządzania Ryzykiem Zontivity można znaleźć na stronie internetowej Agencji: ema.Europa. eu/Find medicine / Human drugs / Europejskie publiczne sprawozdania oceniające W celu uzyskania dodatkowych informacji na temat terapii preparatem Zontivity należy zapoznać się z ulotką dla pacjenta (dołączoną do EPAR) bądź skontaktować się z lekarzem lub farmaceutą. Ostatnia aktualizacja niniejszego podsumowania: 01-2015.
Informacje o Zontivity - vorapaxar opublikowane na tej stronie mogą być nieaktualne lub niekompletne. Aby prawidłowo wykorzystać te informacje, zobacz stronę Wyłączenie odpowiedzialności i przydatne informacje.