Składniki aktywne: Amiodaron (chlorowodorek amiodaronu)
Amiodar 200 mg tabletki
Dlaczego stosuje się Amiodar? Po co to jest?
Amiodar zawiera aktywny składnik amiodaron. Amiodar jest lekiem antyarytmicznym, czyli stosowanym w leczeniu i profilaktyce zaburzeń rytmu serca, takich jak:
- szybkie bicie serca (napadowe i nienapadowe częstoskurcze nadkomorowe) lub nieregularne (dodatkowe skurcze przedsionków, trzepotanie i migotanie przedsionków, dodatkowe skurcze komorowe i częstoskurcze)
- szybkie bicie serca, czasami występujące jako napadowy częstoskurcz nawrotny, taki jak w chorobie zwanej zespołem Wolffa-Parkinsona-White'a.
Amiodar można stosować w leczeniu nieregularnego bicia serca, gdy inne leki nie działają lub nie mogą być stosowane.
Amiodar stosuje się również w profilaktyce kryzysów dusznicy bolesnej (bóle w klatce piersiowej spowodowane problemami związanymi z chorobami serca).
Przeciwwskazania Kiedy nie należy stosować Amiodaru
Nie bierz Amiodaru
- jeśli pacjent ma uczulenie na amiodaron, jod lub którykolwiek z pozostałych składników tego leku
- jeśli masz zaburzenia rytmu serca, takie jak:
- wolne tętno (bradykardia zatokowa) lub choroba zwana „blokem zatokowo-przedsionkowym”
- jeśli u pacjenta występują inne zaburzenia rytmu serca i nie wszczepiono rozrusznika serca (np. ciężki blok przedsionkowo-komorowy, blok dwu- lub trójpowięziowy)
- jeśli masz chorobę zwaną „choroba zatok” i nie masz wszczepionego rozrusznika;
- jeśli pacjent przyjmuje leki, które mogą powodować zaburzenia pracy serca zwane „torsade de pointes” (częstoskurcz komorowy typu „torsade de pointes”, przyspieszone bicie serca) (patrz punkt „Amiodar a inne leki”).
- jeśli masz lub miałeś problemy z tarczycą. W przypadku wątpliwości lub problemów z tarczycą w rodzinie wskazane jest wykonanie badania czynności tarczycy przed leczeniem
- jeśli pacjentka jest w ciąży lub podejrzewa, że jest w ciąży, z wyjątkiem wyjątkowych przypadków (patrz punkt „Ciąża i karmienie piersią”)
- jeśli pacjentka karmi piersią (patrz punkt „Ciąża i karmienie piersią”).
Środki ostrożności dotyczące stosowania Informacje ważne przed zastosowaniem leku Amiodar
Przed rozpoczęciem przyjmowania leku Amiodar należy omówić to z lekarzem lub farmaceutą.
Unikaj ekspozycji na słońce i stosuj środki ochronne podczas przyjmowania Amiodaru.
Lekarz może zlecić wykonanie elektrokardiogramu (EKG) i (lub) badań krwi przed rozpoczęciem i podczas leczenia lekiem Amiodar.
Ogólne znieczulenie
W przypadku konieczności poddania się zabiegowi chirurgicznemu w znieczuleniu ogólnym, należy poinformować anestezjologa o przyjmowaniu leku Amiodar, ponieważ po znieczuleniu zaobserwowano przypadki problemów z sercem lub płucami, czasem śmiertelnych.
Zaburzenia tarczycy
Amiodaron może powodować problemy z tarczycą. Należy zachować szczególną ostrożność, jeśli pacjent miał problemy z tarczycą w przeszłości lub jest osobą w podeszłym wieku.
Porozmawiaj z lekarzem, jeśli zauważysz jakiekolwiek objawy, nawet łagodne, wymienione poniżej, które mogą wystąpić do kilku miesięcy po zaprzestaniu leczenia:
- przyrost lub utrata masy ciała
- nietolerancja zimna
- zmniejszona aktywność
- wolne bicie serca
- zaburzenia rytmu serca
- bóle w klatce piersiowej
- obrzęk z zatrzymaniem wody lub innymi problemami z sercem.
Lekarz zdecyduje, czy przerwać leczenie lekiem Amiodar, czy ewentualnie zastosować odpowiednią terapię.
Zaburzenia wątroby
Nie należy stosować leku Amiodar w przypadku trwającej choroby wątroby.
Podczas leczenia amiodaronem mogą wystąpić ostre (w tym ciężkie, czasami śmiertelne) i przewlekłe zmiany w wątrobie, powiększenie wątroby lub zaburzenia żółci lub pęcherzyka żółciowego.
We wszystkich tych przypadkach lekarz poinformuje pacjenta, czy należy przerwać stosowanie leku, czy go zmniejszyć.
Problemy z płucami
Amiodaron może powodować toksyczne działanie na płuca.W przypadku chorób serca (kardiomiopatii i ciężkiej choroby niedokrwiennej serca) istnieje szczególne ryzyko.
Porozmawiaj z lekarzem, jeśli zauważysz wymienione poniżej objawy, które mogą wystąpić kilka tygodni po zaprzestaniu leczenia:
- zapalenie pęcherzyków płucnych, zapalenie płuc (zapalenie płuc) i inne problemy z płucami (śródmiąższowe zapalenie płuc, zwłóknienie płuc)
- trudności w oddychaniu z powodu zwężenia oskrzeli (astma oskrzelowa)
- suchy kaszel
- trudności w oddychaniu (duszność)
- gorączka
- zmęczenie
- utrata wagi
Lekarz może przepisać prześwietlenie klatki piersiowej, odpowiednią terapię i (lub) przerwanie leczenia Amiodarem.
Dolegliwości serca
Działanie amiodaronu powoduje widoczne zmiany w zapisie elektrokardiogramu (EKG), których nie należy traktować jako objawów toksyczności.
Jeśli jesteś starszym pacjentem, spowolnienie akcji serca może być bardziej wyraźne.
Jeśli u pacjenta wystąpią poważne problemy z sercem, nowe arytmie lub nasilenie wcześniej leczonych arytmii, lekarz rozważy przerwanie leczenia lekiem Amiodar.
Rozrusznik serca
Jeśli masz rozrusznik serca, lekarz będzie wielokrotnie sprawdzał działanie urządzenia przed iw trakcie terapii Amiodarem.
Zaburzenia nerwów i mięśni
Amiodaron może powodować uszkodzenie nerwów i mięśni. Gojenie może potrwać kilka miesięcy po odstawieniu leku Amiodar, a czasami może być niepełne.
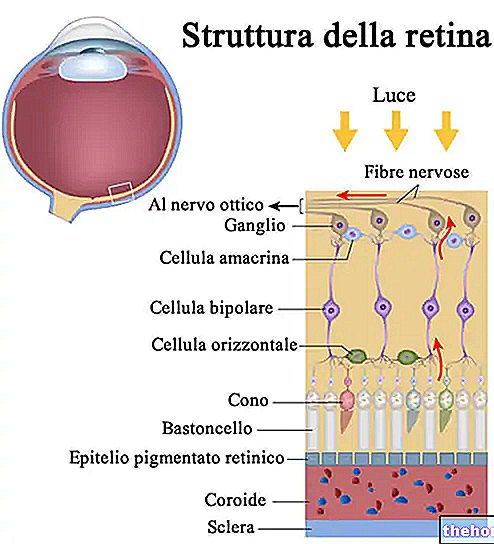
Zaburzenia oka
Jeśli zauważysz niewyraźne widzenie lub pogorszenie widzenia, natychmiast powiadom swojego lekarza, który natychmiast wykona pełne badanie wzroku.
W przypadku uszkodzenia nerwu wzrokowego lekarz zaleci przerwanie stosowania leku Amiodar, aby uniknąć utraty wzroku.
Dzieci i młodzież
Bezpieczeństwo i skuteczność amiodaronu u dzieci i młodzieży nie zostały ustalone i nie zaleca się stosowania amiodaronu u tych pacjentów.
Interakcje Jakie leki lub pokarmy mogą modyfikować działanie Amiodaru®
Należy powiedzieć lekarzowi lub farmaceucie, jeśli pacjent przyjmuje, ostatnio stosował lub może stosować jakiekolwiek inne leki.
Nie należy stosować leku Amiodar razem z następującymi lekami, ponieważ mogą wystąpić działania niepożądane, w tym potencjalnie śmiertelne:
- leki przeciwarytmiczne (leki stosowane w leczeniu zaburzeń rytmu serca), np. sotalol, bepridil
- Winkamina (lek stosowany w niedokrwieniu mózgu)
- Niektóre leki psychiatryczne, w tym sultopryd
- Cyzapryd (lek stosowany w dolegliwościach żołądkowych)
- Dożylna erytromycyna lub pentamidyna (do podawania nie doustnego) (antybiotyki)
- Fluorochinolony (antybiotyki)
- Leki na depresję (inhibitory monoaminooksydazy)
- Leki na nadciśnienie (beta-blokery i blokery kanału wapniowego)
- Werapamil, diltiazem (leki zmniejszające częstość akcji serca), ponieważ mogą powodować spowolnienie akcji serca (bradykardia)
- Stymulujące środki przeczyszczające, ponieważ mogą obniżać poziom potasu we krwi
Należy poinformować lekarza, jeśli pacjent stosuje jeden lub więcej leków wymienionych poniżej, ponieważ będzie on monitorował stan pacjenta podczas leczenia lekiem Amiodar:
- leki stymulujące produkcję moczu (leki moczopędne, stosowane w celu zmniejszenia obrzęku spowodowanego gromadzeniem się płynów i obniżenia wysokiego ciśnienia krwi), stosowane pojedynczo lub w skojarzeniu
- leki glikokortykosteroidowe i mineralokortykoidowe (kortyzon) doustnie lub we wstrzyknięciach
- tetrakozaktyd (hormon)
- amfoterycyna B (lek przeciw zakażeniom grzybiczym) dożylnie.
- Digitalis (lek nasercowy)
- Leki zmniejszające krzepliwość krwi np. dabigatran, warfaryna
- Fenytoina (lek przeciwpadaczkowy)
- Flekainid (lek na zaburzenia rytmu serca)
- Statyny (leki obniżające poziom cholesterolu)
- Cyklosporyna (immunosupresyjna)
- Fentanyl (lek przeciwbólowy)
- Lidokaina (znieczulenie miejscowe)
- Takrolimus (środek immunosupresyjny)
- Sildenafil (lek na zaburzenia erekcji)
- Midazolam i triazolam (środki uspokajające)
- Kolchicyna (lek na dnę moczanową)
- Dihydroergotamina, ergotamina (leki przeciw zaburzeniom krążenia)
Interakcje między Amiodarem a innymi lekami można obserwować przez kilka miesięcy po zaprzestaniu leczenia.
W razie wątpliwości należy zwrócić się do lekarza lub farmaceuty.
Amiodar z jedzeniem i piciem
Działanie i toksyczność Amiodaru mogą być nasilone w przypadku jednoczesnego spożycia owoców lub soku grejpfrutowego.
Ostrzeżenia Ważne jest, aby wiedzieć, że:
Ciąża i karmienie piersią
Jeśli pacjentka jest w ciąży lub karmi piersią, podejrzewa, że może być w ciąży lub planuje mieć dziecko, powinna poradzić się lekarza lub farmaceuty przed zastosowaniem tego leku.
Amiodaru nie należy stosować w okresie ciąży, chyba że korzyści dla matki przewyższają ryzyko dla płodu ze względu na jego wpływ na tarczycę płodu.
Amiodaru nie należy stosować u matek karmiących piersią, ponieważ przenika do mleka matki.
Prowadzenie i używanie maszyn
Na podstawie danych dotyczących bezpieczeństwa amiodaronu nie wykazano wpływu na zdolność prowadzenia pojazdów i obsługiwania maszyn.
Amiodar zawiera laktozę (cukier mleczny)
Tabletki Amiodar zawierają laktozę: jeśli lekarz poinformował pacjenta o nietolerancji niektórych cukrów, przed przyjęciem tego leku należy skontaktować się z lekarzem.
Dawkowanie i sposób użycia Jak stosować Amiodar: Dawkowanie
Lek należy zawsze stosować zgodnie z zaleceniami lekarza. W razie wątpliwości skonsultuj się z lekarzem lub farmaceutą.
Amiodaron ma bardzo zróżnicowane działanie w zależności od osoby, z tego powodu lekarz oceni drogę podania, dawkę początkową i dawkę podtrzymującą w oparciu o ciężkość choroby i jej odpowiedź.
Leczenie zaburzeń rytmu
Zalecana dawka wynosi 600 mg (3 tabletki po 200 mg) na dobę, aż do uzyskania dobrej odpowiedzi na leczenie, średnio w ciągu dwóch tygodni.
Następnie lekarz może stopniowo zmniejszać dawkę, aż do ustalenia dawki podtrzymującej, która zwykle wynosi od 100 do 400 mg (od pół tabletki do 2 tabletek) na dobę.
Gdy ustalenie zadowalającej dziennej dawki podtrzymującej jest trudne, lekarz może przepisać leczenie przerywane (5 dni w tygodniu lub 2/3 tygodnie w miesiącu).
Profilaktyczne leczenie kryzysów dławicowych
Terapia ataku: Zalecana dawka to 600 mg (3 tabletki po 200 mg) dziennie przez około 7 dni.
Leczenie podtrzymujące: zalecana dawka to 100-400 mg (między pół tabletki a 2 tabletki) na dobę lub z przerwami (5 dni w tygodniu lub 2/3 tygodnie w miesiącu).
Stosowanie u dzieci i młodzieży
Bezpieczeństwo i skuteczność amiodaronu u dzieci i młodzieży nie zostały ustalone i nie zaleca się stosowania amiodaronu u tych pacjentów.
Pominięcie przyjęcia leku Amiodar
Nie należy stosować dawki podwójnej w celu uzupełnienia pominiętej dawki.
Przerwanie stosowania leku Amiodar
W przypadku dalszych pytań dotyczących stosowania tego leku należy zwrócić się do lekarza lub farmaceuty.
Przedawkowanie Co zrobić w przypadku przyjęcia zbyt dużej dawki leku Amiodar
W przypadku zażycia zbyt dużej dawki leku Amiodar należy natychmiast powiedzieć o tym lekarzowi lub udać się do najbliższego szpitala.
W przypadku dalszych pytań dotyczących stosowania leku Amiodar należy zwrócić się do lekarza lub farmaceuty.
Niewiele jest dostępnych informacji na temat nadmiernej dawki amiodaronu.
Było kilka doniesień o bradykardii zatokowej (powolne bicie serca), zatrzymaniu akcji serca, częstoskurczu komorowym (szybkie bicie serca), „torsade de pointes” (zaburzenia aktywności elektrycznej serca), problemach z krążeniem krwi i uszkodzeniu wątroby.
Skutki uboczne Jakie są skutki uboczne Amiodaru
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią, a ich nasilenie może być różne.
Najczęściej obserwowane działania niepożądane nie uzasadniają przerwania leczenia.
Zgłaszano jednak poważne działania niepożądane, szczególnie dotyczące płuc lub wątroby.
W każdym przypadku lekarz zdecyduje, czy zmniejszyć dawkę, czy przerwać leczenie, zarówno w zależności od potencjalnego nasilenia działania niepożądanego, jak i nasilenia choroby.
Bardzo częste działania niepożądane (mogą wystąpić u więcej niż 1 na 10 osób)
- Mikrodepozyty w rogówce, zwykle ograniczone do obszaru pod źrenicą, mogą im towarzyszyć kolorowe aureole w oślepiającym świetle lub niewyraźne widzenie
- Pojawienie się plam lub zaczerwienienia na skórze po ekspozycji na światło słoneczne lub lampy słoneczne
- Zwiększony poziom transaminaz we krwi (wskazujący na uszkodzenie wątroby)
- Nudności wymioty
- Zmiany w smaku
Częste działania niepożądane (mogą dotyczyć do 1 na 10 osób)
- Wolne tętno (bradykardia)
- Swędząca, czerwonawa wysypka (egzema). Nieprawidłowe łupkowo-szare lub niebieskawe zabarwienie skóry
- Słaba czynność tarczycy
- Nadczynność tarczycy czasami śmiertelna
- Ostre uszkodzenie wątroby, z podwyższonym poziomem transaminaz we krwi i/lub zażółceniem skóry, błon śluzowych i oczu (żółtaczka), któremu czasami towarzyszy śmiertelna niewydolność wątroby
- Toksyczność płucna (np. pęcherzykowe/śródmiąższowe zapalenie płuc lub zwłóknienie, zapalenie opłucnej, zarostowe zapalenie oskrzelików ze zorganizowanym zapaleniem płuc), czasami śmiertelne
- Drżenie
- Koszmary
- Zaburzenia snu
- Zaparcie
Niezbyt częste działania niepożądane (mogą wystąpić u 1 na 100 osób)
- Zaburzenia czynności elektrycznej serca (zaburzenia przewodzenia, blok zatokowo-przedsionkowy, blok przedsionkowo-komorowy różnego stopnia)
- Początek lub pogorszenie zaburzeń rytmu, po których czasami następuje niewydolność serca
- Uszkodzenie nerwów i mięśni odwracalne po odstawieniu leku
- Suchość w ustach
Bardzo rzadkie działania niepożądane (mogą wystąpić u 1 na 10 000 osób)
- Zmniejszenie liczby czerwonych krwinek przed zniszczeniem (niedokrwistość hemolityczna)
- Zmniejszenie liczby czerwonych krwinek z nieprodukcyjnych (niedokrwistość aplastyczna)
- Mała liczba płytek krwi (małopłytkowość)
- Powolne bicie serca (znaczna bradykardia) lub zatrzymanie zatok
- Zapalenie i (lub) uszkodzenie nerwu wzrokowego (neuropatia/zapalenie nerwu wzrokowego), które może prowadzić do ślepoty
- Zaczerwienienie skóry podczas radioterapii
- Wysypki na skórze
- Zapalenie z łuszczeniem się skóry (złuszczające zapalenie skóry)
- Wypadanie włosów i włosów
- Zespół nieprawidłowego wydzielania hormonu antydiuretycznego (SIADH), choroba spowodowana nadmiarem hormonu ADH (adiuretyny) we krwi
- Przewlekłe uszkodzenie wątroby (pseudoalkoholowe zapalenie wątroby, marskość) czasami śmiertelne
- Skurcz oskrzeli (reakcja astmatyczna)
- Ciężkie reakcje płucne (ADRS, zespół ostrej niewydolności oddechowej dorosłych), czasami śmiertelne
- Zwiększona kreatynina we krwi
- Utrata koordynacji ruchów
- Wysokie ciśnienie krwi wewnątrz łagodnej czaszki (guz rzekomy mózgu)
- Bół głowy
- Zapalenie najądrza (zapalenie najądrza), struktury nad jądrem
- Impotencja
- Zapalenie naczyń (żył i tętnic)
Działania niepożądane o nieznanej częstości (częstość nie może być określona na podstawie dostępnych danych)
- Zmiana zapalna (ziarniniak) szpiku kostnego
- Zmiana czynności elektrycznej serca (Torsade de pointes)
- Ciężkie reakcje alergiczne (reakcja anafilaktyczna, wstrząs anafilaktyczny)
- Nagłe zapalenie trzustki (ostre zapalenie trzustki)
- Ciężkie, zagrażające życiu reakcje skórne charakteryzujące się wysypką, pęcherzami skórnymi, łuszczeniem się skóry i bólem (toksyczne martwicze oddzielanie się naskórka (TEN), zespół Stevensa-Johnsona (SJS), pęcherzowe zapalenie skóry, reakcja polekowa z eozynofilią i objawami ogólnoustrojowymi (DRESS)).
- Zmniejszony apetyt
- Nieprawidłowe ruchy mięśni, sztywność, drżenie i niepokój (parkinsonizm); nieprawidłowa percepcja zapachów (parosmia)
- Zamieszanie (delirium)
- Pokrzywka
- Zmiana zapalna (ziarniniak) wątroby
- Krwawienie z płuc
- Obrzęk spowodowany gromadzeniem się płynów (obrzęk), zwłaszcza kończyn dolnych i twarzy (obrzęk naczynioruchowy)
Zgłaszanie skutków ubocznych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie możliwe działania niepożądane niewymienione w tej ulotce, należy porozmawiać z lekarzem lub farmaceutą. Działania niepożądane można również zgłaszać bezpośrednio za pośrednictwem krajowego systemu zgłaszania pod adresem www.agenziafarmaco.it/it/responsabili Zgłaszanie działań niepożądanych może pomóc w uzyskaniu dodatkowych informacji na temat bezpieczeństwa stosowania tego leku.
Wygaśnięcie i przechowywanie
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na pudełku po EXP.Termin ważności oznacza ostatni dzień podanego miesiąca.
Nie należy wyrzucać żadnych leków do kanalizacji ani domowych pojemników na odpadki. Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa.Pomoże to chronić środowisko.
Inne informacje
Co zawiera lek Amiodar
- Substancją czynną jest chlorowodorek amiodaronu. Każda tabletka zawiera 200 mg amiodaronu chlorowodorku.
- Pozostałe składniki to: laktoza jednowodna, skrobia kukurydziana, poliwidon, bezwodna krzemionka koloidalna, magnezu stearynian.
Opis wyglądu leku Amiodar i co zawiera opakowanie
Pudełko tekturowe zawierające 2 blistry po 10 tabletek każdy.
Ulotka pakietu źródłowego: AIFA (Włoska Agencja Leków). Treść opublikowana w styczniu 2016 r. Przedstawione informacje mogą być nieaktualne.
Aby mieć dostęp do najbardziej aktualnej wersji, warto wejść na stronę AIFA (Włoskiej Agencji Leków). Zastrzeżenie i przydatne informacje.
01.0 NAZWA PRODUKTU LECZNICZEGO
TABLETKI AMIODAR
02.0 SKŁAD JAKOŚCIOWY I ILOŚCIOWY
Jedna tabletka zawiera:
Aktywna zasada: 200 mg chlorowodorku amiodaronu.
Pełny wykaz substancji pomocniczych, patrz punkt 6.1
03.0 POSTAĆ FARMACEUTYCZNA
Podzielne tabletki.
04.0 INFORMACJE KLINICZNE
04.1 Wskazania terapeutyczne
Leczenie i profilaktyka ciężkich zaburzeń rytmu opornych na inne specyficzne terapie: częstoskurcze nadkomorowe (napadowe i nienapadowe), dodatkowe skurcze przedsionków, trzepotanie i migotanie przedsionków.
Napadowe częstoskurcze napadowe nadkomorowe jak w zespole Wolffa-Parkinsona-White'a. Dodatkowe skurcze komorowe i częstoskurcze.
Profilaktyczne leczenie kryzysów dusznicy bolesnej.
04.2 Dawkowanie i sposób podawania
Amiodaron ma szczególne właściwości farmakologiczne (50% wchłanianie doustne, rozległa dystrybucja tkankowa, powolna eliminacja, opóźniona odpowiedź terapeutyczna po podaniu doustnym), które są bardzo zróżnicowane w zależności od osoby, z tego powodu droga podania, dawka początkowa i podtrzymująca muszą być oceniane w każdym przypadku z osobna, dostosowanie ich do ciężkości choroby i odpowiedzi klinicznej.
Zalecane dawki to:
Leczenie zaburzeń rytmu:
Zalecana początkowa średnia dawka wynosi 600 mg na dobę, aż do uzyskania dobrej odpowiedzi terapeutycznej, średnio w ciągu dwóch tygodni. Następnie dawkę można stopniowo zmniejszać, aż dawka podtrzymująca zostanie zwykle ustalona na poziomie 100-400 mg na dobę.
Gdy trudno jest ustalić zadowalającą dzienną dawkę podtrzymującą, można zastosować terapię przerywaną (np. 2/3 tygodnie w miesiącu lub 5 dni w tygodniu).
Leczenie profilaktyczne kryzysów angorycznych:
• atak: 600 mg dziennie przez około 7 dni
• podtrzymanie: 100-400 mg dziennie lub z przerwami (5 dni w tygodniu lub 2/3 tygodnie w miesiącu).
Terapia skojarzona
Informacje dotyczące pacjentów przyjmujących amiodaron jednocześnie z inhibitorami reduktazy HMG-CoA (statynami), patrz punkty 4.4 i 4.5.
04.3 Przeciwwskazania
• Nadwrażliwość na substancję czynną, jod lub na którąkolwiek substancję pomocniczą.
• Bradykardia zatokowa; blok zatokowo-przedsionkowy; ciężkie zaburzenia przewodzenia, bez elektrostymulacji (ciężkie bloki przedsionkowo-komorowe, dwu- lub trójpęczkowe).
• Choroba zatok bez elektrostymulatora (ryzyko zatrzymania zatok).
• Połączenie z lekami mogącymi powodować „torsade de pointes” (patrz punkt 4.5).
• Dystyroidyzm lub poprzednicy tarczycy. W przypadkach wątpliwych (niepewne tło, wywiad rodzinny w kierunku tarczycy) przed leczeniem należy wykonać badanie czynnościowe tarczycy.
• Ciąża, z wyjątkiem wyjątkowych przypadków (patrz punkt 4.6).
• Karmienie piersią (patrz punkt 4.6)
04.4 Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania
Specjalne ostrzeżenia
Amiodaron może powodować objawy uboczne o różnej częstotliwości i nasileniu.
Najczęściej obserwowane objawy nie uzasadniają przerwania leczenia (patrz punkt 4.8). Zgłaszano jednak poważne skutki uboczne, szczególnie w przypadku urazów płuc lub przewlekłego zapalenia wątroby.
Toksyczność płucna
Toksyczność płucna związana z przyjmowaniem amiodaronu jest częstą i poważną reakcją niepożądaną, która może wystąpić nawet u 10% pacjentów i może być śmiertelna u około 8% dotkniętych nią pacjentów, głównie z powodu braku rozpoznania. Czas wystąpienia reakcji w trakcie leczenia waha się od kilku dni do kilku miesięcy lub lat przyjmowania, w niektórych przypadkach początek może nastąpić również po pewnym czasie od zawieszenia leczenia.
Ryzyko zatrucia nie powoduje jednak niekorzystnego stosunku ryzyka do korzyści amiodaronu, co pozwala zachować jego przydatność, jednak należy zwrócić szczególną uwagę na natychmiastowe rozpoznanie pierwszych objawów toksyczności płucnej, zwłaszcza u pacjentów z kardiomiopatią i ciężką chorobą wieńcową. choroba serca, w której taka identyfikacja może być bardziej problematyczna.
Ryzyko toksycznego działania amiodaronu na płuca wzrasta przy dawkach powyżej 400 mg/dobę, ale może również wystąpić przy niskich dawkach przyjmowanych przez mniej niż 2 lata.
Toksyczność płucna objawia się zapaleniem pęcherzyków płucnych, zapaleniem płuc, śródmiąższowym zapaleniem płuc, zwłóknieniem płuc, astmą oskrzelową.Pacjenci, u których rozwija się toksyczność płucna, często mają niespecyficzne objawy, takie jak kaszel bez odkrztuszania, duszność, gorączka i utrata masy ciała.
Wszystkie te objawy mogą być maskowane przez patologię, w której wskazany jest amiodaron i mogą być bardzo poważne u pacjentów w wieku powyżej 70 lat, którzy zwykle mają zmniejszoną wydolność funkcjonalną lub istniejące wcześniej choroby serca. Wczesna diagnoza za pomocą kontroli radiograficznej płuc i ewentualnie niezbędnych badań klinicznych i instrumentalnych ma kluczowe znaczenie, ponieważ toksyczność płucna jest wysoce odwracalna, zwłaszcza w postaci zarostowego zapalenia oskrzelików i zapalenia płuc. Objawy płucne i obiektywizm muszą być zatem okresowo sprawdzane, a leczenie należy wstrzymać w przypadku podejrzenia toksyczności płucnej, biorąc pod uwagę terapię kortyzonem: objawy zwykle ustępują w ciągu 2-4 tygodni od odstawienia amiodaronu.W niektórych przypadkach może ujawnić się toksyczność płucna późno, nawet kilka tygodni po zawieszeniu terapii: osoby z suboptymalnymi funkcjami organicznymi, które mogłyby eliminować lek wolniej, muszą być zatem uważnie obserwowane.
W każdym przypadku, zmniejszenie dawki lub zawieszenie leczenia będzie musiało być brane pod uwagę zarówno w zależności od potencjalnego nasilenia działania ubocznego, jak i nasilenia postępującej postaci sercowej.
Lek należy zatem stosować dopiero po dokładnej ocenie stanu pacjenta, aby ocenić, czy oczekiwane korzyści rekompensują hipotetyczne wady; ponadto pacjent musi być dokładnie monitorowany z klinicznego i laboratoryjnego punktu widzenia, aby móc wykryć niepożądane objawy przy pierwszych objawach i zastosować odpowiednie środki.
Zaburzenia serca (patrz punkt 4.8)
Farmakologiczne działanie amiodaronu powoduje zmiany elektrokardiograficzne: wydłużenie odstępu QT (związane z wydłużeniem repolaryzacji), z możliwym pojawieniem się załamków U. Nie są to jednak objawy toksyczności.
Spowolnienie częstości akcji serca może być bardziej wyraźne u pacjentów w podeszłym wieku.
Leczenie należy przerwać w przypadku wystąpienia bloku przedsionkowo-komorowego II lub III stopnia, bloku zatokowo-przedsionkowego lub bloku dwupęczkowego.
Istnieją doniesienia o nowych arytmiach lub pogorszeniu leczonych arytmii, czasami śmiertelnych. Odróżnienie utraty skuteczności leku od efektu proarytmicznego jest ważne, ale trudne, w każdym przypadku wiąże się to z pogorszeniem stanu serca. Działania proarytmiczne są zgłaszane rzadziej w przypadku amiodaronu niż w przypadku innych leków przeciwarytmicznych i zwykle występują w kontekście interakcji i (lub) zaburzeń elektrolitowych (patrz punkty 4.5 i 4.8).
W przypadku jednoczesnego przepisywania innych leków kardiologicznych należy upewnić się, że nie są znane interakcje (patrz punkt 4.5).
Ze względu na zmniejszone ujemne działanie inotropowe amiodaron można stosować doustnie w przypadku niewydolności serca.
Nadczynność tarczycy (patrz punkty 4.4 „Środki ostrożności dotyczące stosowania” i 4.8)
Może wystąpić w trakcie leczenia amiodaronem lub do kilku miesięcy po jego odstawieniu. Objawy kliniczne, zwykle łagodne, takie jak utrata masy ciała, wystąpienie arytmii, dusznica bolesna, zastoinowa niewydolność serca powinny ostrzec lekarza. Diagnoza poparta jest wyraźnym spadkiem poziomu ultraczułego TSH (usTSH) w surowicy. W takim przypadku należy przerwać leczenie amiodaronem. Powrót do zdrowia następuje na ogół w ciągu kilku miesięcy od zaprzestania leczenia; powrót do stanu klinicznego poprzedza normalizację wyników badań czynności tarczycy. Ciężkie przypadki, z klinicznymi objawami tyreotoksyczności, czasami śmiertelnymi, wymagają natychmiastowej interwencji terapeutycznej. Leczenie należy dostosować. w indywidualnym przypadku: leki przeciwtarczycowe (co nie zawsze może być skuteczne) i możliwe leczenie kortykosteroidami.
Zaburzenia wątroby (patrz punkt 4.8)
Zaleca się ścisłe monitorowanie czynności wątroby (aminotransferaz) na początku leczenia amiodaronem i regularnie w trakcie leczenia.Ostre zaburzenia wątroby (w tym ciężka niewydolność wątroby lub niewydolność wątroby, czasami śmiertelna) i przewlekłe choroby wątroby mogą wystąpić po podaniu amiodaronu doustnie i dożylnie oraz w ciągu W związku z tym dawkę amiodaronu należy zmniejszyć lub przerwać leczenie, jeśli zwiększenie aktywności aminotransferaz jest ponad 3-krotnie wyższe od górnej granicy normy.
Kliniczne i biologiczne objawy przewlekłych zaburzeń czynności wątroby spowodowanych doustnym podawaniem amiodaronu mogą być minimalne (hepatomegalia, zwiększenie aktywności aminotransferaz do 5-krotności wartości odpowiadającej górnej granicy normy) i przemijające po przerwaniu leczenia, jednak zgłaszano przypadki. śmiertelny wynik.
W przypadku hepatomegalii lub podejrzenia cholestazy lek należy niezwłocznie odstawić, a chorego poddać kontroli ultrasonograficznej. Z tych powodów lek nie może być stosowany u pacjentów z wyraźnymi klinicznymi i laboratoryjnymi objawami aktywnej choroby wątroby; w łagodniejszych przypadkach może być stosowany tylko wtedy, gdy jest to niezbędne i musi zostać zawieszony, gdy nastąpi pogorszenie uszkodzenia wątroby.
Zaburzenia nerwowo-mięśniowe (patrz punkt 4.8)
Amiodaron może wywoływać obwodową neuropatię czuciowo-ruchową i (lub) miopatię. Zagojenie następuje zwykle w ciągu kilku miesięcy po odstawieniu amiodaronu, ale czasami może być niepełne.
Zaburzenia oka (patrz punkt 4.8)
W przypadku niewyraźnego widzenia lub pogorszenia ostrości wzroku należy natychmiast wykonać pełne badanie okulistyczne, w tym badanie dna oka.
Początek neuropatii wzrokowej i (lub) zapalenia nerwu wzrokowego wymaga odstawienia amiodaronu w celu uniknięcia potencjalnej progresji do ślepoty.
Interakcje leków (patrz punkt 4.5)
Nie zaleca się jednoczesnego stosowania amiodaronu z następującymi lekami: beta-adrenolityki, blokery kanału wapniowego zmniejszające częstość akcji serca (werapamil, diltiazem), pobudzające środki przeczyszczające, które mogą powodować hipokaliemię.
Laktoza
Każda tabletka zawiera 71 mg laktozy, dlatego zgodnie z zalecanym dawkowaniem maksymalna ilość laktozy, jaką można przyjmować z AMIODAREM to 213 mg na dobę. Pacjenci z rzadką dziedziczną nietolerancją galaktozy, niedoborem laktazy typu Lapp lub zespołem złego wchłaniania glukozy-galaktozy nie powinni przyjmować tego leku.
Środki ostrożności dotyczące stosowania
Ponieważ działania niepożądane (patrz punkt 4.8) są na ogół zależne od dawki, należy podać najmniejszą skuteczną dawkę podtrzymującą.
Należy doradzić pacjentom, aby unikali ekspozycji na słońce i stosowali środki ochronne podczas leczenia (patrz punkt 4.8).
Monitorowanie (patrz rozdziały 4.4 „Ostrzeżenia specjalne” i 4.8)
Przed rozpoczęciem leczenia amiodaronem zaleca się wykonanie EKG i pomiar stężenia potasu w surowicy.W trakcie leczenia zaleca się monitorowanie aktywności aminotransferaz (patrz punkt 4.4 „Specjalne ostrzeżenia”) i EKG. Ponadto, ponieważ amiodaron może powodować niedoczynność lub nadczynność tarczycy, zaleca się prowadzenie monitorowania klinicznego i biologicznego (usTSH) przed rozpoczęciem i w trakcie leczenia oraz przez kilka miesięcy po jego zakończeniu, szczególnie u pacjentów z chorobami tarczycy w wywiadzie lub osoby starsze zawieszenie. W przypadku podejrzenia dysfunkcji tarczycy należy zmierzyć poziom usTSH w surowicy.
Zwłaszcza w kontekście przewlekłego podawania leków antyarytmicznych zgłaszano przypadki zwiększonej defibrylacji komorowej i/lub progu stymulacji stymulatora lub wszczepialnego kardiowersora-defibrylatora, co może potencjalnie modyfikować jego skuteczność.Weryfikacja działania urządzenia przed i podczas terapii amiodaronem.
Nieprawidłowości tarczycy (patrz punkt 4.8).
Obecność jodu w cząsteczce amiodaronu może zakłócać wiązanie radioaktywnego jodu. Jednak wyniki testów czynnościowych tarczycy (wolna T3, wolna T4, ultraczułe TSH) pozostają możliwe do interpretacji.
Amiodaron hamuje obwodową konwersję tyroksyny (T4) do trijodotyroniny (T3) i może powodować izolowane zmiany biochemiczne (wzrost wolnej T4 w surowicy, podczas gdy wolna T3 nieznacznie spada lub nawet pozostaje na normalnym poziomie) u pacjentów z kliniczną eutyreozyą. W takich przypadkach nie ma powodu do przerwania leczenia amiodaronem.
Podejrzenie niedoczynności tarczycy należy rozważyć w przypadku wystąpienia następujących ogólnie łagodnych objawów klinicznych: przyrost masy ciała, nietolerancja zimna, zmniejszona aktywność, nadmierna bradykardia. Diagnoza jest poparta wyraźnym wzrostem usTSH w surowicy. Eutyreoza powraca zwykle w ciągu 1 do 3 miesięcy po zaprzestaniu leczenia. W sytuacjach zagrażających życiu leczenie amiodaronem można kontynuować w połączeniu z L-tyroksyną. Dawkę L-tyroksyny dostosowuje się do poziomu TSH.
Pacjenci pediatryczni
Nie wykazano bezpieczeństwa i skuteczności amiodaronu u tych pacjentów, dlatego nie zaleca się jego stosowania u tych pacjentów.
Znieczulenie (patrz punkty 4.5 i 4.8)
Przed zabiegiem anestezjolog powinien zostać poinformowany, że pacjent jest leczony amiodaronem.
Związek ze statynami
Zaleca się, aby w skojarzeniu z amiodaronem stosować statyny niemetabolizowane przez CYP 3A4 (patrz punkt 4.5).
04.5 Interakcje z innymi produktami leczniczymi i inne formy interakcji
Skojarzenia przeciwwskazane
- Leki mogące wywołać „torsade de pointes” (patrz punkt 4.3):
• leki przeciwarytmiczne, takie jak leki klasy IA, sotalol, bepridil.
• leki nie przeciwarytmiczne, takie jak winkamina, niektóre leki neuroleptyczne, w tym sultoprid, cyzapryd, erytromycyna E.V., pentamidyna (do podawania pozajelitowego), ponieważ może występować zwiększone ryzyko zagrażającego życiu „torsade de pointes”.
- leki MAOI
Stowarzyszenia niezalecane
- Beta-blokery i blokery kanału wapniowego, które zmniejszają częstość akcji serca (werapamil, diltiazem) ze względu na możliwość automatyzmu (nadmierna bradykardia) i zaburzenia przewodzenia.
- Stymulujące środki przeczyszczające: z powodu pojawienia się możliwej hipokaliemii, co w konsekwencji zwiększa ryzyko „torsade de pointes”; dlatego należy stosować inne rodzaje środków przeczyszczających.
- Należy unikać fluorochinolonów u pacjentów leczonych amiodaronem.
Skojarzenia wymagające ostrożności
- Leki zdolne do wywoływania hipokaliemii:
• leki moczopędne mogące powodować hipokaliemię, samodzielnie lub w połączeniu
• ogólnoustrojowe glikokortykoidy i mineralokortykosteroidy, tetrakozaktyd
• amfoterycyna B przez E.V.
Należy zapobiegać (i korygować) hipokaliemię, monitorować odstęp QT i nie stosować leków przeciwarytmicznych w przypadku „torsade de pointes” (należy rozpocząć stymulację komorową; można zastosować magnez dożylnie).
- Doustne antykoagulanty:
Amiodaron zwiększa stężenie warfaryny poprzez hamowanie cytochromu P450 2C9. Połączenie warfaryny i amiodaronu może nasilać działanie doustnego leku przeciwzakrzepowego, zwiększając w ten sposób ryzyko krwawienia.Stężenie protrombiny należy kontrolować bardziej regularnie i dostosowywać dawkowanie leku przeciwzakrzepowego zarówno podczas leczenia amiodaronem, jak i po jego przerwaniu.
- Cyfrowy
Mogą wystąpić zaburzenia automatyzmu (nadmierna bradykardia) i przewodzenia przedsionkowo-komorowego (działanie synergiczne), ponadto możliwy jest wzrost stężenia digoksyny w osoczu na skutek zmniejszenia klirensu digoksyny.
Dlatego należy monitorować stężenia digoksyny w elektrokardiografii i osoczu; a pacjenci powinni być monitorowani pod kątem klinicznych objawów toksyczności naparstnicy. Może być konieczne dostosowanie dawki naparstnicy.
- Fenytoina
Amiodaron zwiększa stężenie fenytoiny w osoczu poprzez hamowanie cytochromu P450 2C9. Skojarzenie fenytoiny z amiodaronem może zatem prowadzić do przedawkowania fenytoiny powodującego objawy neurologiczne.Należy prowadzić monitorowanie kliniczne i zmniejszyć dawkę fenytoiny, gdy tylko pojawią się objawy przedawkowania; należy określić stężenie fenytoiny w osoczu.
- Flekainid
Amiodaron zwiększa stężenie flekainidu w osoczu poprzez hamowanie cytochromu CYP 2D6. Następnie należy dostosować dawkę flekainidu.
- Leki metabolizowane przez cytochrom P450 3A4:
Gdy leki te są podawane jednocześnie z amiodaronem, inhibitorem CYP 3A4, może wystąpić zwiększenie ich stężenia w osoczu, co może prowadzić do zwiększenia ich toksyczności.
• Statyny: Ryzyko działania toksycznego na mięśnie zwiększa się w przypadku jednoczesnego podawania amiodaronu ze statynami metabolizowanymi przez CYP 3A4, takimi jak symwastatyna, atorwastatyna i lowastatyna. Zaleca się, aby w skojarzeniu z amiodaronem stosować statyny niemetabolizowane przez CYP 3A4.
• Cyklosporyna: Skojarzenie z amiodaronem może zwiększać stężenie cyklosporyny w osoczu.Dawkowanie należy dostosować.
• Fentanyl: Połączenie z amiodaronem może nasilać działanie farmakologiczne fentanylu i zwiększać ryzyko jego toksyczności.
• Inne leki metabolizowane przez CYP 3A4: lidokaina, takrolimus, syldenafil, midazolam, triazolam, dihydroergotamina, ergotamina.
Znieczulenie ogólne (patrz punkty 4.4 „Środki ostrożności dotyczące stosowania” i 4.8)
U pacjentów poddawanych znieczuleniu ogólnemu zgłaszano potencjalnie poważne powikłania: bradykardię (niewrażliwość na atropinę), niedociśnienie, zaburzenia przewodzenia, zmniejszenie pojemności minutowej serca.
Obserwowano bardzo rzadkie przypadki ciężkich powikłań oddechowych (zespół ostrej niewydolności oddechowej dorosłych), czasami śmiertelnych, zwykle w okresie bezpośrednio po zabiegu chirurgicznym.Może to być związane z możliwą interakcją z wysokim stężeniem tlenu.
04.6 Ciąża i laktacja
Ciąża
Amiodaron jest przeciwwskazany w ciąży, chyba że korzyści przewyższają ryzyko, ze względu na jego wpływ na tarczycę płodu.
Czas karmienia
Amiodaron jest przeciwwskazany u matek karmiących piersią, ponieważ przenika w znacznych ilościach do mleka matki.
04.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Na podstawie danych dotyczących bezpieczeństwa amiodaronu nie wykazano wpływu na zdolność prowadzenia pojazdów i obsługiwania maszyn.
04.8 Działania niepożądane
Następujące działania niepożądane zostały sklasyfikowane według klasyfikacji układów i narządów oraz częstości przy użyciu następującej konwencji: bardzo często (> = 10%), często (> = 1% i = 0,1% i = 0,01% i
Zaburzenia układu krwionośnego i limfatycznego
Bardzo rzadkie:
• Niedokrwistość hemolityczna
• Anemia aplastyczna
• Trombocytopenia
Patologie serca
Pospolity:
bradykardia, zwykle umiarkowana i zależna od dawki.
Niezwykły:
• zaburzenia przewodzenia (blok zatokowo-przedsionkowy, różne stopnie bloku przedsionkowo-komorowego) (patrz punkt 4.4 „Środki ostrożności dotyczące stosowania”).
• początek lub pogorszenie arytmii, po którym czasami dochodzi do zatrzymania akcji serca (patrz punkt 4.4 „Specjalne ostrzeżenia” i 4.5).
- Bardzo rzadkie:
Znaczna bradykardia lub zatrzymanie zatokowe u pacjentów z dysfunkcją węzła zatokowego i/lub u pacjentów w podeszłym wieku.
Patologie oczu
- Bardzo częste
Mikrodepozyty na rogówce, zazwyczaj ograniczone do obszaru pod źrenicą. Mogą towarzyszyć postrzeganiu kolorowych aureoli w oślepiającym świetle lub niewyraźnym widzeniu. Mikrodepozyty rogówki składają się ze złożonych złogów lipidowych i ustępują po przerwaniu leczenia.
- Bardzo rzadkie
Neuropatia/zapalenie nerwu wzrokowego, które może prowadzić do ślepoty (patrz punkt 4.4 „Specjalne ostrzeżenia”).
Zaburzenia skóry i tkanki podskórnej
- Bardzo częste
Uczulenie na światło (patrz punkt 4.4 „Środki ostrożności dotyczące stosowania”)
- Pospolity
Przebarwienia skóry w kolorze łupkowo-szarym lub niebieskawym w przypadku długotrwałego leczenia wysokimi dawkami dziennymi; te przebarwienia ustępują powoli po przerwaniu leczenia.
- Bardzo rzadkie
• rumień podczas radioterapii
• ogólnie niespecyficzne wysypki skórne
• złuszczające zapalenie skóry
• łysienie
-Częstotliwość nieznana
Pokrzywka
Zaburzenia endokrynologiczne (patrz punkty 4.4 „Specjalne ostrzeżenia” i 4.4 „Środki ostrożności dotyczące stosowania”)
- Pospolity:
• Niedoczynność tarczycy
• Nadczynność tarczycy czasami śmiertelna
- Bardzo rzadkie:
Zespół nieprawidłowego wydzielania hormonu antydiuretycznego (SIADH)
Zaburzenia wątroby i dróg żółciowych (patrz punkty 4.4 „Specjalne ostrzeżenia” i 4.4 „Środki ostrożności dotyczące stosowania”)
- Bardzo częste:
izolowany wzrost aktywności aminotransferaz w surowicy, zwykle umiarkowany (1,5 do 3 razy większy). na początku terapii mogą powrócić do normy po zmniejszeniu dawki lub nawet spontanicznie.
- Pospolity:
Ostra choroba wątroby z podwyższonym poziomem transaminaz w surowicy i (lub) żółtaczką, w tym niewydolność wątroby, czasami śmiertelna.
- Bardzo rzadkie:
Przewlekłe choroby wątroby (pseudoalkoholowe zapalenie wątroby, marskość) czasami śmiertelne.
Zaburzenia układu oddechowego, klatki piersiowej i śródpiersia (patrz punkt 4.4 „Specjalne ostrzeżenia”)
- Ciężka toksyczność płucna, czasami śmiertelna, może wystąpić u około 10% pacjentów, zwłaszcza jeśli nie zostanie ona szybko zdiagnozowana. Ta toksyczność obejmuje zapalenie pęcherzyków płucnych, zapalenie płuc, objawy astmy, lipoidowe zapalenie płuc i zwłóknienie płuc. Toksyczności płucnej, kaszlu i duszności mogą towarzyszyć radiologiczne i czynnościowe objawy śródmiąższowego zapalenia płuc (zmieniona dyfuzja pęcherzykowo-włośniczkowa); pojawienie się tych objawów klinicznych wymaga wstrzymania terapii i podania leków kortykosteroidowych.Ta symptomatologia może również objawiać się późno po przerwaniu leczenia: dlatego wymagane jest uważne i długotrwałe monitorowanie pacjenta w celu zidentyfikowania możliwych zmian w czynności płuc.
• U pacjentów, u których wystąpi duszność wysiłkowa, sama lub związana z pogorszeniem stanu ogólnego (zmęczenie, utrata masy ciała, gorączka) należy wykonać prześwietlenie klatki piersiowej.
• Choroby płuc ustępują zwykle po wczesnym przerwaniu leczenia amiodaronem. Objawy kliniczne zwykle ustępują w ciągu 3-4 tygodni, po czym następuje wolniejsza poprawa czynności płuc i obrazu radiologicznego (kilka miesięcy). Dlatego należy przerwać leczenie amiodaronem i rozważyć leczenie kortykosteroidami.
- Pospolity:
toksyczność płucna (pęcherzykowe/śródmiąższowe zapalenie lub zwłóknienie płuc, zapalenie opłucnej, zarostowe zapalenie oskrzelików ze zorganizowanym zapaleniem płuc/BOOP), czasami śmiertelne (patrz punkt 4.4 „Specjalne ostrzeżenia”).
- Bardzo rzadkie:
• skurcz oskrzeli u pacjentów z ciężką niewydolnością oddechową, a zwłaszcza u pacjentów z astmą
• zespół ostrej niewydolności oddechowej dorosłych, czasami śmiertelny, zwykle bezpośrednio po zabiegu chirurgicznym (możliwa interakcja z „wysokim stężeniem tlenu)” (patrz punkty 4.4 „Specjalne ostrzeżenia”, 4.4 „Środki ostrożności dotyczące stosowania” i 4.5).
- Częstość nieznana: krwotok płucny
Zaburzenia układu odpornościowego
- Częstość nieznana: obrzęk naczynioruchowy (obrzęk Quinckego)
Zaburzenia żołądkowo-jelitowe
- Bardzo częste:
łagodne zaburzenia żołądkowo-jelitowe (nudności, wymioty, zaburzenia smaku), które zwykle występują po podaniu dawki nasycającej i ustępują po zmniejszeniu dawki.
Testy diagnostyczne
-Bardzo rzadkie:
wzrost kreatyniny we krwi.
Zaburzenia układu nerwowego
- Pospolity:
• drżenie pozapiramidowe.
• koszmary.
• zaburzenia snu.
- Niezwykłe:
• obwodowa neuropatia czuciowo-ruchowa i (lub) miopatia, zwykle przemijające po odstawieniu leku (patrz punkt 4.4 „Specjalne ostrzeżenia”).
- Bardzo rzadkie:
• ataksja móżdżkowa.
• łagodne nadciśnienie śródczaszkowe (guz rzekomy mózgu).
• bół głowy.
Choroby układu rozrodczego i piersi
- Bardzo rzadkie:
• zapalenie najądrza.
• impotencja.
Patologie naczyniowe
- Bardzo rzadkie:
zapalenie naczyń.
04.9 Przedawkowanie
Niewiele jest dostępnych informacji dotyczących ostrego przedawkowania amiodaronu. Zgłoszono kilka przypadków bradykardii zatokowej, zatrzymania akcji serca, częstoskurczu komorowego, „torsade de pointes”, niewydolności krążenia i uszkodzenia wątroby.
Leczenie musi być objawowe. Amiodaron i jego metabolity nie podlegają dializie.
05.0 WŁAŚCIWOŚCI FARMAKOLOGICZNE
05.1 Właściwości farmakodynamiczne
Grupa farmakoterapeutyczna: Układ sercowo-naczyniowy, leki przeciwarytmiczne, klasa III. Kod ATC: C01BD01
Właściwości antyarytmiczne:
- Faza 3 wydłużenia potencjału czynnościowego włókna sercowego głównie ze względu na zmniejszenie prądu potasowego (klasa III według klasyfikacji Vaughana Williamsa), to wydłużenie nie jest skorelowane z częstością akcji serca.
- Zmniejszona automatyzacja zatok, prowadząca do bradykardii, niewrażliwa na podanie atropiny.
- Niekonkurencyjne hamowanie alfa- i beta-adrenergiczne.
- Spowolnienie przewodnictwa zatokowo-przedsionkowego, przedsionkowego i węzłowego, które jest bardziej wyraźne, gdy częstość akcji serca jest wysoka.
- Brak zmian w przewodzeniu śródkomorowym.
- Na poziomie przedsionkowym, węzłowym i komorowym: wydłużenie okresu refrakcji i zmniejszenie pobudliwości mięśnia sercowego.
- Spowolnienie przewodzenia i wydłużenie okresów refrakcji w dodatkowych odcinkach przedsionkowo-komorowych.
Właściwości przeciwniedokrwienne:
- Umiarkowany spadek oporu obwodowego i zmniejszenie częstości akcji serca z wynikającym z tego zmniejszeniem zapotrzebowania na tlen.
- Niekonkurencyjny antagonizm dla receptorów alfa- i beta-adrenergicznych.
- Zwiększony wyrzut wieńcowy dzięki bezpośredniemu oddziaływaniu na mięśnie gładkie tętnic mięśnia sercowego.
- Utrzymanie pojemności minutowej serca z powodu zmniejszonego ciśnienia w aorcie i oporu obwodowego.
Inne:
- Brak znaczących negatywnych efektów inotropowych.
05.2 Właściwości farmakokinetyczne
Po podaniu doustnym amiodaron wchłania się powoli i zmiennie.
Objętość dystrybucji amiodaronu jest bardzo duża, ale zmienna ze względu na rozległą akumulację w różnych rejonach (tkanka tłuszczowa, narządy o dużej perfuzji, takie jak wątroba, płuca i śledziona).
Biodostępność po podaniu doustnym waha się od 30 do 80%, w zależności od indywidualnego pacjenta (średnia wartość wynosi około 50%).Po jednorazowym podaniu maksymalne stężenie w osoczu osiągane jest po 3-7 godzinach. Efekty terapeutyczne uzyskuje się zwykle po tygodniu ( od kilku dni do dwóch tygodni) w zależności od dawki nasycającej.
Amiodaron ma długi okres półtrwania i wykazuje znaczną zmienność osobniczą (od 20 do 100 dni).W pierwszych dniach terapii lek kumuluje się prawie we wszystkich tkankach, zwłaszcza tłuszczowych. Eliminacja następuje po kilku dniach. stan stężenia w osoczu osiąga się od jednego do kilku miesięcy, w zależności od indywidualnego pacjenta.
Biorąc pod uwagę powyższe cechy, dawki nasycające muszą być stosowane w celu szybkiego uzyskania poziomów w tkankach niezbędnych do uzyskania efektu terapeutycznego.
Każda dawka 200 mg amiodaronu zawiera 75 mg jodu, z czego 6 mg odrywa się od cząsteczki jako wolny jod. Amiodaron jest wydalany głównie z drogami żółciowymi i kałowymi. Wydalanie nerkowe jest znikome: pozwala to na podawanie standardowych dawek pacjentom z niewydolnością nerek.
Po przerwaniu leczenia eliminacja trwa kilka miesięcy, dlatego należy liczyć się z utrzymywaniem się efektu farmakodynamicznego od 10 dni do miesiąca.
05.3 Przedkliniczne dane o bezpieczeństwie
Toksyczność ostra: LD50 u szczura 170 mg/kg E.V.,>3000 mg/kg os, u myszy 450 mg/kg i.p.,>3000 mg/kg os, u psa rasy beagle 85-150 mg/kg E.V.
Toksyczność przewlekła: nie wykryto śmiertelności, utraty masy ciała ani zmiany parametrów biologicznych przy dawkach doustnych do 37,5 mg/kg/dobę (4 tygodnie) i 16 mg/kg/dobę (52 tygodnie) u szczurów oraz do 12,5 mg/ kg / dzień u psów.
Teratogeneza: badania przeprowadzone na szczurach (100 mg/kg/dzień) i królikach (75 mg/kg/dzień) nie wykazały żadnych objawów toksyczności dla płodu.
06.0 INFORMACJE FARMACEUTYCZNE
06.1 Zaróbki
Laktoza jednowodna Skrobia kukurydziana Poliwidon Krzemionka koloidalna bezwodna Magnezu stearynian
06.2 Niezgodność
Nie są znane żadne niezgodności.
06.3 Okres ważności
3 lata.
06.4 Specjalne środki ostrożności przy przechowywaniu
Ten lek nie wymaga żadnych specjalnych warunków przechowywania.
06.5 Rodzaj opakowania bezpośredniego i zawartość opakowania
Pudełko tekturowe zawierające 2 blistry po 10 tabletek każdy.
06.6 Instrukcje użytkowania i obsługi
Brak specjalnych instrukcji.
07.0 PODMIOT POZWOLENIA NA DOPUSZCZENIE DO OBROTU
SIGMA-TAU Industrie Farmaceutiche Riunite S.p.A.
Viale Shakespeare, 47 -00144 Rzym
08.0 NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
A.I.C. n. 022033031
09.0 DATA PIERWSZEGO ZEZWOLENIA LUB PRZEDŁUŻENIA ZEZWOLENIA
Zezwolenie: 24.02.1971
Odnowienie: 01.06.2005
10.0 DATA ZMIAN TEKSTU
czerwiec 2010