WPROWADZENIE: Chrząstka stawowa to wysoce wyspecjalizowana tkanka łączna składająca się z komórek zwanych chondrocytami i otaczającej tkanki podporowej, macierzy. Ma perłowo-biały kolor i zakrywa końce kości stawowych, chroniąc je przed tarciem.Działa podobnie jak amortyzator, który jest w stanie chronić normalne relacje stawowe i umożliwia ruch.
Ze względu na całkowity brak unaczynienia i unerwienia chrząstka wykazuje słabą zdolność regeneracji w przypadku urazu, zwłaszcza jeśli jest on ciężki. Nawet gdy ta regeneruje się, nadal powoduje powstanie tkanki typu chrząstki włóknistej, mniej odpornej i elastycznej niż pierwotna; może zatem zagrażać funkcjonalności stawu i sprzyjać wystąpieniu z czasem zjawisk zwyrodnieniowych (artroza lub choroba zwyrodnieniowa stawów).
Uszkodzenia chrząstki są bardzo powszechnym problemem, łatwo występującym u osób starszych (zwyrodnieniowa choroba zwyrodnieniowa stawów), ale czasami także u młodych, gdzie uszkodzenia pochodzenia traumatycznego występują częściej z wysokim ryzykiem przekształcenia się w formy artretyczne. możliwości leczenia były ograniczone, a pacjent został skazany na kalectwo lub, jeśli to możliwe, na wymianę stawu na protezę stawową. Dziś więcej nadziei dają nowoczesne techniki chirurgiczne związane z inżynierią tkankową.
Możliwa jest stymulacja szpiku kostnego do tworzenia naprawczej tkanki chrzęstno-włóknistej, wykonanie wielu małych otworów (perforacji), powodujących mikrozłamania lub wypiłowanie powierzchni kości podchrzęstnej (część kostna pod chrząstką); jak wspomniano kilka linijek temu, tworzona tkanka naprawcza jest typu chrzęstno-włóknistego (seria B) i jako taka ma znacznie niższą funkcjonalność niż chrząstka dostarczana przez matkę naturę. Z tego powodu techniki te są obecnie wskazane w leczeniu płytkich i niewielkich zmian chrzęstnych.
W przypadku zmian bardziej rozległych można zdecydować się na przeszczep chrząstki.
Przeszczep chrząstki
Warto przede wszystkim wyjaśnić, że termin ten odnosi się nie do jednej, ale do trzech różnych technik chirurgicznych.
→ Implanty ochrzęstnej lub okostnej (cienkie błony, które pokrywają odpowiednio chrząstkę, z wyjątkiem części stawowych i kości, z wyjątkiem powierzchni stawowych i punktów wprowadzenia ścięgien). Chirurg pobiera płaty tych tkanek i wprowadza je do uszkodzonego obszaru, gdzie wywołują one wzrost tkanki podobnej do chrząstki lub chrząstki włóknistej.
WSKAZANIA: Wyniki długoterminowe są sprzeczne; z tego powodu nie jest to powszechna technika.
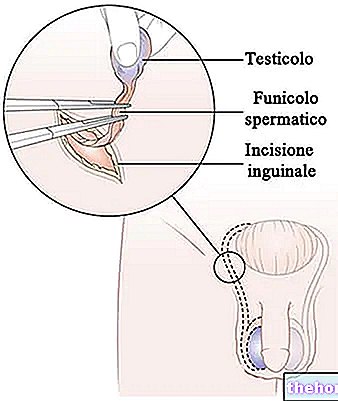
→ Mosaicoplastyka lub przeszczep chrzęstno-kostny: polega na użyciu cylindrów tkanki kostno-chrzęstnej (tj. fragmentów kości z leżącą na niej chrząstką) pobranych z uszkodzonego stawu tego samego pacjenta i wszczepionych uciskiem do ubytku chrząstki.
WSKAZANIA: ten przeszczep chrząstki można wykonać artroskopowo, dzięki czemu jest mało inwazyjny i nie powoduje problemów z odrzuceniem i infekcją. Jest wykonywany w tym samym czasie operacyjnym i jest wskazany tylko w przypadku niewielkich zmian, a głębokość nie jest czynnikiem ograniczającym; z oczywistych względów materiał kostno-chrzęstny niezbędny do przeszczepu jest w rzeczywistości ograniczony, a wyższe próbki mogłyby spowodować znaczne uszkodzenia w miejscu pobrania. Przeszczep chrząstki jest zatem wynikiem kompromisu: „obszar krytyczny dla funkcjonalności stawu” to „ naprawiony” pobierając chrząstkę z mniej ważnego obszaru, ale nie dla tego bezużytecznego lub zbędnego.
Przeszczepu chrząstki nie można wykonać w przypadku nieoperacyjnych stawów, takich jak palce, stopa lub kręgosłup; zamiast tego jest wskazany na kolano, kostkę, ramię i biodro.
→ Autologiczny przeszczep chondrocytów: komórki chrząstki są pobierane od pacjenta poprzez usunięcie małego wycinka chrząstki w obszarze nieobciążonym. Za pomocą technik biotechnologicznych pobrane chondrocyty izoluje się i hoduje w laboratorium przez 2-4 tygodnie, podczas których różnicują się poprzez zwielokrotnienie swojej liczby. W tym momencie pacjent przechodzi nową operację, podczas której zmiana zostaje oczyszczona i pokryta okostną, pozostawiając niewielki otwór, przez który następnie zostaną wstrzyknięte hodowane komórki. Płat okostnowy pobrany z przednio-przyśrodkowej powierzchni kości piszczelowej ipsilateralnej jest odpowiedzialny za wszelkie komplikacje, które mogą pojawić się w krótkim czasie; ponadto wymaga dość złożonej techniki chirurgicznej, której nie można wykonać artroskopowo. Aby przezwyciężyć te problemy, implanty autologicznych chondrocytów mogą być stosowane na nośniku kwasu hialuronowego pochodzenia biotechnologicznego, co również ma tę zaletę, że wymaga mniej inwazyjnej techniki chirurgicznej. Badania mają obecnie na celu identyfikację nowych nośników biotechnologicznych, które mogą sprzyjać wszczepianiu i proliferacji przeszczepionych kultur chondrocytów, zgodnie z charakterystyką „naturalnej” chrząstki stawowej.
Również w tym przypadku, ponieważ pacjent jest jednocześnie dawcą i biorcą, nie ma problemów z odrzuceniem lub infekcją. W przeciwieństwie do poprzedniej techniki czynnikiem ograniczającym jest nie tyle rozległość zmiany, co jej głębokość: jeśli uszkodzenie rozciąga się na leżącą poniżej kość (poważne urazy, osteochondroza, zaawansowana artroza), implant z trudem się zakorzenia, ponieważ nie podłoża kostnego opisanego w poprzednim przypadku Poszukuje się zatem materiałów biotechnologicznych, które działają jako odpowiednie podłoże, aby uniknąć dyspersji chondrocytów w otaczającym środowisku i sprzyjać ich wzrostowi nawet w obecności obecnie nieuleczalnych patologii.
UWAGI: zarówno zabiegi oparte na perforacjach, otarciach i mikrozłamaniach, jak i te z przeszczepem chrząstki są wskazane dla pacjentów w wieku poniżej 40-50 lat, ponieważ starzenie się zmniejsza zdolność proliferacyjną chrząstki do zera. ten artykuł dotyczy zaawansowanej choroby zwyrodnieniowej stawów.