Składniki aktywne: medroksyprogesteron (octan medroksyprogesteronu)
FARLUTAL 150 mg/3 ml zawiesina do wstrzykiwań do podania domięśniowego
Wkładki do opakowań Farlutal są dostępne dla rozmiarów opakowań:- FARLUTAL 150 mg/3 ml zawiesina do wstrzykiwań do podania domięśniowego
- Farlutal 250 mg tabletki, Farlutal 500 mg tabletki, Farlutal 500 mg/5 ml zawiesina doustna, Farlutal 1 g/10 ml zawiesina doustna
- Farlutal 10 mg tabletki, Farlutal 20 mg tabletki
- FARLUTAL 500 mg / 2,5 ml zawiesina do wstrzykiwań do wstrzykiwań domięśniowych, FARLUTAL 1 g / 5 ml zawiesina do wstrzykiwań do stosowania domięśniowego
Dlaczego stosuje się Farlutal? Po co to jest?
KATEGORIA TERAPEUTYCZNA
Progestyna.
WSKAZANIA TERAPEUTYCZNE
Endometrioza, wtórny brak miesiączki, paliatywne leczenie nowotworów hormonozależnych (układ moczowo-płciowy i piersi).
Przeciwwskazania Kiedy nie należy stosować leku Farlutal
Nadwrażliwość na substancję czynną lub na którąkolwiek substancję pomocniczą.
Medroksyprogesteron (MPA) jest przeciwwskazany u pacjentów z następującymi schorzeniami:
- stwierdzona lub podejrzenie ciąży
- krwawienie o nieokreślonym charakterze
- ciężka niewydolność wątroby
- podejrzenie lub wczesne stadium raka piersi
Środki ostrożności dotyczące stosowania Informacje ważne przed zastosowaniem leku Farlutal
Stosowanie preparatu z estrogenami, progestagenami i ich połączeniami nie powinno być dozwolone w okresie ciąży, w wieku rozrodczym musi być poprzedzone testem ciążowym.
Preparat może prowadzić do powstania nacieków na pośladkach; dlatego zaleca się wstrząsnąć zawiesiną przed użyciem i wstrzyknąć ją głęboko w wewnętrzne obszary mięśniowe.
Interakcje Jakie leki lub pokarmy mogą modyfikować działanie Farlutalu?
Poinformuj lekarza lub farmaceutę, jeśli ostatnio przyjmowałeś jakiekolwiek inne leki, nawet te bez recepty.
Jednoczesne podawanie produktu Farlutal z aminoglutetymidem może znacznie zmniejszyć biodostępność produktu Farlutal i zmniejszyć jego działanie terapeutyczne.
Pacjentów stosujących duże dawki preparatu FARLUTAL należy poinformować o zmniejszeniu skuteczności stosowania aminoglutetymidu.
Octan medroksyprogesteronu (MPA) jest metabolizowany głównie poprzez hydroksylację przez CYP3A4 in vitro. Nie przeprowadzono specjalnych badań dotyczących interakcji lekowych w celu oceny efektów klinicznych induktorów CYP3A4 lub inhibitorów MPA.
Ostrzeżenia Ważne jest, aby wiedzieć, że:
- W przypadku krwawienia z pochwy zalecana jest ocena diagnostyczna.
- Ponieważ progestageny mogą powodować pewne zatrzymanie płynów, należy monitorować stany, na które może wpływać ten czynnik.
- Pacjenci z depresją kliniczną w wywiadzie powinni być uważnie monitorowani podczas leczenia medroksyprogesteronem.
- Podczas leczenia progestagenem odnotowano spadek tolerancji glukozy. Z tego powodu pacjenci z cukrzycą powinni być pod ścisłą obserwacją podczas terapii progestagenem.
- Patolodzy (laboratorium) powinni być poinformowani o stosowaniu przez pacjentkę medroksyprogesteronu, jeśli badana jest tkanka endometrium lub szyjki macicy.
- Należy poinformować lekarza/laboratorium, że stosowanie medroksyprogesteronu może obniżać poziomy następujących markerów endokrynnych:
- do. sterydy osocza / moczu (np. kortyzol, estrogen, pregnanediol, progesteron, testosteron)
- b. Gonadotropiny z osocza / moczu (np. LH i FSH)
- C. Globulina wiążąca hormony płciowe
- W przypadku nagłej częściowej lub całkowitej utraty wzroku lub w przypadku wytrzeszczu, podwójnego widzenia lub migreny przed kontynuacją leczenia należy wykonać badanie okulistyczne w celu wykluczenia obrzęku brodawek i zmian naczyniowych siatkówki.
- Medroksyprogesteron nie wiązał się z wywoływaniem zaburzeń zakrzepowych lub zakrzepowo-zatorowych, jednak jego stosowanie nie jest zalecane u pacjentów z żylną chorobą zakrzepowo-zatorową (ŻChZZ) w wywiadzie. Zaleca się przerwanie leczenia medroksyprogesteronem u pacjentów, u których rozwinęła się ŻChZZ.
- Medroksyprogesteron może powodować objawy Cushingoida.
- Niektórzy pacjenci przyjmujący medroksyprogesteron mogą doświadczać zahamowania czynności nadnerczy. Medroksyprogesteron może obniżać poziom ACTH i hydrokortyzonu we krwi.
- Należy poinformować lekarza/laboratorium, że poza biomarkerami endokrynologicznymi wymienionymi w punkcie „Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania, stosowanie medroksyprogesteronu we wskazaniach onkologicznych może również determinować „częściową niedoczynność nadnerczy (zmniejszoną odpowiedź osi przysadki ) podczas testu metopironowego, wykazując w ten sposób zdolność kory nadnerczy do odpowiedzi na ACTH przed podaniem metopironu.
- Podawanie zarówno pojedynczej, jak i wielokrotnych dawek medroksyprogesteronu może skutkować przedłużonym brakiem jajeczkowania z brakiem miesiączki i/lub nieregularnymi miesiączkami.
- Hiperkalcemia u pacjentów z przerzutami do kości.
- Niewydolność wątroby (patrz rozdział „Przeciwwskazania”).
- Niewydolność nerek.
Wiek nie jest czynnikiem ograniczającym terapię, jednak leczenie progestynami może maskować początek przekwitania.
Zmniejszenie gęstości mineralnej kości
Obniżenie poziomu estrogenów w surowicy przez octan medroksyprogesteronu może skutkować zmniejszeniem gęstości mineralnej kości u kobiet przed menopauzą.To zmniejszenie gęstości mineralnej kości jest szczególnie niepokojące w okresie dojrzewania i wczesnej dorosłości, w okresach krytycznych dla wzrostu kości. Redukcja kości jest większa w przypadku i może nie być całkowicie odwracalne. zmniejszenie gęstości mineralnej kości podczas leczenia wydaje się być zasadniczo odwracalne, a wytwarzanie estrogenów w jajnikach jest zwiększone po przerwaniu stosowania medroksyprogesteronu do wstrzykiwań.
Retrospektywne badanie kohortowe w celu oceny wpływu wstrzykiwanego medroksyprogesteronu na częstość złamań kości przeprowadzono u 312 395 kobiet stosujących antykoncepcję w Wielkiej Brytanii. Porównano współczynniki występowania złamań (IRR) między osobami stosującymi medroksyprogesteron i niekorzystającymi.
Współczynnik zapadalności na każde złamanie w okresie obserwacji (co 5,5 roku) wynosił 1,41 (95% CI 1,35, 1,47). Porównania dokonano między podkohortami (N = 166,367) w okresie obserwacji i sześciu miesięcy przed pierwszym zarejestrowanym leczeniem antykoncepcyjnym między danymi uzyskanymi przed i po tym okresie. Porównując medroksyprogesteron stosujący i niestosujący, odsetek „przypadków na złamanie” przed leczeniem „(IRR 1,28, 95% CI 1,07, 1,53) porównano z odsetkiem „zapadalności” „po leczeniu” (IRR 1,37, 95% CI 1,29, 1,45). Ogólne wyniki tego badania prowadzą do wniosku, że wyższa częstość występowania złamań wśród osób stosujących medroksyprogesteron wynika głównie z innych czynników, a nie z ekspozycji na medroksyprogesteron przez okres dwóch lat) w celu kontroli urodzeń lub leczenia endometrium tylko wtedy, gdy inne podobne metody leczenia nie są odpowiednie.Medroksyprogesteron należy ocenić, gdy kobieta potrzebuje długotrwałego ciągłego stosowania leku. U dorastających kobiet interpretacja danych dotyczących medroksyprogesteronu powinna uwzględniać wiek pacjentki i dojrzałość szkieletu.
W analizie ryzyka/korzyści u kobiet z czynnikami ryzyka osteoporozy, takimi jak:
- Przewlekłe używanie tytoniu i/lub alkoholu
- Przewlekłe zażywanie leków, które mogą zmniejszać masę kostną, m.in. leki przeciwdrgawkowe lub kortykosteroidy
- Obniżenie wskaźnika masy ciała lub zaburzenia odżywiania, m.in. jadłowstręt psychiczny lub bulimia
- Zaburzenia metabolizmu kości
- Silna rodzinna historia osteoporozy
- Przedłużony brak jajeczkowania z brakiem miesiączki i (lub) zaburzeniami miesiączkowania może wystąpić po podaniu pojedynczej lub wielokrotnej dawki medroksyprogesteronu do wstrzykiwań.
Wszystkim pacjentom zaleca się przyjmowanie odpowiedniej ilości wapnia i witaminy D.
Wobec braku porównywalnych danych, zagrożenia zidentyfikowane w badaniu Women's Health Initiative (WHI) należy również uznać za podobne do innych dawek estrogenu skoniugowanego z doustnym octanem medroksyprogesteronu oraz w przypadku innych połączeń i powiązanych postaci farmaceutycznych. terapia.
Rak piersi
Zgłaszano zwiększone ryzyko raka piersi po stosowaniu doustnych kombinacji estrogenowo-progestagenowych u kobiet po menopauzie Wyniki pochodzące z randomizowanego, kontrolowanego placebo badania klinicznego, badania klinicznego WHI i badań epidemiologicznych wykazały zwiększone ryzyko raka piersi u kobiet, które od kilku lat stosują skojarzenie estrogen-progestagen jako terapię hormonalną. Nadmierne ryzyko wzrasta wraz z czasem stosowania, co ujawniło badanie WHI ze sprzężonymi estrogenami końskimi (CEE) plus MPA oraz badania obserwacyjne. Odnotowano również wzrost nieprawidłowych mammogramów z użyciem estrogenu i progestagenu, co wymaga dalszej oceny.
Choroby sercowo-naczyniowe
Nie należy stosować samego estrogenu lub w połączeniu z progestagenem w celu zapobiegania chorobom układu krążenia. Kilka prospektywnych, randomizowanych badań dotyczących odległych skutków skojarzonego leczenia estrogenowo-progestagenowego u kobiet po menopauzie wykazało zwiększone ryzyko wystąpienia zdarzeń sercowo-naczyniowych, takich jak zawał mięśnia sercowego, choroba wieńcowa, udar i żylna choroba zakrzepowo-zatorowa.
Choroba wieńcowa
Nie ma dowodów z randomizowanych, kontrolowanych badań klinicznych dotyczących korzyści sercowo-naczyniowych wynikających z ciągłego skojarzonego stosowania skoniugowanych estrogenów (CEE) i octanu medroksyprogesteronu (MPA) Dwa rozszerzone badania kliniczne (WHI CEE/MPA oraz Heart and Estrogen/Progestin Replacement Study – HERS ) wykazały możliwe zwiększone ryzyko powikłań sercowo-naczyniowych w pierwszym roku leczenia i brak ogólnych korzyści.
W badaniu WHI WHI CEE/MPA zaobserwowano zwiększone ryzyko incydentów wieńcowych (definiowanych jako zawał mięśnia sercowego niezakończony zgonem i śmiertelna choroba wieńcowa) u kobiet przyjmujących CEE/MPA w porównaniu do kobiet otrzymujących placebo (37 vs. 30 na 10 000 osób na rok). Zwiększone ryzyko żylnej choroby zakrzepowo-zatorowej obserwowano w pierwszym roku leczenia i utrzymywało się przez cały okres obserwacji.
Udar mózgu
W badaniu WHI CEE/MPA zaobserwowano zwiększone ryzyko udaru mózgu u kobiet przyjmujących CEE/MPA w porównaniu do kobiet otrzymujących placebo (29 vs 21 na 10 000 osób rocznie). Zwiększone ryzyko zaobserwowano w pierwszym roku leczenia i utrzymywało się przez cały okres obserwacji.
Żylna choroba zakrzepowo-zatorowa / zatorowość płucna
Terapia hormonalna wiąże się z wyższym względnym ryzykiem żylnej choroby zakrzepowo-zatorowej (ŻChZZ), tj. zakrzepicy żył głębokich lub zatorowości płucnej. W badaniu WHI CEE/MPA u kobiet przyjmujących CEE/MPA zaobserwowano dwukrotnie większą częstość występowania żylnej choroby zakrzepowo-zatorowej, w tym zakrzepicy żył głębokich i zatorowości płucnej, w porównaniu do kobiet otrzymujących placebo. Zwiększone ryzyko obserwowano w pierwszym roku leczenia i utrzymywało się przez cały okres obserwacji (patrz punkt Specjalne ostrzeżenia).
Demencja
Badanie WHIMS (Women's Health Initiative Memory Study (WHIMS), pomocnicze badanie WHI podawania CEE/MPA, wykazało zwiększone ryzyko prawdopodobnej demencji u kobiet w wieku 65 lat i starszych po menopauzie.
Ponadto terapia CEE/MPA nie zapobiegła łagodnym zaburzeniom poznawczym (MCI) u tych kobiet. Nie zaleca się stosowania terapii hormonalnej (HT) w celu zapobiegania otępieniu lub łagodnym zaburzeniom funkcji poznawczych u kobiet w wieku 65 lat i starszych.
Rak jajnika
Niektóre badania epidemiologiczne wykazały, że stosowanie przez pięć lub więcej lat samych produktów estrogenowych lub estrogenu z progestagenem u kobiet po menopauzie wiązało się ze zwiększonym ryzykiem raka jajnika. progestageny nie wykazały zwiększonego ryzyka raka jajnika.Inne badania nie wykazały żadnego istotnego związku.W badaniu WHI CEE/MPA stwierdzono, że estrogen plus progestageny zwiększają ryzyko raka jajnika, ale ryzyko to nie jest istotne statystycznie. kobiety stosujące HTZ wykazały zwiększone ryzyko śmiertelnego raka jajnika.
Zalecenia dotyczące wywiadu i badania fizykalnego
Przed rozpoczęciem terapii hormonalnej należy zebrać pełny wywiad lekarski. Przed leczeniem i okresowym badaniem fizykalnym należy zwrócić szczególną uwagę na ciśnienie krwi, narządy miednicy, narządy jamy brzusznej i piersi, w tym cytologię szyjki macicy
Ciąża i karmienie piersią
Poproś lekarza lub farmaceutę o poradę przed zażyciem jakiegokolwiek leku.
Ciąża
Octan medroksyprogesteronu nie jest zalecany u kobiet w ciąży. Niektóre dane sugerują możliwy związek między podawaniem progestyn w pierwszym trymestrze ciąży a występowaniem wad rozwojowych narządów płciowych u płodu w określonych okolicznościach.
Noworodki urodzone z nieoczekiwanych ciąż, które występują 1 lub 2 miesiące po wstrzyknięciu octanu medroksyprogesteronu, mogą być narażone na zwiększone ryzyko niskiej masy urodzeniowej, co w konsekwencji wiąże się ze zwiększonym ryzykiem zgonu noworodka.Ryzyko przypisywane jest niskie jak prawdopodobieństwo ciąży jest niski podczas stosowania octanu medroksyprogesteronu Nie ma ostatecznych informacji dotyczących innych postaci octanu medroksyprogesteronu.
Jeśli pacjentka zajdzie w ciążę podczas stosowania tego leku, powinna zostać poinformowana o potencjalnym ryzyku dla płodu.
Czas karmienia
Medroksyprogesteron i jego metabolity przenikają do mleka matki. Nie ma dowodów sugerujących, że stanowi to zagrożenie dla niemowlęcia.
Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Wpływ octanu medroksyprogesteronu na zdolność prowadzenia pojazdów i obsługiwania maszyn nie był systematycznie oceniany.
Ważne informacje o niektórych składnikach:
FARLUTAL zawiera parahydroksybenzoesan metylu. Może powodować reakcje alergiczne (nawet opóźnione) i wyjątkowo skurcz oskrzeli.
FARLUTAL zawiera parahydroksybenzoesan propylu. Może powodować reakcje alergiczne (nawet opóźnione) i wyjątkowo skurcz oskrzeli.
Farlutal zawiera mniej niż 1 mmol (23 mg) sodu na fiolkę, co oznacza, że jest praktycznie „wolny od sodu”.
Dawkowanie i sposób użycia Jak stosować Farlutal: Dawkowanie
Endometrioza: 50 mg na tydzień lub 100 mg co dwa tygodnie przez co najmniej sześć miesięcy.
Wtórny brak miesiączki: po leczeniu estrogenem wstrzyknąć pojedynczą dawkę 50 mg w 15. dniu sztucznego cyklu.
Leczenie paliatywne nowotworów hormonozależnych: dawkowanie na ogół zmienia się, w zależności od lokalizacji, od 1000 do 3000 mg na tydzień (podzielone na 2-3 podania: głębokie wstrzyknięcia domięśniowe). Normalnie mniejsze dawki stosowano w ok. godz. endometrium, najwyższe w piersi w fazie zaawansowanej i przerzutowej.
Farlutal można odpowiednio łączyć z innymi metodami leczenia przeciwnowotworowego (chemioterapia, radioterapia).
Przedawkowanie Co zrobić w przypadku przyjęcia zbyt dużej dawki leku Farlutal
Nie są znane żadne dane na ten temat.
W przypadku przypadkowego połknięcia/przyjmowania nadmiernej dawki FARLUTALU należy natychmiast powiadomić lekarza lub udać się do najbliższego szpitala.
W przypadku jakichkolwiek pytań dotyczących stosowania leku FARLUTAL należy zwrócić się do lekarza lub farmaceuty.
Skutki uboczne Jakie są skutki uboczne Farlutal
Jak każdy lek, FARLUTAL może powodować działania niepożądane, chociaż nie u każdego one wystąpią
Tabela działań niepożądanych (w zastosowaniu ginekologicznym i onkologicznym)
*Częstotliwość tych działań niepożądanych została obliczona na podstawie danych z 4 badań klinicznych z udziałem około 1300 pacjentów z chorobą nowotworową
Dodatkowe zdarzenia niepożądane zgłoszone po wprowadzeniu do obrotu
Po wprowadzeniu produktu do obrotu zgłaszano rzadkie przypadki osteoporozy, w tym złamań osteoporotycznych u pacjentów przyjmujących domięśniowo octan medroksyprogesteronu.
Przestrzeganie instrukcji zawartych w ulotce dołączonej do opakowania zmniejsza ryzyko wystąpienia działań niepożądanych
Zgłaszanie skutków ubocznych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie możliwe działania niepożądane niewymienione w tej ulotce, należy porozmawiać z lekarzem lub farmaceutą. Działania niepożądane można również zgłaszać bezpośrednio za pośrednictwem krajowego systemu zgłaszania pod adresem „https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse”. Więcej informacji na temat bezpieczeństwa stosowania tego leku.
Wygaśnięcie i przechowywanie
Termin ważności: patrz data ważności podana na opakowaniu.
UWAGA: Nie stosować leku po upływie terminu ważności wskazanego na opakowaniu.
Termin ważności dotyczy produktu w nienaruszonym opakowaniu, prawidłowo przechowywanego.
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa, co pomoże chronić środowisko.
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
KOMPOZYCJA
Każda butelka zawiera: składnik aktywny: octan medroksyprogesteronu 150 mg.
Substancje pomocnicze: makrogol „4000”; polisorbat „80”; parahydroksybenzoesan metylu; parahydroksybenzoesan propylu; chlorek sodu: karmeloza sodu; woda do wstrzykiwań.
POSTAĆ I ZAWARTOŚĆ FARMACEUTYCZNA
Zawiesina do wstrzykiwań do podania domięśniowego
FARLUTAL 150 mg / 3 ml, 1 butelka
Ulotka pakietu źródłowego: AIFA (Włoska Agencja Leków). Treść opublikowana w styczniu 2016 r. Przedstawione informacje mogą być nieaktualne.
Aby mieć dostęp do najbardziej aktualnej wersji, warto wejść na stronę AIFA (Włoskiej Agencji Leków). Zastrzeżenie i przydatne informacje.
01.0 NAZWA PRODUKTU LECZNICZEGO
FARLUTAL 150 MG / 3 ML ZAWIESINA INIEKCYJNA DO STOSOWANIA DOMIĘŚNIOWEGO
02.0 SKŁAD JAKOŚCIOWY I ILOŚCIOWY
FARLUTAL 150 mg/3 ml ZAWIESINA DO WSTRZYKIWAŃ DO STOSOWANIA DOMIĘŚNIOWEGO
Każda butelka o pojemności 3 ml zawiera:
składnik aktywny: octan medroksyprogesteronu 150 mg.
Substancje pomocnicze o znanym działaniu: parahydroksybenzoesan metylu; parahydroksybenzoesan propylu, chlorek sodu.
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
03.0 POSTAĆ FARMACEUTYCZNA
Zawiesina do wstrzykiwań.
04.0 INFORMACJE KLINICZNE
04.1 Wskazania terapeutyczne
Endometrioza, wtórny brak miesiączki, paliatywne leczenie nowotworów
zależny od hormonów (układ moczowo-płciowy i piersi).
04.2 Dawkowanie i sposób podawania
Podawać wyłącznie domięśniowo.
Endometrioza: 50 mg na tydzień lub 100 mg co dwa tygodnie przez co najmniej sześć miesięcy.
Wtórny brak miesiączki: po leczeniu estrogenem wstrzyknąć pojedynczą dawkę 50 mg w 15. dniu sztucznego cyklu.
Leczenie paliatywne nowotworów hormonozależnych: dawkowanie na ogół zmienia się, w zależności od lokalizacji, od 1000 do 3000 mg na tydzień (podzielone na 2-3 podania: głębokie wstrzyknięcia domięśniowe).
Normalnie mniejsze dawki stosowano w ok. godz. endometrium, najwyższe w piersi w fazie zaawansowanej i przerzutowej.
04.3 Przeciwwskazania
Nadwrażliwość na substancję czynną lub na którąkolwiek substancję pomocniczą wymienioną w punkcie 6.1.
Medroksyprogesteron (MPA) jest przeciwwskazany u pacjentów z następującymi schorzeniami:
• stwierdzona lub podejrzewana ciąża
• krwawienie o nieokreślonym charakterze
• ciężka niewydolność wątroby
• podejrzenie raka piersi lub raka piersi we wczesnym stadium
04.4 Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania
• W przypadku krwawienia z pochwy zaleca się przeprowadzenie badania diagnostycznego.
• Ponieważ progestageny mogą powodować pewne zatrzymanie płynów, należy monitorować stany, na które może wpływać ten czynnik.
• Pacjenci z depresją kliniczną w wywiadzie powinni być uważnie obserwowani podczas leczenia medroksyprogesteronem.
• Podczas leczenia progestagenem zaobserwowano zmniejszenie tolerancji glukozy. Z tego powodu pacjenci z cukrzycą powinni być pod ścisłą obserwacją podczas terapii progestagenem.
• Patolodzy (laboratorium) powinni być poinformowani o stosowaniu przez pacjentkę medroksyprogesteronu, jeśli badana jest tkanka endometrium lub szyjki macicy.
• Należy poinformować lekarza/laboratorium, że stosowanie medroksyprogesteronu może zmniejszać poziomy następujących markerów endokrynnych:
do. sterydy osocza / moczu (np. kortyzol, estrogen, pregnanediol, progesteron, testosteron)
b. Gonadotropiny z osocza / moczu (np. LH i FSH)
C. Globulina wiążąca hormony płciowe
• W przypadku nagłej częściowej lub całkowitej utraty wzroku lub w przypadku wytrzeszczu, podwójnego widzenia lub migreny, przed kontynuowaniem leczenia należy wykonać badanie wzroku w celu wykluczenia obrzęku brodawek i zmian naczyniowych siatkówki.
• Medroksyprogesteron nie wiązał się z wywoływaniem zaburzeń zakrzepowych lub zakrzepowo-zatorowych, jednak jego stosowanie nie jest zalecane u pacjentów z żylną chorobą zakrzepowo-zatorową (ŻChZZ) w wywiadzie. Zaleca się przerwanie leczenia medroksyprogesteronem u pacjentów, u których rozwinęła się ŻChZZ.
• Medroksyprogesteron może powodować objawy Cushingoida.
• Niektórzy pacjenci leczeni medroksyprogesteronem mogą doświadczać osłabienia czynności nadnerczy. Medroksyprogesteron może obniżać poziom ACTH i hydrokortyzonu we krwi.
• Lekarza/laboratorium należy poinformować, że poza biomarkerami endokrynologicznymi wymienionymi w punkcie „Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania (punkt 4.4)” stosowanie medroksyprogesteronu we wskazaniach onkologicznych może również skutkować „częściową niewydolnością nadnerczy (zmniejszeniem odpowiedzi osi przysadka-nadnercza) podczas testu metopironowego. Dlatego konieczne jest wykazanie zdolności kory nadnerczy do odpowiedzi na ACTH przed podaniem metopironu.
• Podawanie zarówno pojedynczej, jak i wielokrotnych dawek medroksyprogesteronu może skutkować przedłużonym brakiem jajeczkowania z brakiem miesiączki i/lub nieregularnymi miesiączkami.
• Hiperkalcemia u pacjentów z przerzutami do kości.
• Niewydolność wątroby (patrz punkt 4.3 „Przeciwwskazania”).
• Niewydolność nerek
Wiek nie jest czynnikiem ograniczającym terapię, jednak leczenie progestynami może maskować początek przekwitania.
Preparat może prowadzić do powstania nacieków na pośladkach; dlatego zaleca się wstrząsnąć zawiesiną przed użyciem i wstrzyknąć ją głęboko w wewnętrzne obszary mięśniowe.
Zmniejszenie gęstości mineralnej kości
Obniżenie poziomu estrogenów w surowicy spowodowane przez octan medroksyprogesteronu może skutkować zmniejszeniem gęstości mineralnej kości u kobiet przed menopauzą.To zmniejszenie gęstości mineralnej kości jest szczególnie niepokojące w okresie dojrzewania i wczesnej dorosłości, w okresach krytycznych dla wzrostu kości. Redukcja kości jest większa w przypadku wydłuża czas stosowania i może nie być całkowicie odwracalne Nie wiadomo, czy stosowanie medroksyprogesteronu we wstrzyknięciach przez młodsze kobiety może prowadzić do zmniejszenia masy kostnej i zwiększonego ryzyka złamań osteoporotycznych w późniejszym życiu. zmniejszenie gęstości mineralnej kości podczas leczenia wydaje się być zasadniczo odwracalne, a wytwarzanie estrogenów w jajnikach jest zwiększone po odstawieniu medroksyprogesteronu do wstrzykiwań (patrz punkt 5.1 – Właściwości farmakodynamiczne).
Retrospektywne badanie kohortowe w celu oceny wpływu wstrzykiwanego medroksyprogesteronu na częstość złamań kości przeprowadzono u 312 395 kobiet stosujących antykoncepcję w Wielkiej Brytanii. Porównano częstość występowania złamań (IRR) pomiędzy osobami stosującymi medroksyprogesteron i niestosującymi.Współczynnik częstości występowania dla każdego złamania w okresie obserwacji (co 5,5 roku) wynosił 1,41 (95% CI 1,35; 1,47). - kohorty (N = 166 367) w okresie obserwacji i sześć miesięcy przed pierwszym odnotowanym leczeniem antykoncepcyjnym pomiędzy danymi uzyskanymi przed i po tym okresie, stosujące medroksyprogesteron lub nie, odsetek „przypadków na złamanie” przed leczeniem „(IRR 1,28, 95% CI 1,07, 1,53) porównano z odsetkiem „zapadalności” „po leczeniu” (IRR 1,37, 95% CI 1,29, 1,45). Ogólne wyniki tego badania prowadzą do wniosku, że najwyższa zapadalność złamań wśród osób stosujących medroksyprogesteron wynika głównie z innych czynników, a nie z narażenia na medroksyprogesteron.
Medroksyprogesteron do wstrzykiwań należy stosować długoterminowo (np. przez dwa lata) w celu kontroli urodzeń lub leczenia endometrium tylko wtedy, gdy inne podobne metody leczenia nie są odpowiednie. Medroksyprogesteron należy ocenić, gdy kobieta potrzebuje długotrwałego ciągłego stosowania leku. U dorastających kobiet interpretacja danych dotyczących medroksyprogesteronu powinna uwzględniać wiek pacjentki i dojrzałość szkieletu.
W analizie ryzyka/korzyści u kobiet z czynnikami ryzyka osteoporozy, takimi jak:
• Przewlekłe używanie tytoniu i/lub alkoholu
• Przewlekłe zażywanie leków, które mogą zmniejszać masę kostną, m.in. leki przeciwdrgawkowe lub kortykosteroidy
• Obniżenie wskaźnika masy ciała lub zaburzenia odżywiania, np. jadłowstręt psychiczny lub bulimia
• Zaburzenia metabolizmu kości
• Silna rodzinna historia osteoporozy
• Przedłużony brak jajeczkowania z brakiem miesiączki i/lub zaburzeniami miesiączkowania może wystąpić po podaniu pojedynczej lub wielokrotnej dawki medroksyprogesteronu do wstrzykiwań
Wszystkim pacjentom zaleca się przyjmowanie odpowiedniej ilości wapnia i witaminy D.
Ze względu na brak porównywalnych danych, ryzyko zidentyfikowane w badaniu klinicznym Women's Health Initiative Study (WHI) (patrz punkt 5.1 – Właściwości farmakodynamiczne) należy również uznać za podobne do innych dawek estrogenu sprzężonego z doustnym i doustnym octanem medroksyprogesteronu. kombinacje i formy farmaceutyczne związane z terapią hormonalną.
Rak piersi
Zgłaszano zwiększone ryzyko raka piersi po zastosowaniu doustnych kombinacji estrogenowo-progestagenowych u kobiet po menopauzie Wyniki pochodzące z randomizowanego, kontrolowanego placebo badania klinicznego, badania klinicznego WHI i badań epidemiologicznych (patrz punkt 5.1 – Właściwości farmakodynamiczne) donosili o zwiększonym ryzyku raka piersi u kobiet, które przez kilka lat stosowały kombinację estrogenowo-progestagenową jako terapię hormonalną. Nadmierne ryzyko wzrasta wraz z czasem stosowania, co ujawniło badanie WHI ze sprzężonymi estrogenami końskimi (CEE) plus MPA oraz badania obserwacyjne. Odnotowano również wzrost nieprawidłowych mammogramów z użyciem estrogenu i progestagenu, co wymaga dalszej oceny.
Choroby sercowo-naczyniowe
Nie należy stosować samego estrogenu lub w połączeniu z progestagenem w celu zapobiegania chorobom układu krążenia. Kilka prospektywnych, randomizowanych badań dotyczących odległych skutków skojarzonego leczenia estrogenowo-progestagenowego u kobiet po menopauzie wykazało zwiększone ryzyko wystąpienia zdarzeń sercowo-naczyniowych, takich jak zawał mięśnia sercowego, choroba wieńcowa, udar i żylna choroba zakrzepowo-zatorowa.
Choroba wieńcowa
Nie ma dowodów z randomizowanych, kontrolowanych badań klinicznych dotyczących korzyści sercowo-naczyniowych wynikających z ciągłego skojarzonego stosowania skoniugowanych estrogenów (CEE) i octanu medroksyprogesteronu (MPA) Dwa rozszerzone badania kliniczne (WHI CEE/MPA oraz Heart and Estrogen/Progestin Replacement Study – HERS ) (patrz punkt 5.1 – Właściwości farmakodynamiczne) wykazały możliwe zwiększone ryzyko powikłań sercowo-naczyniowych w pierwszym roku leczenia i brak ogólnych korzyści.
W badaniu WHI WHI CEE/MPA zaobserwowano zwiększone ryzyko incydentów wieńcowych (definiowanych jako zawał mięśnia sercowego niezakończony zgonem i śmiertelna choroba wieńcowa) u kobiet przyjmujących CEE/MPA w porównaniu do kobiet otrzymujących placebo (37 vs. 30 na 10 000 osób na rok). Zwiększone ryzyko żylnej choroby zakrzepowo-zatorowej obserwowano w pierwszym roku leczenia i utrzymywało się przez cały okres obserwacji.
Udar mózgu
W badaniu WHI CEE/MPA zaobserwowano zwiększone ryzyko udaru mózgu u kobiet przyjmujących CEE/MPA w porównaniu do kobiet otrzymujących placebo (29 vs 21 na 10 000 osób rocznie). Zwiększone ryzyko zaobserwowano w pierwszym roku leczenia i utrzymywało się przez cały okres obserwacji.
Żylna choroba zakrzepowo-zatorowa / zatorowość płucna
Terapia hormonalna wiąże się z wyższym względnym ryzykiem żylnej choroby zakrzepowo-zatorowej (ŻChZZ), tj. zakrzepicy żył głębokich lub zatorowości płucnej. W badaniu WHI CEE/MPA u kobiet przyjmujących CEE/MPA zaobserwowano dwukrotnie większą częstość występowania żylnej choroby zakrzepowo-zatorowej, w tym zakrzepicy żył głębokich i zatorowości płucnej, w porównaniu do kobiet otrzymujących placebo. Zwiększone ryzyko obserwowano w pierwszym roku leczenia i utrzymywało się przez cały okres obserwacji (patrz punkt 4.4 – Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania).
Demencja
Badanie WHIMS (Women's Health Initiative Memory Study (WHIMS) (patrz punkt 5.1 – Właściwości farmakodynamiczne), badanie pomocnicze WHI, związane z podawaniem CEE/MPA, wykazało zwiększone ryzyko prawdopodobnego otępienia u kobiet podyplomowych , menopauza w wieku 65 lat lub więcej.
Ponadto terapia CEE/MPA nie zapobiegła łagodnym zaburzeniom poznawczym (MCI) u tych kobiet. Nie zaleca się stosowania terapii hormonalnej (HT) w celu zapobiegania otępieniu lub łagodnym zaburzeniom funkcji poznawczych u kobiet w wieku 65 lat i starszych.
Rak jajnika
Niektóre badania epidemiologiczne wykazały, że stosowanie przez pięć lub więcej lat samych produktów estrogenowych lub estrogenu z progestagenem u kobiet po menopauzie wiązało się ze zwiększonym ryzykiem raka jajnika. progestageny nie wykazały zwiększonego ryzyka raka jajnika.Inne badania nie wykazały żadnego istotnego związku.W badaniu WHI CEE/MPA stwierdzono, że estrogen plus progestageny zwiększają ryzyko raka jajnika, ale ryzyko to nie jest istotne statystycznie. kobiety stosujące HTZ wykazały zwiększone ryzyko śmiertelnego raka jajnika.
Zalecenia dotyczące wywiadu i badania fizykalnego
Przed rozpoczęciem terapii hormonalnej należy zebrać pełny wywiad lekarski. Przed leczeniem i okresowym badaniem fizykalnym należy zwrócić szczególną uwagę na ciśnienie krwi, narządy miednicy, jamy brzusznej i zatok, w tym cytologię szyjki macicy.
Ważne informacje o niektórych składnikach:
FARLUTAL zawiera parahydroksybenzoesan metylu. Może powodować reakcje alergiczne (nawet opóźnione) i wyjątkowo skurcz oskrzeli.
FARLUTAL zawiera parahydroksybenzoesan propylu. Może powodować reakcje alergiczne (nawet opóźnione) i wyjątkowo skurcz oskrzeli.
Farlutal zawiera mniej niż 1 mmol (23 mg) sodu na fiolkę, co oznacza, że jest praktycznie „wolny od sodu”.
04.5 Interakcje z innymi produktami leczniczymi i inne formy interakcji
Jednoczesne podawanie produktu FARLUTAL z aminoglutetymidem może znacząco obniżyć biodostępność produktu FARLUTAL.
Pacjentów stosujących duże dawki preparatu FARLUTAL należy ostrzec o zmniejszonej skuteczności stosowania aminoglutetymidu.
FARLUTAL można odpowiednio łączyć z innymi metodami leczenia przeciwnowotworowego (chemioterapia, radioterapia).
Octan medroksyprogesteronu (MPA) jest metabolizowany głównie poprzez hydroksylację przez CYP3A4 in vitro. Nie przeprowadzono specjalnych badań dotyczących interakcji lekowych w celu oceny efektów klinicznych induktorów CYP3A4 lub inhibitorów MPA.
04.6 Ciąża i laktacja
Ciąża
Octan medroksyprogesteronu jest przeciwwskazany u kobiet w ciąży.
Niektóre dane sugerują możliwy związek między podawaniem progestyn w pierwszym trymestrze ciąży a występowaniem wad rozwojowych narządów płciowych u płodu w określonych okolicznościach.
Noworodki urodzone z nieoczekiwanych ciąż, które występują 1 lub 2 miesiące po wstrzyknięciu octanu medroksyprogesteronu, mogą być narażone na zwiększone ryzyko niskiej masy urodzeniowej, co w konsekwencji wiąże się ze zwiększonym ryzykiem zgonu noworodka.Ryzyko przypisywane jest niskie jak prawdopodobieństwo ciąży jest niski podczas stosowania octanu medroksyprogesteronu Nie ma ostatecznych informacji dotyczących innych postaci octanu medroksyprogesteronu.
Jeśli pacjentka zajdzie w ciążę podczas stosowania tego leku, powinna zostać poinformowana o potencjalnym ryzyku dla płodu.
Czas karmienia
Medroksyprogesteron i jego metabolity przenikają do mleka matki. Nie ma dowodów sugerujących, że stanowi to zagrożenie dla niemowlęcia (patrz punkt 5.2 – Właściwości farmakokinetyczne).
04.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Wpływ octanu medroksyprogesteronu na zdolność prowadzenia pojazdów i obsługiwania maszyn nie był systematycznie oceniany.
04.8 Działania niepożądane
Tabela działań niepożądanych (w zastosowaniu ginekologicznym i onkologicznym)
*Częstotliwość tych działań niepożądanych została obliczona na podstawie danych z 4 badań klinicznych z udziałem około 1300 pacjentów z chorobą nowotworową
Dodatkowe zdarzenia niepożądane zgłoszone po wprowadzeniu do obrotu
Po wprowadzeniu produktu do obrotu zgłaszano rzadkie przypadki osteoporozy, w tym złamań osteoporotycznych u pacjentów przyjmujących domięśniowo octan medroksyprogesteronu.
Zgłaszanie podejrzewanych działań niepożądanych
Zgłaszanie podejrzewanych działań niepożądanych, które występują po dopuszczeniu produktu leczniczego do obrotu, jest ważne, ponieważ umożliwia ciągłe monitorowanie stosunku korzyści do ryzyka produktu leczniczego.
Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem krajowego systemu zgłaszania pod adresem: „www.agenziafarmaco.gov.it/it/responsabili”.
04.9 Przedawkowanie
Brak danych w tym zakresie.
05.0 WŁAŚCIWOŚCI FARMAKOLOGICZNE
05.1 Właściwości farmakodynamiczne
Grupa farmakoterapeutyczna: hormony i substancje pokrewne – progestageny.
Kod ATC: L02AB02.
Octan medroksyprogesteronu jest pochodną progesteronu czynną doustnie i pozajelitowo.
FARLUTAL podawany pozajelitowo w zalecanych dawkach kobietom z odpowiednim poziomem endogennych estrogenów przekształca endometrium proliferacyjne w endometrium wydzielnicze, a jego działanie przeciwnowotworowe przy podawaniu w dawkach farmakologicznych wynika z działania prowadzonego na poziomie podwzgórza oś - przysadkowo-gonady, na poziomie receptorów estrogenowych i na metabolizm steroidów na poziomie tkankowym.
Ze względu na przedłużone działanie i trudności w przewidzeniu czasu krwawienia z odstawienia po podaniu, FARLUTAL nie jest zalecany w przypadku wtórnego braku miesiączki lub krwawienia spowodowanego dysfunkcją macicy. W tych stanach zalecana jest terapia doustna.
Zmniejszenie gęstości mineralnej kości
Nie ma badań dotyczących wpływu octanu medroksyprogesteronu na zmniejszenie gęstości mineralnej kości przy podawaniu w dużych dawkach pozajelitowych (np. stosowanie onkologiczne).
Jednak badanie kliniczne z udziałem dorosłych kobiet w wieku rozrodczym, które otrzymywały domięśniowo 150 mg octanu medroksyprogesteronu co 3 miesiące w celach antykoncepcyjnych, wykazało średnie zmniejszenie gęstości mineralnej kości kręgosłupa lędźwiowego o 5,4% w ciągu 5 lat, z przynajmniej częściowym przywróceniem gęstości kości przez pierwsze dwa lata po zaprzestaniu leczenia.Podobne badanie kliniczne u nastoletnich kobiet, które otrzymywały octan medroksyprogesteronu w dawce 150 mg co 3 miesiące w celach antykoncepcyjnych, wykazało podobne zmniejszenie gęstości mineralnej kości, które było jeszcze bardziej widoczne w ciągu pierwszych dwóch lat leczenia. co najmniej częściowo odwracalne po zaprzestaniu leczenia.
05.2 Właściwości farmakokinetyczne
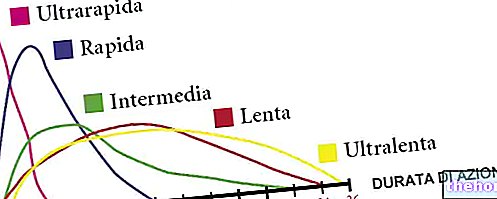
Octan medroksyprogesteronu (MPA) jest szybko wchłaniany z przewodu pokarmowego i pochwy. Po podaniu domięśniowym następuje powolne wchłanianie MPA. Maksymalne stężenia w surowicy obserwuje się po 2-6 godzinach (podawanie doustne) i po 4-20 dniach (podawanie domięśniowe). Pozorny okres półtrwania waha się od około 30-60 godzin po podaniu doustnym do około 6 tygodni po podaniu domięśniowym MPA wiąże się w 90-95% z białkami osocza Przekracza barierę krew-mózg i jest wydzielany z mlekiem MPA jest eliminowany w kale i moczu.
05.3 Przedkliniczne dane o bezpieczeństwie
Dane toksykologiczne dotyczące badań przeprowadzonych na zwierzętach doświadczalnych z użyciem octanu medroksyprogesteronu są następujące:
• LD50, podanie doustne - Mysz: powyżej 10 000 mg/kg.
• LD50, podanie dootrzewnowe – mysz: 6,985 mg/kg.
Po podaniu doustnym szczurom i myszom (334 mg/kg/dobę) oraz psom (167 mg/kg/dobę) leczonych przez 30 dni nie wykazano działania toksycznego.
Badania toksyczności przewlekłej przeprowadzone na szczurach i psach w dawkach 3, 10 i 30 mg/kg/dzień leczonych przez 6 miesięcy nie wykazały żadnych skutków toksycznych przy badanych poziomach.
Przy wyższych dawkach zaobserwowano jedynie pojawienie się oczekiwanych efektów hormonalnych.
Badania teratogenne przeprowadzone na ciężarnych psach rasy Beagle, którym podawano dawki 1, 10 i 50 mg/kg/dobę drogą doustną, ujawniły przerost łechtaczki u samic urodzonych ze zwierząt leczonych najwyższą dawką.
Nie stwierdzono żadnych nieprawidłowości u samców.
Kolejne badanie przeprowadzone w celu weryfikacji zdolności reprodukcyjnych samic urodzonych ze zwierząt leczonych octanem medroksyprogesteronu nie wykazało żadnego spadku płodności.
Długotrwałe badania toksyczności przeprowadzone na małpach, psach i szczurach po podaniu pozajelitowym octanu medroksyprogesteronu wykazały następujące działania:
1) Psy rasy Beagle, którym podawano dawki 3 i 75 mg/kg co 90 dni przez 7 lat, rozwinęły guzki sutka, które obserwowano również u niektórych zwierząt kontrolnych.
Guzki obserwowane u zwierząt kontrolnych były przerywane, podczas gdy guzki, które pojawiły się u zwierząt leczonych lekiem, były większe, liczniejsze, trwałe i u dwóch zwierząt leczonych wyższą dawką rozwinęły się złośliwe nowotwory sutka.
2) Dwie małpy, którym podawano dawkę 150 mg/kg co 90 dni przez 10 lat, rozwinął niezróżnicowany rak macicy, który nie występował u małp z grupy kontrolnej oraz u tych leczonych dawkami 3 i 30 mg / kg co 90 dni przez 10 lat.
Guzki sutka o charakterze przerywanym zaobserwowano u zwierząt z grupy kontrolnej i leczonych dawkami 3 i 30 mg/kg, ale nie w grupie, która otrzymała dawkę 150 mg/kg.
W sekcji zwłok (po 10 latach) guzki stwierdzono tylko u 3 małp z grupy leczonej dawką 30 mg/kg.
Badanie histopatologiczne wykazało, że guzki te miały charakter hiperplastyczny.
3) U szczura leczonego przez 2 lata nie było dowodów na jakiekolwiek zmiany na poziomie macicy i piersi.
Badania mutagenności przeprowadzone przy użyciu testu Salmonella Microsome (test Amesa) oraz testu Micronucleus wykazały, że octan medroksyprogesteronu nie ma działania mutagennego.
Inne badania nie wykazały żadnych zmian w płodności w pierwszym i drugim pokoleniu obserwowanych zwierząt.
Nie ustalono jeszcze, czy powyższe obserwacje można odnieść również do ludzi.
06.0 INFORMACJE FARMACEUTYCZNE
06.1 Zaróbki
makrogol 4000; polisorbat 80; parahydroksybenzoesan metylu; parahydroksybenzoesan propylu; chlorek sodu; karmeloza sodowa; woda p.p.i.
06.2 Niezgodność
Nieistotne.
06.3 Okres ważności
3 lata.
06.4 Specjalne środki ostrożności przy przechowywaniu
Ten lek nie wymaga żadnych specjalnych warunków przechowywania.
06.5 Rodzaj opakowania bezpośredniego i zawartość opakowania
Szklana butelka z gumowym korkiem i aluminiowym kapslem.
1 butelka 150 mg, 3 ml.
06.6 Instrukcje użytkowania i obsługi
Brak specjalnych instrukcji dotyczących utylizacji.
07.0 PODMIOT POZWOLENIA NA DOPUSZCZENIE DO OBROTU
Pfizer Italia S.r.l. - via Isonzo, 71 - 04100 Latina
08.0 NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
FARLUTAL 150 mg / 3 ml AIC n. . 015148075
09.0 DATA PIERWSZEGO ZEZWOLENIA LUB PRZEDŁUŻENIA ZEZWOLENIA
czerwiec 2005
10.0 DATA ZMIAN TEKSTU
Ustalenie AIFA z dnia 08.09.2015 r.