Składniki aktywne: Epoetyna alfa
Binocrit 1000 j.m./0,5 ml roztwór do wstrzykiwań w ampułko-strzykawce
Binocrit 2000 j.m./1 ml roztwór do wstrzykiwań w ampułko-strzykawce
Binocrit 3000 j.m./0,3 ml roztwór do wstrzykiwań w ampułko-strzykawce
Binocrit 4000 j.m./0,4 ml roztwór do wstrzykiwań w ampułko-strzykawce
Binocrit 5000 j.m./0,5 ml roztwór do wstrzykiwań w ampułko-strzykawce
Binocrit 6000 j.m./0,6 ml roztwór do wstrzykiwań w ampułko-strzykawce
Binocrit 7000 j.m./0,7 ml roztwór do wstrzykiwań w ampułko-strzykawce
Binocrit 8000 j.m. / 0,8 ml roztwór do wstrzykiwań w ampułko-strzykawce
Binocrit 9000 j.m. / 0,9 ml roztwór do wstrzykiwań w ampułko-strzykawce
Binocrit 10 000 j.m./1 ml roztwór do wstrzykiwań w ampułko-strzykawce
Binocrit 20 000 j.m./0,5 ml roztwór do wstrzykiwań w ampułko-strzykawce
Binocrit 30 000 j.m. / 0,75 ml roztwór do wstrzykiwań w ampułko-strzykawce
Binocrit 40 000 j.m./1 ml roztwór do wstrzykiwań w ampułko-strzykawce
Wskazania Dlaczego stosuje się Binocrit? Po co to jest?
Binocrit zawiera substancję czynną epoetynę alfa, białko, które stymuluje szpik kostny do wytwarzania większej liczby czerwonych krwinek przenoszących hemoglobinę (substancję przenoszącą tlen).
Epoetyna alfa jest kopią ludzkiego białka erytropoetyny i działa w ten sam sposób.
Binocrit stosuje się w leczeniu objawowej niedokrwistości spowodowanej chorobą nerek:
- u dzieci poddawanych hemodializie
- u osób dorosłych poddawanych hemodializie lub dializie otrzewnowej,
- u dorosłych z ciężką anemią, niepoddawanych jeszcze dializie.
Jeśli u pacjenta występuje choroba nerek, może wystąpić niedobór czerwonych krwinek, jeśli nerki nie wytwarzają wystarczającej ilości erytropoetyny (która jest niezbędna do wytwarzania czerwonych krwinek). Binocrit jest przepisywany w celu stymulowania szpiku kostnego do wytwarzania większej liczby czerwonych krwinek.
Binocrit stosuje się w leczeniu niedokrwistości podczas chemioterapii nowotworów litych, chłoniaka złośliwego lub szpiczaka mnogiego (raka szpiku kostnego) i jeśli lekarz zdecyduje, że może być konieczna transfuzja krwi.Binocrit może zmniejszyć potrzebę transfuzji krwi.
Binocrit stosuje się u osób z umiarkowaną anemią, które oddają część swojej krwi przed operacją, aby pobraną krew można było im podać w trakcie lub po operacji. Ponieważ Binocrit stymuluje produkcję czerwonych krwinek, lekarze mogą pobrać więcej krwi od tych osób.
Binocrit stosuje się u osób dorosłych z umiarkowaną niedokrwistością, które są poddawane poważnej operacji ortopedycznej (takiej jak operacja wymiany stawu biodrowego lub kolanowego) w celu zmniejszenia potencjalnej potrzeby transfuzji krwi.
Przeciwwskazania Kiedy nie należy stosować Binocrit
Nie używaj Binocrit
- jeśli pacjent ma uczulenie na epoetynę alfa lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6).
- jeśli u pacjenta rozpoznano aplazję czystej krwinek czerwonych (szpik kostny nie może wytworzyć wystarczającej ilości czerwonych krwinek) po leczeniu jakimkolwiek lekiem stymulującym wytwarzanie krwinek czerwonych (w tym Binocrit). Patrz punkt 4.
- jeśli u pacjenta występuje wysokie ciśnienie krwi, które nie jest wystarczająco kontrolowane za pomocą leków.
- w celu stymulacji produkcji czerwonych krwinek (aby lekarze mogli pobrać od ciebie więcej krwi), jeśli nie możesz otrzymać transfuzji własnej krwi podczas lub po zabiegu.
- w przypadku planowanego poważnego zabiegu ortopedycznego (takiego jak operacja stawu biodrowego lub kolanowego) oraz:
- mieć ciężką chorobę serca
- masz ciężką chorobę żył lub tętnic
- niedawno miał zawał serca lub udar mózgu
- nie może przyjmować leków rozrzedzających krew Binocrit może nie być odpowiedni dla pacjenta. Porozmawiaj o tym z lekarzem.
Niektóre osoby potrzebują leków zmniejszających ryzyko powstawania zakrzepów krwi podczas leczenia lekiem Binocrit. Jeśli pacjent nie może przyjmować leków zapobiegających powstawaniu zakrzepów krwi, nie powinien przyjmować leku Binocrit.
Środki ostrożności dotyczące stosowania Informacje ważne przed zastosowaniem leku Binocrit
Przed rozpoczęciem stosowania leku Binocrit należy omówić to z lekarzem, farmaceutą lub pielęgniarką.
Binocrit i inne produkty stymulujące wytwarzanie czerwonych krwinek mogą zwiększać ryzyko powstawania zakrzepów krwi u wszystkich pacjentów. Ryzyko to może być większe, jeśli u pacjenta występują inne czynniki ryzyka powstania zakrzepów krwi (na przykład, jeśli w przeszłości miałeś zakrzepy krwi lub jeśli masz nadwagę, cukrzycę, chorobę serca lub musisz przez jakiś czas się położyć. długotrwałe z powodu operacji lub choroby). Poinformuj swojego lekarza o każdej takiej sytuacji. Lekarz pomoże Ci zdecydować, czy Binocrit jest odpowiedni dla Ciebie.
Ważne jest, aby poinformować lekarza, jeśli którakolwiek z poniższych sytuacji dotyczy Ciebie.
Mimo to możesz być w stanie użyć Binocrit, ale najpierw musisz porozmawiać z lekarzem.
Jeśli wiesz, że cierpisz lub cierpiałeś w przeszłości z powodu:
- wysokie ciśnienie krwi;
- drgawki lub drgawki;
- choroba wątroby;
- niedokrwistość z innych przyczyn;
- porfiria (rzadka choroba krwi).
Jeśli jesteś pacjentem z rakiem, pamiętaj, że leki stymulujące produkcję czerwonych krwinek (takie jak Binocrit) mogą działać jako czynniki wzrostu, a zatem teoretycznie mogą wpływać na progresję guza.
W zależności od Twojej sytuacji osobistej, transfuzja krwi może być preferowana. Porozmawiaj o tym z lekarzem.
Jeśli pacjent choruje na wirusowe zapalenie wątroby typu C i otrzymuje interferon i rybawirynę, powinien omówić to z lekarzem, ponieważ połączenie epoetyny alfa z interferonem i rybawiryną w rzadkich przypadkach powodowało osłabienie efektu leczenia i stan zwany czystoczerwonokrwinkową aplazją ( PRCA), ciężka postać niedokrwistości. Binocrit nie jest zatwierdzony do leczenia niedokrwistości związanej z wirusowym zapaleniem wątroby typu C.
Jeśli pacjent jest pacjentem z przewlekłą niewydolnością nerek, a zwłaszcza jeśli nie reaguje odpowiednio na Binocrit, lekarz sprawdzi dawkę leku Binocrit, którą otrzymuje, ponieważ wielokrotne zwiększanie dawki leku Binocrit w przypadku braku odpowiedzi na leczenie może zwiększyć ryzyko problemów z sercem lub naczyniami krwionośnymi oraz ryzyko zawału mięśnia sercowego, udaru mózgu i zgonu.
Zachowaj szczególną ostrożność w przypadku innych produktów stymulujących produkcję czerwonych krwinek: Binocrit należy do grupy produktów, które podobnie jak ludzkie białko erytropoetyna stymulują produkcję czerwonych krwinek. Twój pracownik służby zdrowia zawsze zanotuje konkretny produkt, którego używasz.Jeśli podczas leczenia otrzymasz jakikolwiek lek z tej grupy, inny niż Binocrit, przed zastosowaniem go porozmawiaj ze swoim lekarzem lub farmaceutą.
Interakcje Jakie leki lub pokarmy mogą zmienić działanie leku Binocrit
Binocrit zwykle nie reaguje z innymi lekami, ale należy poinformować lekarza, jeśli pacjent przyjmuje, ostatnio używał lub może stosować jakiekolwiek inne leki, w tym te wydawane bez recepty.
Jeśli pacjent przyjmuje lek o nazwie cyklosporyna (stosowany na przykład po przeszczepieniu nerki), lekarz może zlecić wykonanie badań krwi w celu pomiaru stężenia cyklosporyny podczas przyjmowania leku Binocrit.
Suplementy żelaza i inne stymulanty krwi mogą zwiększyć skuteczność leku Binocrit.Twój lekarz zdecyduje, czy ich przyjmowanie jest właściwe.
Jeśli pójdziesz do szpitala, kliniki lub lekarza rodzinnego, powiedz im, że jesteś leczony lekiem Binocrit. Może to wpłynąć na inne zabiegi lub wyniki testów.
Ostrzeżenia Ważne jest, aby wiedzieć, że:
Ciąża i karmienie piersią
Ważne jest, aby poinformować lekarza, jeśli którakolwiek z poniższych sytuacji dotyczy Ciebie.
Mimo to możesz być w stanie użyć Binocrit, ale najpierw powinieneś omówić to z lekarzem:
- jeśli jesteś w ciąży lub podejrzewasz ciążę.
- jeśli karmisz piersią.
Binocrit zawiera sód
Binocrit zawiera mniej niż 1 mmol (23 mg) sodu na dawkę, co oznacza, że zasadniczo jest „wolny od sodu”.
Dawka, sposób i czas podawania Jak stosować Binocrit: dawkowanie
Lek należy zawsze stosować zgodnie z zaleceniami lekarza. W razie wątpliwości skonsultuj się z lekarzem.
Lekarz przeprowadził badanie krwi i stwierdził, że potrzebujesz Binocrit.
Binocrit można podawać we wstrzyknięciu:
- do żyły lub rurki, która wchodzi do żyły (dożylnie)
- lub pod skórą (podskórnie).
Lekarz zadecyduje o sposobie wstrzykiwania leku Binocrit. Zazwyczaj zastrzyki wykonuje lekarz, pielęgniarka lub inny pracownik służby zdrowia. Niektóre osoby, w zależności od tego, dlaczego potrzebują leczenia preparatem Binocrit, mogą później dowiedzieć się, jak wstrzykiwać go pod skórę: patrz Instrukcja samodzielnego wstrzykiwania preparatu Binocrit na końcu tej ulotki.
Binocrit nie może być używany:
- po upływie daty ważności podanej na etykiecie i opakowaniu zewnętrznym
- jeśli wiesz lub uważasz, że zostało przypadkowo zamrożone lub
- jeśli wystąpiła awaria lodówki.
Podana dawka leku Binocrit zależy od masy ciała w kilogramach. Przyczyna niedokrwistości jest również ważna dla wyboru przez lekarza odpowiedniej dawki.
Lekarz będzie regularnie kontrolował ciśnienie krwi podczas leczenia lekiem Binocrit.
Osoby z chorobą nerek
- Twój lekarz będzie utrzymywał poziom hemoglobiny między 10 a 12 g / dl, ponieważ wysoki poziom hemoglobiny może zwiększać ryzyko zakrzepów krwi i śmierci.
- Zazwyczaj stosowana dawka początkowa preparatu Binocrit u dorosłych i dzieci wynosi 50 jednostek międzynarodowych (j.m.) na kilogram (/kg) masy ciała, podawana trzy razy w tygodniu. U pacjentów poddawanych dializie otrzewnowej Binocrit można podawać dwa razy w tygodniu.
- U dorosłych i dzieci Binocrit podaje się we wstrzyknięciu do żyły (dożylnie) lub do rurki wprowadzanej do żyły.Gdy dostęp ten (przez żyłę lub rurkę) nie jest łatwo dostępny, lekarz może podjąć decyzję o wstrzyknięciu preparatu Binocrit pod skórę (podskórnie). Dotyczy to pacjentów dializowanych i pacjentów jeszcze nie dializowanych.
- Lekarz zleci regularne badania krwi, aby sprawdzić, jak niedokrwistość reaguje na leczenie, i może dostosować dawkę, zwykle najpóźniej co cztery tygodnie.
- Po ustąpieniu niedokrwistości lekarz będzie kontynuował regularne badania krwi.Dawkowanie i częstość podawania leku Binocrit może być dalej dostosowywane w celu utrzymania odpowiedzi na leczenie. Lekarz zastosuje najmniejszą skuteczną dawkę w celu kontrolowania objawów niedokrwistość. .
- Jeśli pacjent nie reaguje odpowiednio na Binocrit, lekarz sprawdzi przyjmowaną dawkę i poinformuje, czy należy zmienić dawki leku Binocrit.
- W przypadku stosowania dłuższej przerwy (większej niż raz w tygodniu) między dawkami leku Binocrit może nie być możliwe utrzymanie odpowiedniego poziomu hemoglobiny i może być konieczne zwiększenie dawki lub częstości podawania leku Binocrit.
- Możesz również otrzymywać suplementację żelazem przed iw trakcie leczenia lekiem Binocrit w celu zwiększenia skuteczności leczenia.
- Jeśli pacjent jest poddawany dializie w momencie rozpoczęcia leczenia lekiem Binocrit, może być konieczna zmiana harmonogramu dializy. Zadecyduje o tym lekarz.
Dorośli na chemioterapii
- Lekarz może rozpocząć leczenie lekiem Binocrit, jeśli stężenie hemoglobiny wynosi 10 g/dl lub mniej.
- Twój lekarz będzie utrzymywał poziom hemoglobiny między 10 a 12 g / dl, ponieważ wysoki poziom hemoglobiny może zwiększać ryzyko zakrzepów krwi i śmierci.
- Zwykle dawka początkowa wynosi 150 jm na kilogram masy ciała trzy razy w tygodniu lub 450 jm na kilogram masy ciała raz w tygodniu.
- Binocrit podaje się we wstrzyknięciu pod skórę.
- Lekarz zleci badania krwi i może dostosować dawkę w zależności od reakcji niedokrwistości na leczenie.
- Możesz również otrzymywać suplementację żelazem przed iw trakcie leczenia lekiem Binocrit w celu zwiększenia skuteczności leczenia.
- Leczenie preparatem Binocrit zwykle trwa przez jeden miesiąc po zakończeniu chemioterapii.
Dorośli, którzy oddają własną krew
- Zazwyczaj stosowana dawka to 600 jm na kilogram masy ciała, dwa razy w tygodniu.
- Binocrit podaje się we wstrzyknięciu dożylnym, bezpośrednio po oddaniu krwi, na 3 tygodnie przed zabiegiem.
- Możesz również otrzymywać suplementację żelazem przed iw trakcie leczenia lekiem Binocrit w celu zwiększenia skuteczności leczenia. Dorośli zakwalifikowani do poważnej operacji ortopedycznej
- Zalecana dawka to 600 jm na kilogram masy ciała raz w tygodniu.
- Binocrit podaje się we wstrzyknięciu podskórnym co tydzień przez trzy tygodnie przed zabiegiem iw dniu zabiegu.
- W przypadku konieczności skrócenia czasu przed zabiegiem, dawkę dobową 300 jm/kg podaje się maksymalnie 10 dni przed zabiegiem, w dniu zabiegu oraz w kolejnych 4 dniach.
- Jeśli badania krwi wykażą zbyt wysokie wartości hemoglobiny przed operacją, leczenie zostanie przerwane.
- Możesz otrzymywać suplementację żelazem przed iw trakcie leczenia lekiem Binocrit w celu zwiększenia skuteczności leczenia.
Instrukcja wstrzykiwania Binocrit pod skórę
Na początku leczenia Binocrit jest zwykle wstrzykiwany przez personel medyczny lub paramedyczny.Potem lekarz może zasugerować, aby pacjent lub jego opiekun nauczyli się samodzielnie wstrzykiwać Binocrit pod skórę (podskórnie).
- Nie należy podejmować prób samodzielnego wstrzykiwania tego leku, chyba że lekarz lub pielęgniarka pokaże, jak to zrobić.
- Binocrit należy zawsze stosować zgodnie z zaleceniami lekarza lub pielęgniarki.
- Pamiętaj, aby wstrzykiwać tylko ilość płynu wskazaną przez lekarza lub pielęgniarkę.
- Binocrit należy stosować wyłącznie po prawidłowym przechowywaniu — patrz punkt 5, Jak przechowywać Binocrit.
- Przed użyciem odstawić strzykawkę Binocrit do osiągnięcia temperatury pokojowej. Zwykle trwa to 15-30 minut. Strzykawkę należy zużyć w ciągu 3 dni od wyjęcia z lodówki.
Z każdej strzykawki należy przyjąć tylko jedną dawkę preparatu Binocrit.
Jeśli Binocrit jest wstrzykiwany pod skórę (podskórnie), wstrzykiwana objętość na ogół nie przekracza jednego mililitra (1 ml) na pojedyncze wstrzyknięcie.
Binocrit podaje się sam i nie miesza się go z innymi płynami do wstrzykiwań.
Nie potrząsać strzykawkami Binocrit. Długotrwałe energiczne potrząsanie może uszkodzić produkt.Jeśli produkt był energicznie potrząsany, nie używaj go.
Instrukcje dotyczące samodzielnego wstrzykiwania preparatu Binocrit znajdują się na końcu tej ulotki.
Pominięcie zastosowania Binocrit
Następne wstrzyknięcie należy wykonać tak szybko, jak sobie o tym przypomni.
W przypadku dalszych pytań dotyczących stosowania tego leku należy zwrócić się do lekarza, pielęgniarki lub farmaceuty.
Przedawkowanie Co zrobić w przypadku przyjęcia zbyt dużej dawki leku Binocrit
W przypadku podejrzenia, że wstrzyknięto zbyt dużą ilość leku Binocrit, należy natychmiast powiedzieć lekarzowi lub pielęgniarce. Działania niepożądane są mało prawdopodobne w przypadku przedawkowania leku Binocrit.
Skutki uboczne Jakie są skutki uboczne Binocrit?
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
W przypadku zauważenia któregokolwiek z wymienionych działań niepożądanych należy natychmiast poinformować lekarza lub pielęgniarkę.
Bardzo częste działania niepożądane
Mogą wystąpić u więcej niż 1 na 10 osób stosujących Binocrit.
- Biegunka
- Mdłości
- On wymiotował
- Gorączka
- Przekrwienie dróg oddechowych, takie jak zatkany nos i ból gardła, zgłaszano u pacjentów z chorobami nerek, którzy nie byli jeszcze poddawani dializie.
Częste skutki uboczne
Mogą dotyczyć do 1 na 10 osób stosujących Binocrit.
- Zwiększone ciśnienie krwi. Następujące objawy mogą wskazywać na nagły wzrost ciśnienia krwi: ból głowy, szczególnie w przypadku nagłego początku i typu przeszywającego podobne do migreny, splątanie lub drgawki Objawy te wymagają pilnego leczenia Wzrost ciśnienia krwi może wymagać leczenia innymi lekami (lub dostosowanie dawki leków, które już przyjmujesz na nadciśnienie).
- Zakrzepy krwi (w tym zakrzepica żył głębokich i zator), które mogą wymagać pilnej interwencji. Objawy mogą obejmować ból w klatce piersiowej, duszność i obrzęk z bólem i zaczerwienieniem, zwykle nóg.
- Kaszel.
- Wysypka skórna, która może być spowodowana reakcją alergiczną.
- Ból kości lub mięśni.
- Objawy grypopodobne, takie jak ból głowy, bóle stawów, uczucie osłabienia, dreszcze, zmęczenie i zawroty głowy. Objawy te mogą występować częściej na początku leczenia. Jeśli objawy te wystąpią podczas wstrzyknięcia dożylnego, wolniejsze wstrzyknięcie może pomóc w ich uniknięciu w przyszłości.
- Zaczerwienienie, pieczenie i ból w miejscu wstrzyknięcia.
- Obrzęk kostek, stóp lub palców.
Niezbyt częste skutki uboczne
Mogą dotyczyć do 1 na 100 osób stosujących Binocrit.
- Wysoki poziom potasu we krwi, który może prowadzić do nieprawidłowego rytmu serca (jest to bardzo częste działanie niepożądane u pacjentów dializowanych).
- Drgawki.
- Przekrwienie nosa lub dróg oddechowych.
Bardzo rzadkie skutki uboczne
Mogą dotyczyć do 1 na 10 000 osób stosujących Binocrit.
- Objawy aplazji czerwonokrwinkowej (PRCA) Wybiórcza aplazja czerwonokrwinkowa (PRCA) oznacza, że szpik kostny nie wytwarza wystarczającej ilości czerwonych krwinek. PRCA powoduje „nagłą i ciężką anemię. Objawy to:
- niezwykłe zmęczenie,
- zawroty głowy,
- duszność.
PRCA była zgłaszana bardzo rzadko, szczególnie u pacjentów z chorobą nerek, po miesiącach lub latach leczenia epoetyną alfa i innymi lekami stymulującymi wytwarzanie krwinek czerwonych.
- Szczególnie na początku leczenia może wystąpić wzrost liczby niektórych małych krwinek (zwanych płytkami krwi), które zwykle biorą udział w tworzeniu się skrzepów.Lekarz przeprowadzi odpowiednie badania.
Jeśli jesteś na hemodializie:
- W przetoce dializacyjnej mogą tworzyć się skrzepy (zakrzepica). Jest to bardziej prawdopodobne, jeśli masz niskie ciśnienie krwi lub jeśli występują powikłania związane z przetoką.
- Zakrzepy mogą również tworzyć się w systemie hemodializy. Lekarz może zdecydować o zwiększeniu dawki heparyny podczas dializy.
Należy natychmiast poinformować lekarza lub pielęgniarkę, jeśli wystąpi którykolwiek z tych objawów lub jeśli podczas przyjmowania leku Binocrit wystąpią jakiekolwiek inne objawy.
Jeśli którykolwiek z objawów niepożądanych nasili się lub wystąpią jakiekolwiek objawy niepożądane niewymienione w tej ulotce, należy poinformować o tym lekarza, pielęgniarkę lub farmaceutę.
Zgłaszanie skutków ubocznych
Jeśli wystąpią jakiekolwiek działania niepożądane, w tym wszelkie możliwe działania niepożądane niewymienione w tej ulotce, należy porozmawiać z lekarzem, farmaceutą lub pielęgniarką.Można również zgłaszać działania niepożądane bezpośrednio za pośrednictwem krajowego systemu zgłaszania wymienionego w załączniku V. działania niepożądane, którym możesz pomóc dostarczyć więcej informacji na temat bezpieczeństwa tego leku.
Wygaśnięcie i przechowywanie
- Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
- Nie stosować tego leku po upływie terminu ważności zamieszczonego na etykiecie po „EXP” i na pudełku po „EXP”.
- Przechowywać i transportować w stanie schłodzonym (2°C - 8°C).
- Binocrit można wyjąć z lodówki i przechowywać w temperaturze pokojowej (do 25°C) do 3 dni. Po wyjęciu strzykawki z lodówki i osiągnięciu temperatury pokojowej (do 25°C) należy ją zużyć w ciągu 3 dni lub wyrzucić.
- Nie zamrażać ani nie wstrząsać.
- Przechowywać w oryginalnym opakowaniu w celu ochrony leku przed światłem.
Nie stosować tego leku, jeśli zauważysz
- który został przypadkowo zamrożony lub
- że wystąpiła awaria lodówki
- że płyn jest zabarwiony lub widzi unoszące się w nim cząsteczki
- że pieczęć jest zerwana.
Nie należy wyrzucać żadnych leków do kanalizacji ani domowych pojemników na odpadki. Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa.Pomoże to chronić środowisko.
Termin ">Inne informacje
Co zawiera Binocrit
- Substancją czynną jest epoetyna alfa (ilość, patrz tabela poniżej).
- Pozostałe składniki to sodu diwodorofosforan dwuwodny, disodu fosforan dwuwodny, sodu chlorek, glicyna, polisorbat 80, kwas solny (do ustalenia pH), sodu wodorotlenek (do ustalenia pH), woda do wstrzykiwań.
Jak wygląda Binocrit i co zawiera opakowanie
Binocrit ma postać przezroczystego i bezbarwnego roztworu do wstrzykiwań w ampułko-strzykawce. Strzykawki są zamknięte w blistrach.
* Opakowania zawierające 1, 4 lub 6 ampułko-strzykawek z osłoną zabezpieczającą igłę lub bez niej.
Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
Ulotka pakietu źródłowego: AIFA (Włoska Agencja Leków). Treść opublikowana w styczniu 2016 r. Przedstawione informacje mogą być nieaktualne.
Aby mieć dostęp do najbardziej aktualnej wersji, warto wejść na stronę AIFA (Włoskiej Agencji Leków). Zastrzeżenie i przydatne informacje.
01.0 NAZWA PRODUKTU LECZNICZEGO -
ROZTWÓR BINOCRIT DO WSTRZYKIWAŃ W AMPUŁKO-STRZYKAWCE
02.0 SKŁAD JAKOŚCIOWY I ILOŚCIOWY -
Binocrit 1000 j.m./0,5 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każdy ml roztworu zawiera 2000 j.m. epoetyny alfa*, co odpowiada 16,8 mcg na ml
Jedna ampułko-strzykawka 0,5 ml zawiera 1000 jednostek międzynarodowych (j.m.), co odpowiada 8,4 mcg epoetyny alfa. *
Binocrit 2000 j.m./1 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każdy ml roztworu zawiera 2000 j.m. epoetyny alfa*, co odpowiada 16,8 mcg na ml
Jedna ampułko-strzykawka o pojemności 1 ml zawiera 2000 jednostek międzynarodowych (j.m.), co odpowiada 16,8 mcg epoetyny alfa. *
Binocrit 3000 j.m./0,3 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każdy ml roztworu zawiera 10 000 j.m. epoetyny alfa*, co odpowiada 84,0 mcg na ml
Jedna ampułko-strzykawka 0,3 ml zawiera 3000 jednostek międzynarodowych (j.m.), co odpowiada 25,2 mcg epoetyny alfa. *
Binocrit 4000 j.m./0,4 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każdy ml roztworu zawiera 10 000 j.m. epoetyny alfa*, co odpowiada 84,0 mcg na ml
Jedna ampułko-strzykawka o pojemności 0,4 ml zawiera 4000 jednostek międzynarodowych (j.m.), co odpowiada 33,6 mcg epoetyny alfa. *
Binocrit 5000 j.m./0,5 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każdy ml roztworu zawiera 10 000 j.m. epoetyny alfa*, co odpowiada 84,0 mcg na ml
Jedna ampułko-strzykawka 0,5 ml zawiera 5000 jednostek międzynarodowych (j.m.), co odpowiada 42,0 mcg epoetyny alfa. *
Binocrit 6000 j.m./0,6 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każdy ml roztworu zawiera 10 000 j.m. epoetyny alfa*, co odpowiada 84,0 mcg na ml
Jedna 0,6 ml ampułko-strzykawka zawiera 6000 jednostek międzynarodowych (j.m.), co odpowiada 50,4 mcg epoetyny alfa. *
Binocrit 7000 j.m./0,7 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każdy ml roztworu zawiera 10 000 j.m. epoetyny alfa*, co odpowiada 84,0 mcg na ml
Jedna ampułko-strzykawka o pojemności 0,7 ml zawiera 7000 jednostek międzynarodowych (j.m.), co odpowiada 58,8 mcg epoetyny alfa. *
Binocrit 8000 j.m. / 0,8 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każdy ml roztworu zawiera 10 000 j.m. epoetyny alfa*, co odpowiada 84,0 mcg na ml
Jedna ampułko-strzykawka 0,8 ml zawiera 8000 jednostek międzynarodowych (j.m.), co odpowiada 67,2 mcg epoetyny alfa. *
Binocrit 9000 j.m. / 0,9 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każdy ml roztworu zawiera 10 000 j.m. epoetyny alfa*, co odpowiada 84,0 mcg na ml
Jedna ampułko-strzykawka o pojemności 0,9 ml zawiera 9000 jednostek międzynarodowych (j.m.), co odpowiada 75,6 mcg epoetyny alfa. *
Binocrit 10 000 j.m./1 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każdy ml roztworu zawiera 10 000 j.m. epoetyny alfa*, co odpowiada 84,0 mcg na ml
Jedna ampułko-strzykawka o pojemności 1 ml zawiera 10 000 jednostek międzynarodowych (j.m.), co odpowiada 84,0 mcg epoetyny alfa. *
Binocrit 20 000 j.m./0,5 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każdy ml roztworu zawiera 40 000 j.m. epoetyny alfa*, co odpowiada 336,0 mcg na ml
Jedna ampułko-strzykawka 0,5 ml zawiera 20 000 jednostek międzynarodowych (j.m.), co odpowiada 168,0 mcg epoetyny alfa. *
Binocrit 30 000 j.m. / 0,75 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każdy ml roztworu zawiera 40 000 j.m. epoetyny alfa*, co odpowiada 336,0 mcg na ml
Jedna 0,75 ml ampułko-strzykawka zawiera 30 000 jednostek międzynarodowych (j.m.), co odpowiada 252,0 mcg epoetyny alfa. *
Binocrit 40 000 j.m./1 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każdy ml roztworu zawiera 40 000 j.m. epoetyny alfa*, co odpowiada 336,0 mcg na ml
Jedna ampułko-strzykawka o pojemności 1 ml zawiera 40 000 jednostek międzynarodowych (j.m.), co odpowiada 336,0 mcg epoetyny alfa. *
* Wytwarzany w komórkach jajnika chomika chińskiego (CHO) przy użyciu technologii rekombinacji DNA
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
Ten produkt leczniczy zawiera mniej niż 1 mmol (23 mg) sodu na dawkę, co oznacza, że zasadniczo jest „wolny od sodu”.
03.0 POSTAĆ FARMACEUTYCZNA -
Roztwór do wstrzykiwań w ampułko-strzykawce (wstrzyknięcie)
Przejrzysty i bezbarwny roztwór
04.0 INFORMACJE KLINICZNE -
04.1 Wskazania terapeutyczne -
Binocrit jest wskazany w leczeniu objawowej niedokrwistości związanej z przewlekłą niewydolnością nerek (CRI):
• w hemodializie dorośli i dzieci w wieku od 1 do 18 lat oraz dorośli pacjenci poddawani dializie otrzewnowej (patrz punkt 4.4).
• u dorosłych pacjentów z niewydolnością nerek niepoddawanych jeszcze dializie w leczeniu ciężkiej niedokrwistości pochodzenia nerkowego z towarzyszącymi objawami klinicznymi (patrz punkt 4.4).
Binocrit jest wskazany do stosowania u osób dorosłych otrzymujących chemioterapię z powodu guzów litych, chłoniaka złośliwego lub szpiczaka mnogiego, u których występuje ryzyko transfuzji, na co wskazuje stan ogólny pacjenta (sytuacja sercowo-naczyniowa, wcześniej występująca niedokrwistość na początku chemioterapii) w leczeniu niedokrwistości i zmniejszania wymagania dotyczące transfuzji.
Binocrit jest wskazany u osób dorosłych, które biorą udział w programie autologicznego przetoczenia w celu zwiększenia wytwarzania krwi autologicznej. Leczenie należy prowadzić wyłącznie u pacjentów z umiarkowaną niedokrwistością (zakres stężenia hemoglobiny [Hb] od 10 do 13 g/dl [6,2 do 8,1 mmol/l], bez niedoboru żelaza), gdy techniki oszczędzania krwi nie są dostępne lub niewystarczające i planowane duża planowa operacja wymaga dużej ilości krwi (4 lub więcej jednostek krwi dla kobiet, 5 lub więcej jednostek dla mężczyzn).
Binocrit jest wskazany u osób dorosłych bez niedoboru żelaza, u których uważa się, że istnieje wysokie ryzyko powikłań po przetoczeniu, przed dużymi planowymi zabiegami ortopedycznymi, w celu zmniejszenia narażenia na przetoczenia krwi allogenicznej. g / dl lub między 6,2 a 8,1 mmol / l) nie jest częścią programu autologicznego przetoczenia iw przypadku którego oczekuje się umiarkowanej utraty krwi (900-1800 ml).
04.2 Dawkowanie i sposób podawania -
Terapię produktem Binocrit należy rozpoczynać pod nadzorem lekarzy doświadczonych w leczeniu pacjentów z powyższymi wskazaniami.
Dawkowanie
Wszystkie inne przyczyny niedokrwistości (niedobór żelaza, kwasu foliowego lub witaminy B12, zatrucie glinem, zakażenie lub stan zapalny, utrata krwi, hemoliza i zwłóknienie szpiku kostnego dowolnego pochodzenia) należy ocenić i leczyć przed rozpoczęciem leczenia epoetyną alfa i przy podejmowaniu decyzji o zwiększenie dawki. Aby zapewnić optymalną odpowiedź na epoetynę alfa, konieczne jest zapewnienie odpowiednich zapasów żelaza oraz, w razie potrzeby, podawanie suplementu żelaza (patrz punkt 4.4).
Leczenie objawowej niedokrwistości u dorosłych pacjentów z przewlekłą niewydolnością nerek
Objawy i konsekwencje niedokrwistości mogą się różnić w zależności od wieku, płci i chorób współistniejących, lekarz wymaga indywidualnej oceny przebiegu klinicznego i stanu każdego pacjenta.
Zalecany pożądany zakres stężenia hemoglobiny wynosi od 10 g/dl do 12 g/dl (6,2 do 7,5 mmol/l).Binocrit należy podawać tak, aby wartości hemoglobiny nie wzrosły powyżej 12 g/dl (7,5 mmol/l). Należy unikać wzrostu stężenia hemoglobiny o więcej niż 2 g/dl (1,25 mmol/l) w ciągu kilku tygodni.W takim przypadku należy odpowiednio dostosować dawkę.
Ze względu na zmienność wewnątrzosobniczą, indywidualne wartości hemoglobiny powyżej i poniżej pożądanego zakresu stężenia hemoglobiny mogą czasami być obserwowane: 10 g/dl (6,2 mmol/l) i 12 g/dl (7,5 mmol/l).
Należy unikać przedłużonego poziomu hemoglobiny powyżej 12 g/dl (7,5 mmol/l). Jeśli stężenie hemoglobiny wzrośnie o więcej niż 2 g/dl (1,25 mmol/l) miesięcznie lub jeśli poziom hemoglobiny utrzymuje się powyżej 12 g/dl (7,5 mmol/l), zmniejsz dawkę preparatu Binocrit o 25%. 13 g/dl (8,1 mmol/l), przerwać terapię do momentu spadku wartości poniżej 12 g/dl (7,5 mmol/l), a następnie wznowić leczenie preparatem Binocrit w dawce o 25% niższej niż poprzednia dawka.
Pacjentów należy ściśle monitorować, aby upewnić się, że najniższa zatwierdzona skuteczna dawka preparatu Binocrit jest stosowana do odpowiedniej kontroli niedokrwistości i objawów niedokrwistości, przy jednoczesnym utrzymaniu stężenia hemoglobiny poniżej lub równego 12 g/dl (7,45 mmol/l).
Należy zachować ostrożność podczas zwiększania dawek preparatu Binocrit u pacjentów z przewlekłą niewydolnością nerek.U pacjentów ze słabą odpowiedzią hemoglobiny na produkt Binocrit należy rozważyć alternatywne wyjaśnienia słabej odpowiedzi (patrz punkty 4.4 i 5.1).
Leczenie preparatem Binocrit składa się z dwóch faz: fazy korekcji i fazy podtrzymującej.
Dorośli pacjenci poddawani hemodializie
U pacjentów poddawanych hemodializie, u których dostęp dożylny jest łatwo dostępny, preferowane jest podawanie dożylne.
Faza korekty
Dawka początkowa to 50 jm/kg, trzy razy w tygodniu.
W razie potrzeby zwiększ lub zmniejsz dawkę o 25 j.m./kg (trzy razy w tygodniu), aż do osiągnięcia pożądanego zakresu stężenia hemoglobiny, od 10 g/dl do 12 g/dl (od 6,2 do 7,5 mmol/l) (powinno to następować stopniowo w odstępach co najmniej czterech tygodni).
Faza konserwacji
Zalecana całkowita dawka tygodniowa wynosi od 75 j.m./kg do 300 j.m./kg.
Należy odpowiednio dostosować dawkę, aby utrzymać wartości hemoglobiny w pożądanym zakresie stężeń od 10 g/dl do 12 g/dl (6,2 do 7,5 mmol/l).
Pacjenci z początkowo bardzo niskimi wartościami hemoglobiny (8 g/dL lub >5 mmol/L).
Dorośli pacjenci z niewydolnością nerek niepoddani jeszcze dializie
Jeżeli dostęp dożylny nie jest łatwo dostępny, Binocrit można podawać podskórnie.
Faza korekty
Dawka początkowa 50 j.m./kg 3 razy w tygodniu, a następnie, jeśli to konieczne, zwiększaj ją o 25 j.m./kg (3 razy w tygodniu) aż do osiągnięcia pożądanej wartości (należy to robić stopniowo w odstępach co najmniej czterech tygodni ).
Faza konserwacji
W fazie podtrzymującej Binocrit można podawać 3 razy w tygodniu lub, w przypadku podawania podskórnego, raz w tygodniu lub raz na 2 tygodnie.
Należy odpowiednio dostosować dawki i odstępy między dawkami, aby utrzymać wartości hemoglobiny na pożądanym poziomie: hemoglobina między 10 g/dl a 12 g/dl (6,2 do 7,5 mmol/l). Wydłużenie odstępu między dawkami może wymagać zwiększenia dawki.
Maksymalna dawka nie powinna przekraczać 150 jm/kg 3 razy w tygodniu, 240 jm/kg (maksymalnie 20 000 jm) raz w tygodniu lub 480 jm/kg (maksymalnie 40 000 jm) raz co 2 tygodni.
Dorośli pacjenci poddawani dializie otrzewnowej
Jeżeli dostęp dożylny nie jest łatwo dostępny, Binocrit można podawać podskórnie.
Faza korekty
Dawka początkowa to 50 jm/kg, dwa razy w tygodniu.
Faza konserwacji
Zalecana dawka podtrzymująca wynosi od 25 jm/kg do 50 jm/kg dwa razy w tygodniu w 2 równych wstrzyknięciach.
Należy odpowiednio dostosować dawkę, aby utrzymać wartości hemoglobiny na pożądanym poziomie, między 10 g/dl a 12 g/dl (6,2 do 7,5 mmol/l).
Leczenie dorosłych pacjentów z niedokrwistością wywołaną chemioterapią
Objawy i konsekwencje niedokrwistości mogą się różnić w zależności od wieku, płci i ogólnego nasilenia choroby, lekarz wymaga indywidualnej oceny przebiegu klinicznego i stanu każdego pacjenta.
Binocrit należy podawać pacjentom z niedokrwistością (np. ze stężeniem hemoglobiny ≤ 10 g/dl (6,2 mmol/l)).
Dawka początkowa wynosi 150 jm/kg podskórnie, 3 razy w tygodniu.
Alternatywnie Binocrit można podawać w dawce początkowej 450 j.m./kg podskórnie raz w tygodniu.
Należy odpowiednio dostosować dawkę, aby utrzymać wartości hemoglobiny w pożądanym zakresie stężeń od 10 g/dl do 12 g/dl (6,2 do 7,5 mmol/l).
Ze względu na zmienność wewnątrzosobniczą pojedyncze stężenia hemoglobiny powyżej i poniżej pożądanego zakresu stężenia hemoglobiny mogą czasami być obserwowane.Zaleca się, aby zmienność stężenia hemoglobiny rozwiązać poprzez optymalne zarządzanie dawką, biorąc pod uwagę zakres stężenia hemoglobiny.10 g / dl (6,2 mmol/l) do pożądanego poziomu 12 g/dl (7,5 mmol/l) Należy unikać przedłużonego stężenia hemoglobiny powyżej 12 g/dl (7,5 mmol/l); wytyczne dotyczące odpowiedniego dostosowania dawki dla stężenia hemoglobiny powyżej 12 g/dl (7,5 mmol) / L) są opisane poniżej.
• Czy stężenie hemoglobiny wzrosło o co najmniej 1 g/dl (0,62 mmol/l) lub liczba retikulocytów wzrosła o? 40 000 komórek/mcL powyżej wartości wyjściowych po czterech tygodniach leczenia należy utrzymać dawkę 150 jm/kg trzy razy w tygodniu lub 450 jm/kg raz w tygodniu.
• Jeśli wzrost stężenia hemoglobiny wynosi
• Jeśli wzrost stężenia hemoglobiny wynosi
Dostosowanie dawki w celu utrzymania stężenia hemoglobiny między 10 g/dl a 12 g/dl (6,2 i 7,5 mmol/l)
Jeśli stężenie hemoglobiny wzrośnie o więcej niż 2 g/dl (1,25 mmol/l) miesięcznie lub jeśli poziom stężenia hemoglobiny przekroczy 12 g/dl (7,5 mmol/l), zmniejsz dawkę Binocrit o około 25-50%.
Jeżeli stężenie hemoglobiny przekroczy 13 g/dl (8,1 mmol/l), należy przerwać terapię do momentu spadku wartości poniżej 12 g/dl (7,5 mmol/l), a następnie wznowić leczenie preparatem Binocrit w dawce o 25% niższej niż poprzednia dawka.
Zalecany schemat dawkowania przedstawiono w poniższej tabeli:
Pacjenci powinni być ściśle monitorowani, aby upewnić się, że najniższa zatwierdzona dawka środka stymulującego erytropoezę (środek stymulujący erytropoezę, ESA) w celu odpowiedniej kontroli objawów niedokrwistości.
Terapię epoetyną alfa należy kontynuować do miesiąca po zakończeniu chemioterapii.
Leczenie dorosłych pacjentów chirurgicznych uczestniczących w programie autologicznej predoncji
Pacjenci z łagodną niedokrwistością (hematokryt od 33 do 39%), którzy wymagają wstępnego odłożenia 4 lub więcej jednostek krwi, powinni być leczeni dożylnie 600 jm/kg Binocrit, dwa razy w tygodniu przez trzy tygodnie przed zabiegiem. Binocrit należy podawać po zakończeniu procedury dawstwa.
Leczenie dorosłych pacjentów zakwalifikowanych do poważnej planowej operacji ortopedycznej
Zalecana dawka to 600 j.m./kg Binocrit, podawana podskórnie raz w tygodniu przez trzy tygodnie (dni -21, -14 i -7) przed zabiegiem oraz w dniu zabiegu (dzień 0).
W przypadkach, gdy ze względów medycznych konieczne jest skrócenie czasu do zabiegu do mniej niż trzech tygodni, należy podać podskórnie 300 jm/kg Binocrit przez 10 kolejnych dni przed zabiegiem, w dniu zabiegu oraz w czterech dni bezpośrednio po.
Jeśli poziom hemoglobiny osiągnie lub przekroczy 15 g/dl (9,38 mmol/l) w okresie przedoperacyjnym, należy odstawić Binocrit i nie podawać kolejnych dawek.
Populacja pediatryczna
Leczenie objawowej niedokrwistości u pacjentów z przewlekłą niewydolnością nerek poddawanych hemodializie
Objawy i konsekwencje niedokrwistości mogą się różnić w zależności od wieku, płci i chorób współistniejących, lekarz wymaga indywidualnej oceny przebiegu klinicznego i stanu każdego pacjenta.
U pacjentów pediatrycznych zalecany zakres stężenia hemoglobiny wynosi od 9,5 g/dl do 11 g/dl (5,9 do 6,8 mmol/l).Binocrit należy podawać tak, aby wartości hemoglobiny nie wzrosły powyżej 11 g/dl (6,8 mmol/l). Należy unikać wzrostu stężenia hemoglobiny o więcej niż 2 g/dl (1,25 mmol/l) w okresie czterech tygodni i odpowiednio dostosować dawkę.
Pacjentów należy ściśle monitorować, aby upewnić się, że do odpowiedniej kontroli niedokrwistości i objawów niedokrwistości stosowana jest najniższa zatwierdzona dawka preparatu Binocrit.
Leczenie preparatem Binocrit składa się z dwóch faz: fazy korekcji i fazy podtrzymującej.
U pacjentów pediatrycznych poddawanych hemodializie, u których dostęp dożylny jest łatwo dostępny, preferowane jest podawanie dożylne.
Faza korekty
Dawka początkowa wynosi 50 jm/kg dożylnie, 3 razy w tygodniu.
W razie potrzeby zwiększ lub zmniejsz dawkę o 25 j.m./kg (trzy razy w tygodniu), aż do osiągnięcia pożądanego zakresu stężenia hemoglobiny, od 9,5 g/dl do 11 g/dl (od 5,9 do 6, 8 mmol/l) ( należy to robić stopniowo w odstępach co najmniej czterech tygodni).
Faza konserwacji
Należy odpowiednio dostosować dawkę, aby utrzymać stężenie hemoglobiny w pożądanym zakresie stężeń od 9,5 g/dl do 11 g/dl (5,9 do 6,8 mmol/l).
Zazwyczaj dzieci o masie ciała poniżej 30 kg wymagają wyższych dawek podtrzymujących niż dzieci o masie ciała powyżej 30 kg i dorośli.
Pacjenci pediatryczni z bardzo niskimi wyjściowymi wartościami hemoglobiny (6,8 g/dL lub >4,25 mmol/L).
Niedokrwistość u pacjentów z przewlekłą niewydolnością nerek przed rozpoczęciem dializy lub poddaniem się dializie otrzewnowej
Nie ustalono bezpieczeństwa i skuteczności stosowania epoetyny alfa u pacjentów z przewlekłą niewydolnością nerek i niedokrwistością przed rozpoczęciem dializy lub poddawanych dializie otrzewnowej. Obecnie dostępne dane dotyczące podskórnego stosowania epoetyny alfa w tych populacjach opisano w punkcie 5.1, ale nie można sformułować zaleceń dotyczących dawkowania.
Leczenie dzieci i młodzieży z niedokrwistością wywołaną chemioterapią
Nie ustalono bezpieczeństwa i skuteczności epoetyny alfa u dzieci poddawanych chemioterapii (patrz punkt 5.1).
Leczenie pediatrycznych pacjentów chirurgicznych uczestniczących w programie autologicznej predoncji
Nie określono bezpieczeństwa stosowania ani skuteczności epoetyny alfa u dzieci i młodzieży Brak dostępnych danych.
Leczenie pacjentów pediatrycznych oczekujących na duży planowy zabieg ortopedyczny
Nie określono bezpieczeństwa stosowania ani skuteczności epoetyny alfa u dzieci i młodzieży Brak dostępnych danych.
Sposób podawania
Środki ostrożności, które należy podjąć przed użyciem lub podaniem produktu leczniczego.
Przed użyciem odstawić strzykawkę Binocrit do osiągnięcia temperatury pokojowej, co zwykle zajmuje 15-30 minut.
Podobnie jak w przypadku wszystkich innych produktów do wstrzykiwania, należy sprawdzić, czy roztwór nie zawiera cząstek i nie wykazuje żadnych przebarwień. Binocrit to sterylny, ale niezakonserwowany produkt, przeznaczony wyłącznie do jednorazowego użytku. Podaj wymaganą ilość.
Leczenie objawowej niedokrwistości u dorosłych pacjentów z przewlekłą niewydolnością nerek
U pacjentów z przewlekłą niewydolnością nerek, u których dostęp dożylny jest regularnie dostępny (pacjenci poddawani hemodializie), preferowane jest podawanie dożylne produktu Binocrit.
Jeżeli dostęp dożylny nie jest łatwo dostępny (pacjenci jeszcze nie poddawani dializie i pacjenci poddawani dializie otrzewnowej) Binocrit można podawać we wstrzyknięciu podskórnym.
Leczenie dorosłych pacjentów z niedokrwistością wywołaną chemioterapią
Binocrit należy podawać we wstrzyknięciu podskórnym.
Leczenie dorosłych pacjentów chirurgicznych uczestniczących w programie autologicznej predoncji
Binocrit należy podawać dożylnie.
Leczenie dorosłych pacjentów zakwalifikowanych do poważnej planowej operacji ortopedycznej
Binocrit należy podawać we wstrzyknięciu podskórnym.
Leczenie objawowej niedokrwistości u dzieci i młodzieży z przewlekłą niewydolnością nerek poddawanych hemodializie
U dzieci i młodzieży z przewlekłą niewydolnością nerek, u których dostęp dożylny jest regularnie dostępny (pacjenci poddawani hemodializie), preferowane jest podawanie dożylne produktu Binocrit.
Podawanie dożylne
Podawać przez co najmniej jedną do pięciu minut, w zależności od całkowitej dawki. U pacjentów hemodializowanych bolus można podać podczas sesji dializy przez odpowiedni dostęp żylny w linii dializacyjnej. Alternatywnie, wstrzyknięcie można wykonać pod koniec sesji dializy przez rurkę z igłą do przetoki, a następnie 10 ml izotonicznego roztworu soli fizjologicznej w celu przepłukania rurki i zapewnienia wstrzyknięcia produktu do krążenia (patrz Dawkowanie, „Dorośli pacjenci poddawani hemodializie”). ).
U pacjentów reagujących na leczenie objawami grypopodobnymi preferowane jest wolniejsze podawanie (patrz punkt 4.8).
Nie podawać leku Binocrit we wlewie dożylnym lub w skojarzeniu z innymi produktami leczniczymi w roztworze (więcej informacji znajduje się w punkcie 6.6).
Podanie podskórne
Nie przekraczać maksymalnej objętości 1 ml w każdym miejscu wstrzyknięcia.W celu wstrzyknięcia większej objętości należy użyć wielu miejsc wstrzyknięcia.
Wstrzyknąć w kończyny lub przednią ścianę brzucha.
W przypadkach, gdy lekarz stwierdzi, że pacjent lub jego opiekun mogą samodzielnie bezpiecznie i skutecznie podawać Binocrit podskórnie, należy udzielić wskazówek dotyczących prawidłowego dawkowania i sposobu podawania.
„Instrukcję samodzielnego wstrzykiwania preparatu Binocrit” można znaleźć na końcu ulotki dołączonej do opakowania.
04.3 Przeciwwskazania -
• Nadwrażliwość na substancję czynną lub na którąkolwiek substancję pomocniczą wymienioną w punkcie 6.1.
• Nie należy podawać preparatu Binocrit ani żadnej innej erytropoetyny pacjentom, u których po leczeniu jakąkolwiek erytropoetyną rozwinęła się aplazja czysto czerwonokrwinkowa (PRCA) (patrz punkt 4.4).
• Niekontrolowane nadciśnienie.
• U pacjentów otrzymujących suplement Binocrit należy przestrzegać wszystkich przeciwwskazań związanych z programami autologicznego przetoczenia krwi.
Stosowanie preparatu Binocrit u pacjentów zakwalifikowanych do dużych planowych operacji ortopedycznych, którzy nie uczestniczą w programie autologicznego przetoczenia krwi, jest przeciwwskazane u pacjentów z ciężką chorobą naczyń wieńcowych, obwodowych, szyjnych lub mózgowych, w tym u pacjentów po niedawno przebytym zawale mięśnia sercowego lub udarach mózgowo-naczyniowych .
• Pacjenci chirurgiczni, którzy z jakiegokolwiek powodu nie mogą otrzymać odpowiedniej profilaktyki przeciwzakrzepowej.
04.4 Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania -
Uwagi ogólne
U pacjentów leczonych epoetyną alfa ciśnienie krwi należy ściśle monitorować i kontrolować w razie potrzeby. Epoetynę alfa należy stosować ostrożnie w przypadku nieleczonego, niewłaściwie leczonego lub słabo kontrolowanego nadciśnienia tętniczego. Może zaistnieć potrzeba dodania produktów leczniczych o zwiększenie dawki leczenia przeciwnadciśnieniowego Przerwać leczenie epoetyną alfa, jeśli nie można kontrolować ciśnienia krwi.
Kryzysy nadciśnieniowe z encefalopatią i napady padaczkowe wymagające natychmiastowej pomocy lekarskiej i intensywnej opieki również występowały podczas leczenia epoetyną alfa pacjentów z poprzednio prawidłowym lub niskim ciśnieniem krwi.
Epoetynę alfa należy stosować ostrożnie u pacjentów z padaczką, napadami drgawkowymi w wywiadzie lub stanami chorobowymi związanymi z predyspozycją do napadów drgawkowych, takimi jak zakażenia OUN i przerzuty do mózgu.
Epoetynę alfa należy stosować ostrożnie u pacjentów z przewlekłą niewydolnością wątroby.Bezpieczeństwo stosowania epoetyny alfa u pacjentów z zaburzeniami czynności wątroby nie zostało ustalone.
U pacjentów leczonych ESA (patrz punkt 4.8) obserwowano zwiększoną częstość występowania zakrzepicy naczyń (VTE). Obejmują one zakrzepicę i zator żył i tętnic (w tym niektóre przypadki zakończone zgonem), takie jak zakrzepica żył głębokich, zator tętnicy płucnej , zakrzepica siatkówki i zawał mięśnia sercowego Ponadto zgłaszano incydenty naczyniowo-mózgowe (w tym zawał mózgu, krwotok mózgowy i napady przemijającego niedokrwienia).
Zgłaszane ryzyko wystąpienia tych ŻChZZ należy starannie rozważyć w stosunku do oczekiwanych korzyści z leczenia epoetyną alfa, szczególnie u pacjentów z istniejącymi wcześniej czynnikami ryzyka ŻChZZ, w tym otyłością i przebytą ŻChZZ (np. zakrzepicą żył głębokich, zatorowością płucną i incydentem naczyniowym mózgu). .
U wszystkich pacjentów należy ściśle monitorować stężenie hemoglobiny ze względu na potencjalnie wyższe ryzyko wystąpienia zdarzeń zakrzepowo-zatorowych i zgonu, jeśli pacjenci są leczeni przy stężeniach hemoglobiny powyżej zakresu stężeń wskazania.
Podczas leczenia epoetyną alfa może wystąpić umiarkowany, zależny od dawki wzrost liczby płytek krwi w prawidłowym zakresie. Ten wzrost ustępuje w trakcie kontynuowania leczenia. Ponadto zgłaszano nadpłytkowość powyżej normy. Zaleca się. liczba monitorowana regularnie w ciągu pierwszych ośmiu tygodni terapii.
Wszystkie inne przyczyny niedokrwistości (niedobór żelaza, kwasu foliowego lub witaminy B12, zatrucie glinem, zakażenie lub stan zapalny, utrata krwi, hemoliza i zwłóknienie szpiku kostnego dowolnego pochodzenia) należy ocenić i leczyć przed rozpoczęciem leczenia epoetyną alfa i przy podejmowaniu decyzji o zwiększenie dawki. W większości przypadków wartości ferrytyny w surowicy spadają wraz ze wzrostem hematokrytu. Aby zapewnić optymalną odpowiedź na epoetynę alfa, konieczne jest zapewnienie odpowiednich zapasów żelaza oraz, w razie potrzeby, podanie suplementu żelaza (patrz punkt 4.2):
• U pacjentów z przewlekłą niewydolnością nerek zaleca się podawanie żelaza (żelazo pierwiastkowe, 200 do 300 mg/dobę doustnie u dorosłych i 100 do 200 mg/dobę doustnie u dzieci), jeśli stężenie ferrytyny w surowicy jest mniejsze niż 100 ng/ml.
• U pacjentów z rakiem zaleca się podawanie żelaza (żelazo pierwiastkowe, 200 do 300 mg/dobę doustnie), jeśli wysycenie transferyny jest mniejsze niż 20%.
• U pacjentów biorących udział w programie przetoczenia autologicznego podanie żelaza (żelazo pierwiastkowe, 200 mg/dobę doustnie) musi nastąpić na kilka tygodni przed rozpoczęciem przetoczenia autologicznego, w celu wytworzenia obfitych złogów żelaza przed rozpoczęciem leczenia epoetyną alfa i przez cały okres leczenia epoetyną alfa.
• U pacjentów zakwalifikowanych do dużych planowych operacji ortopedycznych podawanie żelaza (żelazo pierwiastkowe, 200 mg/dobę doustnie) powinno odbywać się przez cały czas trwania leczenia epoetyną alfa.Jeśli to możliwe, podawanie żelaza należy rozpocząć przed rozpoczęciem leczenia epoetyną alfa aby powstały odpowiednie zapasy żelaza.
Bardzo rzadko wystąpienie lub zaostrzenie porfirii obserwowano u pacjentów leczonych epoetyną alfa.Epoetynę alfa należy stosować ostrożnie u pacjentów z porfirią.
Aby poprawić identyfikowalność środków stymulujących erytropoezę (ESA), nazwa podawanego środka musi być zarejestrowana (lub wskazana) jednoznacznie w dokumentacji medycznej pacjenta.
Pacjenci powinni przechodzić z jednego ESA na inny tylko pod odpowiednim nadzorem.
Aplazja czystej krwinek czerwonych (PRCA)
PRCA zależna od przeciwciał była zgłaszana po miesiącach lub latach podskórnego leczenia epoetyną, głównie u pacjentów z przewlekłą niewydolnością nerek. Zgłaszano również przypadki u pacjentów z wirusowym zapaleniem wątroby typu C leczonych interferonem i rybawiryną w przypadku jednoczesnego leczenia ESA. Epoetyna alfa nie jest zatwierdzona do leczenia niedokrwistości związanej z wirusowym zapaleniem wątroby typu C.
U pacjentów, u których nagle występuje brak skuteczności terapii, określany spadkiem hemoglobiny (1-2 g/dl lub 0,62-1,25 mmol/l na miesiąc) przy zwiększonym zapotrzebowaniu na transfuzję, należy określić liczbę retikulocytów i typową należy przeanalizować przyczyny braku odpowiedzi (niedobór żelaza, kwasu foliowego lub witaminy B12, zatrucie glinem, zakażenie lub stan zapalny, utrata krwi, hemoliza i zwłóknienie szpiku kostnego dowolnego pochodzenia).
W przypadku paradoksalnego zmniejszenia stężenia hemoglobiny i wystąpienia ciężkiej niedokrwistości związanej z małą liczbą retikulocytów należy przerwać leczenie epoetyną alfa i określić przeciwciała przeciw erytropoetynie. Należy również rozważyć badanie szpiku kostnego w celu „możliwego rozpoznania PRCA.
Nie należy rozpoczynać innych terapii ESA ze względu na ryzyko reakcji krzyżowej.
Leczenie objawowej niedokrwistości u dorosłych i dzieci z przewlekłą niewydolnością nerek
U pacjentów z przewlekłą niewydolnością nerek leczonych epoetyną alfa, poziom hemoglobiny należy regularnie mierzyć do osiągnięcia stabilnego poziomu, a następnie w okresowych odstępach czasu.
U pacjentów z przewlekłą niewydolnością nerek wzrost stężenia hemoglobiny powinien wynosić około 1 g/dl (0,62 mmol/l) na miesiąc i nie powinien przekraczać 2 g/dl (1,25 mmol/l) na miesiąc, aby zminimalizować ryzyko pogorszenia nadciśnienia.
U pacjentów z przewlekłą niewydolnością nerek podtrzymujące stężenie hemoglobiny nie powinno przekraczać górnej granicy zakresu stężenia hemoglobiny, jak zalecono w punkcie 4.2.W badaniach klinicznych obserwowano zwiększone ryzyko zgonu i poważnych zdarzeń sercowo-naczyniowych. poziom stężenia hemoglobiny powyżej 12 g/dL (7,5 mmol/L).
Kontrolowane badania kliniczne nie wykazały znaczących korzyści związanych z podawaniem epoetyn, gdy stężenie hemoglobiny przekroczyło poziomy niezbędne do kontrolowania objawów niedokrwistości i uniknięcia transfuzji krwi.
Należy zachować ostrożność przy zwiększaniu dawek preparatu Binocrit u pacjentów z przewlekłą niewydolnością nerek, ponieważ duże skumulowane dawki epoetyny mogą wiązać się ze zwiększonym ryzykiem zgonu oraz poważnych zdarzeń sercowo-naczyniowych i mózgowo-naczyniowych.U pacjentów ze słabą odpowiedzią hemoglobiny na epoetyny. należy wziąć pod uwagę słabą odpowiedź (patrz punkty 4.2 i 5.1).
Pacjenci z przewlekłą niewydolnością nerek leczeni podskórnie epoetyną alfa powinni być okresowo monitorowani pod kątem utraty skuteczności, definiowanej jako brak lub zmniejszona odpowiedź na leczenie epoetyną alfa u pacjentów, którzy wcześniej odpowiedzieli na takie leczenie. Ten stan charakteryzuje się przedłużonym spadkiem stężenia hemoglobiny pomimo zwiększenia dawki epoetyny alfa (patrz punkt 4.8).
Niektórzy pacjenci stosujący dłuższe odstępy między dawkami epoetyny alfa (większe niż raz w tygodniu) mogą nie utrzymywać odpowiedniego poziomu hemoglobiny (patrz punkt 5.1) i mogą wymagać zwiększenia dawki epoetyny alfa. Poziom hemoglobiny należy regularnie monitorować.
Zakrzepica przetoki występowała u pacjentów poddawanych hemodializie, szczególnie u pacjentów ze skłonnością do niedociśnienia lub z powikłaniami przetok tętniczo-żylnych (np. zwężenia, tętniaki itp.) U tych pacjentów zaleca się wczesną rewizję przecieku i wczesną rewizję przetoki profilaktyka przeciwzakrzepowa, np. kwasem acetylosalicylowym.
W pojedynczych przypadkach obserwowano hiperkaliemię, chociaż nie ustalono związku przyczynowego. U pacjentów z przewlekłą niewydolnością nerek należy monitorować elektrolity w surowicy. W przypadku podwyższonego lub wzrastającego stężenia potasu w surowicy, oprócz odpowiedniego leczenia hiperkaliemii, należy rozważyć przerwanie podawania epoetyny alfa do czasu wyrównania stężenia potasu w surowicy.
Ze względu na podwyższony hematokryt, podczas leczenia epoetyną alfa często konieczne jest zwiększenie dawki heparyny podczas hemodializy. Jeśli heparynizacja nie jest optymalna, może dojść do niedrożności układu dializacyjnego.
W oparciu o obecnie dostępne informacje, wyrównanie niedokrwistości epoetyną alfa u dorosłych pacjentów z niewydolnością nerek niepoddawanych jeszcze dializie nie przyspiesza progresji niewydolności nerek.
Leczenie pacjentów z niedokrwistością wywołaną chemioterapią
U pacjentów z nowotworem leczonych epoetyną alfa poziom hemoglobiny należy regularnie mierzyć do osiągnięcia stabilnego poziomu, a następnie w okresowych odstępach czasu.
Epoetyny to czynniki wzrostu, które przede wszystkim stymulują produkcję erytrocytów. Receptory erytropoetyny mogą ulegać ekspresji na powierzchni różnych komórek nowotworowych.Jak w przypadku wszystkich czynników wzrostu, istnieje obawa, że epoetyny mogą stymulować wzrost guza.Nie można wykluczyć roli ESA w progresji guza.Skrócony czas przeżycia bez progresji. W kontrolowanych badaniach klinicznych stosowanie epoetyny alfa i innych ESA wiązało się ze zmniejszeniem kontroli lokoregionalnej guza lub zmniejszeniem całkowitego przeżycia:
• zmniejszona kontrola lokoregionalna u pacjentów z zaawansowanym rakiem głowy i szyi leczonych radioterapią, przy podawaniu do uzyskania stężenia hemoglobiny powyżej 14 g/dl (8,7 mmol/l),
• skrócenie czasu przeżycia całkowitego i wzrost liczby zgonów przypisywanych progresji guza po 4 miesiącach u pacjentów z przerzutowym rakiem piersi leczonych chemioterapią przy podawaniu w celu uzyskania stężenia hemoglobiny w zakresie 12-14 g/dl (7,5-8,7 mmol/l) ,
• zwiększone ryzyko zgonu przy podawaniu w celu osiągnięcia stężenia hemoglobiny 12 g/dl (7,5 mmol/l) u pacjentów z aktywnymi nowotworami złośliwymi, nieleczonych chemioterapią ani radioterapią. Stosowanie ESA nie jest wskazane w tej populacji pacjentów.
• 9% zwiększone ryzyko progresji choroby (PD) lub zgonu w grupie epoetyny alfa i terapii standardowej (SOC) oraz 15% zwiększone ryzyko, którego nie można statystycznie wykluczyć u pacjentek z rakiem piersi z przerzutami, leczonych chemioterapią w celu osiągnięcia zakres stężenia hemoglobiny 10-12 g/dl (6,2-7,5 mmol/l).
W związku z powyższym, w niektórych stanach klinicznych transfuzja krwi powinna być preferowanym sposobem leczenia niedokrwistości u chorych na nowotwory.Decyzja o leczeniu rekombinowaną erytropoetyną powinna opierać się na ocenie stosunku korzyści do ryzyka z udziałem czynników ryzyka indywidualnego pacjenta i należy brać pod uwagę specyficzny kontekst kliniczny. Czynniki, które należy wziąć pod uwagę w tej ocenie, powinny obejmować rodzaj nowotworu i jego stadium, stopień niedokrwistości, „oczekiwaną długość życia”, środowisko, w którym pacjent jest leczony oraz stan pacjenta. preferencje (patrz punkt 5.1).
U chorych na nowotwory otrzymujących chemioterapię, przy ocenie adekwatności leczenia epoetyną alfa (pacjenci zagrożeni przetoczeniem) należy wziąć pod uwagę 2-3 tygodniową przerwę między podaniem ESA a pojawieniem się erytrocytów indukowanych erytropoetyną.
Pacjenci chirurgiczni uczestniczący w programach autologicznej predoncji
Należy przestrzegać wszystkich specjalnych ostrzeżeń i środków ostrożności związanych z programami autologicznej dawstwa; w szczególności zastępowanie objętości musi być wykonywane rutynowo.
Pacjenci zakwalifikowani do dużych planowych operacji ortopedycznych
Zawsze przestrzegaj dobrych praktyk zarządzania krwią w okresie okołooperacyjnym.
Pacjenci zakwalifikowani do dużych planowych operacji ortopedycznych powinni otrzymać „odpowiednią profilaktykę przeciwzakrzepową, ponieważ u pacjentów chirurgicznych mogą wystąpić zdarzenia zakrzepowe i naczyniowe, zwłaszcza u pacjentów z współistniejącą chorobą sercowo-naczyniową. Należy również zwrócić szczególną uwagę. Ponadto u pacjentów z wyjściowym stężeniem hemoglobiny >13 g/dl (>8,1 mmol/l) nie można wykluczyć, że leczenie epoetyną alfa może wiązać się ze zwiększonym ryzykiem pooperacyjnych zdarzeń zakrzepowych/naczyniowych. epoetyny alfa nie należy stosować u pacjentów z wyjściowym stężeniem hemoglobiny >13 g/dl (>8,1 mmol/l).
Substancje pomocnicze
Ten produkt leczniczy zawiera mniej niż 1 mmol (23 mg) sodu na ampułko-strzykawkę, co oznacza, że jest zasadniczo „wolny od sodu”.
04.5 Interakcje z innymi produktami leczniczymi i inne formy interakcji -
Nie ma dowodów na to, że leczenie epoetyną alfa wpływa na metabolizm innych produktów leczniczych.
Leki zmniejszające erytropoezę mogą osłabiać odpowiedź na epoetynę alfa.
Ponieważ cyklosporyna jest wiązana przez erytrocyty, istnieje możliwość interakcji leków. Jeśli epoetyna alfa jest podawana jednocześnie z cyklosporyną, należy monitorować stężenie cyklosporyny we krwi i dostosowywać dawkę cyklosporyny w miarę wzrostu hematokrytu.
Nie ma dowodów wskazujących na „interakcję między epoetyną alfa i czynnikiem stymulującym tworzenie kolonii granulocytów (G-CSF) lub czynnikiem stymulującym tworzenie kolonii granulocytów i makrofagów (GM-CSF) w odniesieniu do różnicowania lub proliferacji hematologicznej w próbkach z biopsji guza. in vitro.
U dorosłych pacjentów z rakiem piersi z przerzutami jednoczesne podskórne podawanie 40 000 j.m./ml epoetyny alfa z 6 mg/kg trastuzumabu nie miało wpływu na farmakokinetykę trastuzumabu.
04.6 Ciąża i karmienie piersią -
Ciąża
Brak lub ograniczone dane dotyczące stosowania epoetyny alfa u kobiet w ciąży Badania na zwierzętach wykazały szkodliwy wpływ na reprodukcję (patrz punkt 5.3).
Dlatego epoetyna alfa powinna być stosowana w ciąży tylko wtedy, gdy potencjalne korzyści przewyższają potencjalne ryzyko dla płodu.Stosowanie epoetyny alfa nie jest zalecane u ciężarnych pacjentek chirurgicznych, które biorą udział w programie autologicznego przetoczenia.
Czas karmienia
Nie wiadomo, czy egzogenna epoetyna alfa przenika do mleka ludzkiego.Epoetynę alfa należy stosować ostrożnie u kobiet karmiących piersią Należy podjąć decyzję, czy przerwać karmienie piersią, czy przerwać/przerwać leczenie epoetyną alfa, biorąc pod uwagę korzyści z karmienia piersią dla dziecka i korzyści z leczenia dla dziecka. kobieta.
Nie zaleca się stosowania epoetyny alfa u pacjentek chirurgicznych w okresie laktacji uczestniczących w programie autologicznego przetoczenia.
Płodność
Nie ma badań określających potencjalny wpływ epoetyny alfa na płodność mężczyzn lub kobiet.
04.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn -
Nie przeprowadzono badań dotyczących zdolności prowadzenia pojazdów i obsługiwania maszyn Binocrit nie ma wpływu lub ma nieistotny wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn.
04.8 Działania niepożądane -
Podsumowanie profilu bezpieczeństwa
Najczęstszym działaniem niepożądanym leku podczas leczenia epoetyną alfa jest zależne od dawki podwyższenie ciśnienia krwi lub pogorszenie istniejącego wcześniej nadciśnienia tętniczego. Należy monitorować ciśnienie krwi, szczególnie na początku leczenia (patrz punkt 4.4).
Najczęstszymi działaniami niepożądanymi leku obserwowanymi w badaniach klinicznych z epoetyną alfa są: biegunka, nudności, wymioty, gorączka i ból głowy. Choroba grypopodobna może wystąpić szczególnie na początku leczenia.
Przekrwienie dróg oddechowych, w tym przypadki przekrwienia górnych dróg oddechowych, przekrwienia błony śluzowej nosa i zapalenia nosogardzieli, zgłaszano w badaniach z wydłużonymi przerwami między dawkami u dorosłych pacjentów z niewydolnością nerek i jeszcze niepoddawanych dializie.
U pacjentów leczonych ESA obserwowano zwiększoną częstość występowania zakrzepicy naczyń (TVE) (patrz punkt 4.4).
Tabela działań niepożądanych
Spośród łącznie 3262 pacjentów włączonych do 23 randomizowanych, podwójnie zaślepionych, kontrolowanych placebo lub standardowo kontrolowanych badań, ogólny profil bezpieczeństwa epoetyny alfa oceniono u 992 pacjentów z niedokrwistością, w tym 228 pacjentów z leczoną przewlekłą niewydolnością nerek. z epoetyną alfa w 4 badaniach przewlekłej niewydolności nerek (2 badania przed dializą [N = 131 narażonych pacjentów z przewlekłą niewydolnością nerek] i 2 badania na dializie [N = 97 narażonych pacjentów z przewlekłą niewydolnością nerek]; 1404 pacjentów z nowotworem narażonych na 16 badań na niedokrwistość spowodowaną chemioterapią; 147 osób narażonych w 2 badaniach autologicznego oddawania krwi i 213 osób narażonych w 1 badaniu okołooperacyjnym Działania niepożądane zgłaszane przez ≥ 1% pacjentów leczonych epoetyną alfa w tych badaniach przedstawiono w poniższej tabeli.
Ocena częstości: bardzo często (≥ 1/10); często (≥ 1/100,
1 Zidentyfikowane w doświadczeniu postmarketingowe i kategoria częstotliwości oszacowana na podstawie wskaźników spontanicznych zgłoszeń
² Powszechne w dializie
³ Obejmuje zdarzenia tętnicze i żylne, zarówno śmiertelne, jak i niezakończone zgonem, takie jak zakrzepica żył głębokich, zator tętnicy płucnej, zakrzepica siatkówki, zakrzepica tętnic (w tym zawał mięśnia sercowego), incydenty naczyniowo-mózgowe (w tym zawał mózgu i krwotok mózgowy), przemijające napady niedokrwienne, przeciek. zakrzepica (w tym sprzęt do dializy) i zakrzepica w tętniakach przetoki tętniczo-żylnej
4 Omówiono w podpunkcie poniżej i/lub punkcie 4.4.
Opis wybranych działań niepożądanych
Zgłaszano reakcje nadwrażliwości, w tym przypadki wysypki (w tym pokrzywki), reakcje anafilaktyczne i obrzęk naczynioruchowy (patrz punkt 4.4).
Kryzysy nadciśnieniowe z encefalopatią i napady padaczkowe wymagające natychmiastowej pomocy lekarskiej i intensywnej opieki również występowały podczas leczenia epoetyną alfa pacjentów z poprzednio prawidłowym lub niskim ciśnieniem krwi.
Aplazja czysto czerwonych krwinek, w której pośredniczą przeciwciała (in
Populacja pediatryczna z przewlekłą niewydolnością nerek podczas hemodializy
Ekspozycja pacjentów pediatrycznych z przewlekłą niewydolnością nerek poddawanych hemodializie w badaniach klinicznych i w doświadczeniu postmarketingowe jest ograniczony. W tej populacji nie zgłoszono żadnych działań niepożądanych specyficznych dla dzieci, które nie zostały wymienione w powyższej tabeli lub które są niezgodne z chorobą podstawową.
Zgłaszanie podejrzewanych działań niepożądanych
Zgłaszanie podejrzewanych działań niepożądanych występujących po dopuszczeniu produktu leczniczego do obrotu jest ważne, ponieważ umożliwia ciągłe monitorowanie stosunku korzyści do ryzyka produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem krajowego systemu zgłaszania. „adres www. agenziafarmaco.gov.it/it/responsabili.
04.9 Przedawkowanie -
Margines terapeutyczny epoetyny alfa jest bardzo szeroki.Przedawkowanie epoetyny alfa może wywołać skutki stanowiące przedłużenie działania farmakologicznego hormonu.W obecności nadmiernie wysokiego poziomu hemoglobiny można zastosować upuszczanie krwi.Należy zastosować dodatkowe leczenie wspomagające .
05.0 WŁAŚCIWOŚCI FARMAKOLOGICZNE -
05.1 "Właściwości farmakodynamiczne -
Grupa farmakoterapeutyczna: leki przeciwanemiczne, erytropoetyna, kod ATC: B03XA01
Binocrit jest biopodobnym produktem leczniczym. Bardziej szczegółowe informacje dostępne są na stronie internetowej Europejskiej Agencji Leków: http://www.ema.europa.eu.
Mechanizm akcji
Erytropoetyna (EPO) jest hormonem glikoproteinowym wytwarzanym głównie przez nerki w odpowiedzi na niedotlenienie i jest centralnym regulatorem wytwarzania erytrocytów. „EPO bierze udział we wszystkich fazach rozwoju erytroidów, a jej główne działanie wyraża się na poziomie prekursorów erytroidalnych. Po związaniu się ze swoim receptorem na powierzchni komórki, EPO aktywuje szlaki transmisji sygnałów zakłócających „apoptozę” i stymuluje proliferację komórek erytroidalnych.
Rekombinowana ludzka EPO (epoetyna alfa), eksprymowana w komórkach jajnika chomika chińskiego, ma sekwencję 165 aminokwasów identyczną z sekwencją ludzkiej EPO z moczu; te dwie substancje są nie do odróżnienia od analiz funkcjonalnych. Pozorna masa cząsteczkowa erytropoetyny wynosi od 32 000 do 40 000 daltonów.
Erytropoetyna jest czynnikiem wzrostu, który przede wszystkim stymuluje produkcję czerwonych krwinek.Receptory erytropoetyny mogą ulegać ekspresji na powierzchni różnych typów komórek nowotworowych.
Efekty farmakodynamiczne
Zdrowi wolontariusze
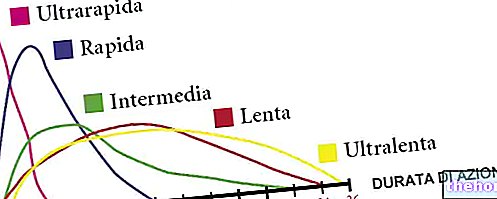
Po podaniu pojedynczych dawek (20 000 do 160 000 jm podskórnie) epoetyny alfa zaobserwowano odpowiedź zależną od dawki dla badanych markerów farmakodynamicznych, w tym retikulocytów, erytrocytów i hemoglobiny. Dla zmian odsetka retikulocytów zaobserwowano zdefiniowany profil stężenie-czas, ze szczytem i powrotem do wartości wyjściowej. Mniej zdefiniowany profil zaobserwowano dla erytrocytów i hemoglobiny Ogólnie rzecz biorąc, wszystkie markery farmakodynamiczne zwiększały się liniowo proporcjonalnie do dawki, a maksymalną odpowiedź osiągano przy wyższych poziomach dawek.
W dodatkowych badaniach farmakodynamicznych oceniano 40 000 jm raz w tygodniu w porównaniu do 150 jm/kg 3 razy w tygodniu. Pomimo różnic w profilach stężenie-czas, odpowiedź farmakodynamiczna (mierzona zmianami odsetka retikulocytów, hemoglobiny i całkowitej liczby erytrocytów) była podobna w tych schematach terapeutycznych.W dalszych badaniach porównywano schemat 40 000 jm epoetyny alfa raz w tygodniu w dawkach od 80 000 do 120 000 jm podawanych podskórnie co dwa tygodnie. Ogólnie rzecz biorąc, na podstawie wyników tych badań farmakodynamicznych u zdrowych osób, schemat 40 000 jm raz w tygodniu wydaje się być skuteczniejszy pod względem wytwarzania erytrocytów w porównaniu ze schematami stosowanymi co dwa tygodnie, chociaż podobne wytwarzanie retikulocytów obserwowano w schematach raz w tygodniu i co dwa tygodnie.
Przewlekłą niewydolność nerek
Wykazano, że epoetyna alfa stymuluje erytropoezę u pacjentów z niedokrwistością i przewlekłą niewydolnością nerek, w tym u pacjentów dializowanych i przed dializą. Pierwszą zauważalną odpowiedzią na epoetynę alfa jest zwiększenie liczby retikulocytów w ciągu 10 dni, a następnie zwiększenie liczby erytrocytów, hemoglobiny i hematokrytu, zwykle w ciągu 2 do 6 tygodni.Odpowiedź dotycząca hemoglobiny różni się w zależności od pacjenta i może być pod wpływem złogów żelaza i współistniejących chorób.
Niedokrwistość wywołana chemioterapią
Wykazano, że epoetyna alfa podawana 3 razy w tygodniu lub raz w tygodniu zwiększa stężenie hemoglobiny i zmniejsza potrzebę transfuzji po pierwszym miesiącu leczenia u pacjentów z niedokrwistością nowotworową poddawanych chemioterapii.
W badaniu porównującym schemat terapeutyczny z 150 IU/kg 3 razy w tygodniu oraz schemat terapeutyczny z 40 000 IU raz w tygodniu u osób zdrowych i chorych na raka z niedokrwistością, profile czasowe zmian odsetka retikulocytów, hemoglobiny i całkowitej liczba erytrocytów była podobna w obu schematach, zarówno u zdrowych osób, jak iu osób z niedokrwistością i nowotworem. Wartości AUC odpowiednich parametrów farmakodynamicznych były podobne w schemacie 150 j.m./kg 3 razy w tygodniu i 40 000 j.m. raz w tygodniu u zdrowych osób, a także w osoby z anemią nowotworową.
Dorośli pacjenci chirurgiczni uczestniczący w programie autologicznej predoncji
Wykazano, że epoetyna alfa stymuluje wytwarzanie erytrocytów, umożliwiając zwiększenie autologicznego pobierania krwi i ograniczenie redukcji stężenia hemoglobiny u dorosłych pacjentów oczekujących na duży planowy zabieg chirurgiczny, u których uważa się, że wstępne złogi nie w pełni zaspokajają okołooperacyjne zapotrzebowanie na krew. Najbardziej widoczne efekty obserwuje się u pacjentów z niskimi wartościami hemoglobiny (≤ 13 g/dl).
Leczenie dorosłych pacjentów zakwalifikowanych do poważnej planowej operacji ortopedycznej
U pacjentów zakwalifikowanych do dużej planowej operacji ortopedycznej z wartościami hemoglobiny przed leczeniem > 10 i ≤ 13 g / dl, wykazano, że epoetyna alfa zmniejsza ryzyko otrzymywania transfuzji allogenicznych i przyspiesza powrót erytroidów (podwyższony poziom hemoglobiny, poziom hematokrytu i liczba retikulocytów).
Skuteczność kliniczna i bezpieczeństwo
Przewlekłą niewydolność nerek
Epoetynę alfa badano w badaniach klinicznych u dorosłych pacjentów z niedokrwistością i przewlekłą niewydolnością nerek, w tym pacjentów poddawanych hemodializie i przed dializą, w celu leczenia niedokrwistości i utrzymania hematokrytu w zakresie stężeń docelowych od 30 do 36%.
W badaniach klinicznych, w których dawki początkowe wynosiły od 50 do 150 jm/kg trzy razy w tygodniu, około 95% pacjentów odpowiedziało klinicznie istotnym wzrostem hematokrytu.Po około dwóch miesiącach leczenia prawie wszyscy pacjenci byli niezależni od transfuzji. osiągnięto docelowy hematokryt, dawkę podtrzymującą ustalano indywidualnie dla każdego pacjenta.
W trzech największych badaniach klinicznych przeprowadzonych u dorosłych pacjentów dializowanych mediana dawki podtrzymującej wymaganej do utrzymania hematokrytu pomiędzy 30 a 36% wynosiła około 75 jm/kg podawane 3 razy w tygodniu.
W wieloośrodkowym, podwójnie zaślepionym, kontrolowanym placebo badaniu jakości życia u pacjentów z przewlekłą niewydolnością nerek poddawanych hemodializie zaobserwowano klinicznie i statystycznie istotną poprawę u pacjentów leczonych epoetyną alfa w porównaniu z placebo pod względem zmęczenia, objawów fizycznych, związków i depresja (Kwestionariusz Chorób Nerek) po sześciu miesiącach terapii. Pacjenci w grupie otrzymującej epoetynę alfa zostali również włączeni do otwartego przedłużonego badania, w którym wykazano poprawę jakości życia i utrzymywano ją przez dodatkowe 12 miesięcy.
Dorośli pacjenci z niewydolnością nerek niepoddani jeszcze dializie
W badaniach klinicznych przeprowadzonych u pacjentów z przewlekłą niewydolnością nerek niepoddawanych dializie, leczonych epoetyną alfa, średni czas trwania terapii wynosił prawie pięć miesięcy. Pacjenci ci zareagowali na leczenie epoetyną alfa w sposób podobny do obserwowanego u pacjentów dializowanych. U pacjentów z przewlekłą niewydolnością nerek niepoddawanych dializie zaobserwowano przedłużony i zależny od dawki wzrost hematokrytu po dożylnym lub podskórnym podaniu epoetyny alfa. Szybkość wzrostu hematokrytu była podobna w przypadku obu dróg podania epoetyny alfa. Wykazano, że epoetyna alfa między 75 a 150 j.m./kg na tydzień utrzymuje hematokryt na wartościach od 36 do 38% przez okres do sześciu miesięcy.
W dwóch badaniach z wydłużonymi przerwami w podawaniu epoetyny alfa (3 razy w tygodniu, raz w tygodniu, raz na 2 tygodnie i raz na 4 tygodnie) niektórzy pacjenci z dłuższymi przerwami w podawaniu nie utrzymywali odpowiednich poziomów hemoglobiny i spełniali protokołowe kryteria odstawienia dla hemoglobiny. (0% w grupie raz na tydzień, 3,7% w grupie raz na 2 tygodnie i 3,3% w grupie raz na 4 tygodnie).
W prospektywnym randomizowanym badaniu oceniono 1432 pacjentów z niedokrwistością i przewlekłą niewydolnością nerek, którzy nie byli dializowani. Pacjenci byli przypisywani do leczenia epoetyną alfa w celu utrzymania stężenia hemoglobiny 13,5 g/dl (powyżej zalecanego stężenia hemoglobiny) lub 11,3 g/dl. Poważne zdarzenie sercowo-naczyniowe (zgon, zawał mięśnia sercowego, udar lub hospitalizacja z powodu zastoinowej niewydolności serca) wystąpiło u 125 (18%) z 715 pacjentów w grupie z wyższym poziomem hemoglobiny w porównaniu z 97 (14%) z 717 pacjentów w z niższymi poziomami hemoglobiny (współczynnik ryzyka [HR] 1,3; 95% CI: 1,0; 1,7; p = 0,03).
Przeprowadzono zbiorcze analizy post-hoc badań klinicznych nad ESA u pacjentów z przewlekłą niewydolnością nerek (poddani dializie, nie poddani dializie, chorzy na cukrzycę i bez cukrzycy). Zaobserwowano trend wzrostu szacowanego ryzyka śmiertelności z jakiejkolwiek przyczyny oraz zdarzeń sercowo-naczyniowych i naczyniowo-mózgowych związanych z większymi skumulowanymi dawkami ESA, niezależnie od obecności lub braku cukrzycy lub dializy (patrz punkt 4.2 i punkt 4.4).
Leczenie pacjentów z niedokrwistością wywołaną chemioterapią
Epoetynę alfa badano w badaniach klinicznych u pacjentów z niedokrwistością nowotworową z guzami limfoidalnymi i litymi oraz u pacjentów poddawanych różnym schematom chemioterapii, w tym schematom bez platyny i bez platyny.W badaniach tych wykazano, że epoetyna alfa podawana 3 razy w tygodniu i raz tygodniowo zwiększa stężenie hemoglobiny i zmniejsza potrzebę transfuzji po pierwszym miesiącu leczenia u pacjentów z niedokrwistością nowotworową. zaobserwowano efekt.
Dostępne dowody wskazują, że pacjenci z nowotworami złośliwymi układu krwiotwórczego i guzami litymi odpowiadają równoważnie na terapię epoetyną alfa oraz że pacjenci z naciekiem nowotworu szpiku kostnego lub bez niego odpowiadają równoważnie na terapię epoetyną alfa. Podobną intensywność chemioterapii w grupach otrzymujących epoetynę alfa i placebo w badaniach nad chemioterapią wykazywał podobny „obszar pod krzywą czasu neutrofili u pacjentów leczonych epoetyną alfa i placebo, a także podobny odsetek pacjenci w grupach otrzymujących epoetynę alfa i placebo, u których bezwzględna liczba neutrofili wynosiła mniej niż 1000 i 500 komórek/mcL.
W prospektywnym, randomizowanym, podwójnie zaślepionym, kontrolowanym placebo badaniu przeprowadzonym z udziałem 375 pacjentów z niedokrwistością z różnymi nowotworami złośliwymi nieszpikowymi i leczonych chemioterapią nie opartą na związkach platyny, zaobserwowano znaczne zmniejszenie następstw związanych z niedokrwistością (zmęczenie). energii i zmniejszonej aktywności) w oparciu o następujące pomiary instrumentalne i skale oceny: Skala Ogólnej Oceny Funkcjonalnej Terapii Nowotworowej – Anemia (FACT-An), Skala Zmęczenia FACT-An oraz Skala Cancer Linear Analogue Scale (CLAS).W dwóch innych mniejszych, randomizowanych, kontrolowanych placebo badaniach nie zaobserwowano istotnej poprawy parametrów jakości życia odpowiednio w skalach EORTC-QLQ-C30 lub CLAS.
Przeżycie i progresję guza analizowano w pięciu dużych badaniach kontrolowanych z udziałem łącznie 2833 pacjentów, w tym czterech podwójnie ślepych badaniach kontrolowanych placebo i jednym otwartym badaniu. Do tych badań włączono pacjentów poddawanych chemioterapii (dwa badania) lub populacje pacjentów, u których nie ma wskazań do stosowania ESA: pacjentów z nowotworem i niedokrwistością niepoddawanych chemioterapii oraz pacjentów z rakiem głowy i szyi poddawanych radioterapii. W dwóch badaniach pożądany poziom stężenia hemoglobiny wynosił >13 g/dl (8,1 mmol/l); w pozostałych badaniach wahała się od 12 do 14 g/dl (7,5 do 8,7 mmol/l). W otwartym badaniu nie było różnicy w całkowitym przeżyciu pacjentów leczonych rekombinowaną ludzką erytropoetyną i grup kontrolnych. W czterech badaniach kontrolowanych placebo, całkowity współczynnik ryzyka przeżycia wahał się od 1,25 do 2,47, na korzyść kontroli. W porównaniu z grupą kontrolną w badaniach tych zaobserwowano statystycznie istotny, stały i niewyjaśniony wzrost śmiertelności u pacjentów z niedokrwistością związaną z kilkoma powszechnymi nowotworami złośliwymi i leczonych rekombinowaną ludzką erytropoetyną. Całkowity wynik przeżycia nie został wystarczająco wyjaśniony przez różnice w częstości występowania zakrzepicy i związanych z nią powikłań u pacjentów leczonych rekombinowaną ludzką erytropoetyną oraz u pacjentów z grupy kontrolnej.
„Analiza danych indywidualnych pacjentów została również przeprowadzona u ponad 13 900 pacjentów z nowotworem (otrzymujących chemioterapię, radioterapię, chemioradioterapię lub niepoddawanych żadnemu leczeniu) uczestniczących w 53 kontrolowanych badaniach klinicznych z udziałem różnych epoetyn. Metaanaliza pacjentów. dane dostarczyły oszacowania punktowego współczynnika ryzyka (współczynnik ryzyka) 1,06 na korzyść grupy kontrolnej (95% CI: 1,00; 1,12; 53 badania i 13 933 pacjentów) oraz dla pacjentów z nowotworami leczonych chemioterapią współczynnik ryzyka dla całkowitego przeżycia wyniósł 1,04 (95% CI: 0,97; 1,11; 38 badań i 10441 pacjentów). Metaanalizy konsekwentnie wykazały również znacząco zwiększone względne ryzyko zdarzeń zakrzepowo-zatorowych u pacjentów z nowotworem leczonych rekombinowaną ludzką erytropoetyną (patrz punkt 4.4).
Otwarte, randomizowane, wieloośrodkowe badanie przeprowadzono z udziałem 2098 kobiet z niedokrwistością z przerzutowym rakiem piersi, które otrzymały chemioterapię pierwszego lub drugiego rzutu. Było to badanie typu non-inferiority zaprojektowane w celu wykluczenia o 15% zwiększonego ryzyka progresji nowotworu lub zgonu dla epoetyny alfa w połączeniu ze standardową terapią (SOC) w porównaniu z samym SOC. Mediana czasu przeżycia wolnego od progresji (przeżycie bez progresji, PFS) według oceny postępu choroby przez badacza wynosił 7,4 miesiąca w każdym ramieniu (HR 1,09, 95% CI: 0,99, 1,20), co wskazuje, że cel badania nie został osiągnięty odciąć Zgłoszono 1337 zgonów. Mediana przeżycia całkowitego w grupie otrzymującej epoetynę alfa plus SOC wyniosła 17,2 miesiąca w porównaniu z 17,4 miesiąca w grupie otrzymującej sam SOC (HR 1,06, 95% CI: 0,95, 1,18). W ramieniu otrzymującym epoetynę alfa plus SOC istotnie mniej pacjentów otrzymywało transfuzje erytrocytów (5,8% vs. 11,4%); jednak w ramieniu otrzymującym epoetynę alfa plus SOC znacznie więcej pacjentów (2,8% w porównaniu z 1,4%) doświadczyło zakrzepowych zdarzeń naczyniowych.
Program predonacji autologicznej
Wpływ epoetyny alfa na ułatwienie autologicznego oddawania krwi u pacjentów z niskim hematokrytem (≤ 39% przy braku niedokrwistości z niedoboru żelaza) oczekujących na poważny zabieg ortopedyczny oceniano w badaniu z podwójnie ślepą próbą. pacjentów oraz badanie z pojedynczą ślepą próbą, kontrolowane placebo, przeprowadzone na 55 pacjentach.
W badaniu z podwójnie ślepą próbą pacjenci otrzymywali epoetynę alfa 600 j.m./kg lub placebo dożylnie raz na dobę co 3 lub 4 dni przez 3 tygodnie (łącznie 6 dawek). Przeciętnie pacjenci leczeni epoetyną alfa byli w stanie oddać znacznie więcej jednostek krwi dla predepozytu (4,5 jednostki) w porównaniu do pacjentów otrzymujących placebo (3,0 jednostki).
W badaniu z pojedynczą ślepą próbą pacjenci otrzymywali epoetynę alfa 300 j.m./kg lub 600 j.m./kg lub placebo dożylnie raz na dobę co 3 lub 4 dni przez 3 tygodnie (łącznie 6 dawek). Pacjenci leczeni epoetyną alfa byli również w stanie oddać znacznie więcej jednostek krwi do depozytu wstępnego (epoetyna alfa 300 j.m./kg = 4,4 jednostki; epoetyna alfa 600 j.m./kg = 4,7 jednostki) w porównaniu do pacjentów otrzymujących placebo (2,9 jednostki). ).
Terapia epoetyną alfa zmniejszyła ryzyko ekspozycji na krew allogeniczną o 50% w porównaniu z pacjentami nieotrzymującymi epoetyny alfa.
Duża planowa operacja ortopedyczna
Wpływ epoetyny alfa (300 j.m./kg lub 100 j.m./kg) na ekspozycję na alogeniczne transfuzje krwi oceniano w podwójnie zaślepionym, kontrolowanym placebo badaniu klinicznym z udziałem dorosłych pacjentów niepoddawanych żelazonie, oczekujących na planowaną dużą operację ortopedyczną w biodro lub kolano. Epoetynę alfa podawano podskórnie w ciągu 10 dni przed zabiegiem, w dniu zabiegu i przez cztery dni po zabiegu. Pacjentów stratyfikowano według wyjściowego stężenia hemoglobiny (≤10 g/dl, >10 do ≤13 g/dl i >13 g/dl).
Epoetyna alfa 300 j.m./kg istotnie zmniejszała ryzyko przetoczeń allogenicznych u pacjentów, u których stężenie hemoglobiny przed leczeniem wahało się od >10 do ≤13 g/dl Szesnaście procent pacjentów leczonych epoetyną alfa 300 j.m./kg, 23% pacjentów leczonych epoetyną alfa 100 jm/kg i 45% pacjentów leczonych placebo wymagało transfuzji.
W otwartym badaniu w grupach równoległych u dorosłych pacjentów bez niedoboru żelaza, u których stężenie hemoglobiny przed leczeniem wahało się od ≥10 do ≤13 g/dl oczekujących na duży zabieg ortopedyczny stawu biodrowego lub kolanowego, porównano epoetynę alfa 300 j.m./kg na dobę podskórnie w ciągu 10 dni przed zabiegiem, w dniu zabiegu iw ciągu czterech dni po zabiegu z epoetyną alfa 600 jm/kg podskórnie raz w tygodniu przez 3 tygodnie przed zabiegiem i w dniu zabiegu.
Od fazy przed leczeniem do fazy przedoperacyjnej średni wzrost stężenia hemoglobiny w grupie 600 j.m./kg na tydzień (1,44 g/dl) był dwukrotnie wyższy niż w grupie 300 j.m./dl kg na dzień (0,73 g / dL). Średnie poziomy hemoglobiny były podobne w obu leczonych grupach przez cały okres pooperacyjny.
Odpowiedź erytropoetyczna obserwowana w obu leczonych grupach skutkowała podobnymi szybkościami transfuzji (16% w grupie 600 j.m./kg na tydzień i 20% w grupie 300 j.m./kg na dobę).
Populacja pediatryczna
Przewlekłą niewydolność nerek
Epoetynę alfa oceniano w otwartym, nierandomizowanym, 52-tygodniowym badaniu klinicznym z otwartym zakresem u dzieci i młodzieży z przewlekłą niewydolnością nerek poddawanych hemodializie Mediana wieku pacjentów włączonych do badania wynosiła 11,6 lat (zakres od 0,5 do 20,1 lat). lat).
Epoetynę alfa podawano dożylnie w dawkach 75 jm/kg/tydzień, podzielonych na 2 lub 3 dawki po dializie, miareczkowanych do 75 jm/kg/tydzień w odstępach 4-tygodniowych (maksymalnie 300 jm/kg/tydzień) aby uzyskać wzrost hemoglobiny o 1 g / dl / miesiąc. Pożądany zakres stężenia hemoglobiny wynosił od 9,6 do 11,2 g/dl. Osiemdziesiąt jeden procent pacjentów osiągnęło ten poziom stężenia hemoglobiny. Mediana czasu do celu wyniosła 11 tygodni, a mediana dawki do celu wyniosła 150 jm/kg/tydzień. Spośród pacjentów, którzy osiągnęli cel, 90% osiągnęło go w schemacie 3 razy w tygodniu.
Po 52 tygodniach 57% pacjentów pozostało w badaniu, otrzymując medianę dawki 200 IU/kg/tydzień.
Dane kliniczne dotyczące podawania podskórnego u dzieci są ograniczone. W 5 otwartych, niekontrolowanych badaniach z niewielką liczbą pacjentów (liczba pacjentów wahała się od 9 do 22, przy całkowitej liczbie N = 72), epoetynę alfa podawano podskórnie dzieciom w pojedynczej dawce rozpoczynającej się od 100 j.m./kg. /tydzień do 150 j.m./kg/tydz., z możliwością zwiększenia do 300 j.m./kg/tydz.W badaniach tych większość pacjentów była wstępnie dializowana (N=44), 27 pacjentów było poddawanych dializie otrzewnowej i dwaj byli poddawani hemodializie, wiek pacjentów wahał się od 4 miesięcy do 17 lat. Ogólnie rzecz biorąc, badania te mają ograniczenia metodologiczne, ale leczenie wiąże się z pozytywnymi tendencjami w kierunku wyższych poziomów hemoglobiny. Nie zgłoszono nieoczekiwanych zdarzeń niepożądanych (patrz punkt 4.2).
Niedokrwistość wywołana chemioterapią
Epoetynę alfa 600 j.m./kg (podawaną dożylnie lub podskórnie raz w tygodniu) oceniano w 16-tygodniowym randomizowanym, podwójnie zaślepionym, kontrolowanym placebo badaniu oraz w randomizowanym, kontrolowanym, otwartym badaniu trwającym 20 tygodni u dzieci z niedokrwistość poddawana chemioterapii mielosupresyjnej w leczeniu różnych dziecięcych nowotworów nieszpikowych.
W 16-tygodniowym badaniu (n = 222) u pacjentów leczonych epoetyną alfa nie stwierdzono istotnego wpływu na jakość życia pacjentów pediatrycznych zgłaszanych przez samych pacjentów lub przez ich rodziców lub w punktacji modułu nowotworowego w porównaniu z placebo ( Ponadto nie było statystycznej różnicy między odsetkiem pacjentów wymagających transfuzji krwinek czerwonych w grupie otrzymującej epoetynę alfa i grupie otrzymującej placebo.
W 20-tygodniowym badaniu (n = 225) nie było istotnej różnicy w pierwszorzędowym punkcie końcowym skuteczności, tj. w odsetku pacjentów, którzy wymagali przetoczenia krwinek czerwonych po 28. dniu (62% pacjentów, którzy otrzymywali epoetynę alfa w porównaniu z 69 % pacjentów otrzymujących standardową terapię).
05.2 "Właściwości farmakokinetyczne -
Wchłanianie
Po wstrzyknięciu podskórnym stężenie epoetyny alfa w surowicy osiągnęło maksimum między 12 a 18 godziną po podaniu. Nie stwierdzono kumulacji po podaniu wielokrotnych dawek 600 jm/kg podskórnie raz w tygodniu.
Całkowita biodostępność epoetyny alfa do wstrzyknięć podskórnych u zdrowych osób wynosi około 20%.
Dystrybucja
Średnia objętość dystrybucji wynosiła 49,3 ml/kg po dożylnych dawkach 50 i 100 j.m./kg u osób zdrowych. Po dożylnym podaniu epoetyny alfa pacjentom z przewlekłą niewydolnością nerek objętość dystrybucji wahała się od 57 do 107 ml/kg po dawkach pojedynczych (12 j.m./kg) i od 42 do 64 ml/kg po dawkach wielokrotnych (48). -192 jm / kg). Dlatego objętość dystrybucji jest nieco większa niż przestrzeń osocza.
Eliminacja
Okres półtrwania epoetyny alfa po wielokrotnym podaniu dożylnym wynosi około 4 godzin u zdrowych osób.
Okres półtrwania po podaniu podskórnym u zdrowych osób szacuje się na około 24 godziny.
Średnie CL / F dla schematów 150 IU / kg 3 razy w tygodniu i 40 000 IU raz w tygodniu u zdrowych osób wynosiły odpowiednio 31,2 i 12,6 ml / h / kg. Średni CL/F dla schematów 150 jm/kg 3 razy w tygodniu i 40 000 jm raz w tygodniu u pacjentów z niedokrwistością nowotworową wynosił odpowiednio 45,8 i 11,3 ml/h/kg. U większości pacjentów z rakiem z niedokrwistością poddawanych cyklicznej chemioterapii, CL/F był niższy po podskórnych dawkach 40 000 IU raz w tygodniu i 150 IU/kg 3 razy w tygodniu w porównaniu z wartościami obserwowanymi u zdrowych osób.
Liniowość / Nieliniowość
U zdrowych osób obserwowano proporcjonalny do dawki wzrost stężenia epoetyny alfa w surowicy po podaniu dożylnym 150 i 300 jm/kg 3 razy w tygodniu. Podanie podskórne pojedynczych dawek od 300 do 2400 jm/kg epoetyny alfa powodowało liniową korelację między średnią Cmax a dawką oraz między średnią AUC a dawką.U zdrowych osób zaobserwowano odwrotną korelację między pozornym klirensem a dawką.
W badaniach mających na celu zbadanie wydłużenia odstępu między dawkami (40 000 IU raz w tygodniu i 80 000, 100 000 i 120 000 IU co dwa tygodnie) zaobserwowano liniową, ale nieproporcjonalną do dawki korelację między średnim Cmax a dawką oraz między średnią wartością AUC. i dawki w stanie stacjonarnym.
Zależności farmakokinetyczne/farmakodynamiczne
Epoetyna alfa wykazuje zależny od dawki wpływ na parametry hematologiczne, który jest niezależny od drogi podania.
Populacja pediatryczna
U dzieci i młodzieży z przewlekłą niewydolnością nerek po wielokrotnym podaniu dożylnym epoetyny alfa obserwowano okres półtrwania wynoszący około 6,2 do 8,7 h. Profil farmakokinetyczny epoetyny alfa u dzieci i młodzieży wydaje się podobny do profilu u dorosłych.
Dane farmakokinetyczne u noworodków są ograniczone.
Badanie z udziałem 7 wcześniaków z bardzo niską masą urodzeniową i 10 zdrowych dorosłych, którym podano dożylnie erytropoetynę. sugerowali, że objętość dystrybucji była około 1,5 do 2 razy większa u wcześniaków niż u zdrowych dorosłych, a klirens był około 3 razy większy u wcześniaków niż u zdrowych dorosłych.
Zaburzenia czynności nerek
U pacjentów z przewlekłą niewydolnością nerek okres półtrwania podanej dożylnie epoetyny alfa jest nieco dłuższy, około 5 godzin, w porównaniu z osobami zdrowymi.
05.3 Przedkliniczne dane o bezpieczeństwie -
W badaniach toksykologicznych po podaniu wielokrotnym u psów i szczurów, ale nie małp, terapia epoetyną alfa była związana z subklinicznym zwłóknieniem szpiku kostnego. Zwłóknienie szpiku kostnego jest znanym powikłaniem przewlekłej niewydolności nerek u ludzi i może być związane z wtórną nadczynnością przytarczyc lub nieznanymi czynnikami.Częstość zwłóknienia szpiku kostnego nie była zwiększona w badaniu przeprowadzonym z udziałem pacjentów hemodializowanych leczonych przez 3 lata epoetyną alfa w porównaniu z zgodna grupa kontrolna pacjentów dializowanych nieleczonych epoetyną alfa.
Epoetyna alfa nie indukuje mutacji genów u bakterii (test Amesa), aberracji chromosomowych w komórkach ssaków, mikrojąder u myszy ani mutacji genów w locus HGPRT.
Nie przeprowadzono długoterminowych badań rakotwórczości. Niezgodne dane istniejące w literaturze, na podstawie uzyskanych wyników in vitro z próbkami ludzkiego guza sugerują możliwą rolę erytropoetyn w proliferacji guza. Znaczenie kliniczne jest niepewne.
W hodowlach ludzkich komórek szpiku kostnego epoetyna alfa specyficznie stymuluje erytropoezę i nie wpływa na leukopoezę. Nie stwierdzono cytotoksycznego wpływu epoetyny alfa na komórki szpiku kostnego.
W badaniach na zwierzętach wykazano, że epoetyna alfa podawana w cotygodniowych dawkach około 20-krotności zalecanej dawki tygodniowej u ludzi powoduje zmniejszenie masy ciała płodu, opóźnienie kostnienia i wzrost śmiertelności płodów. zmniejszenie przyrostu masy ciała i ich znaczenie dla ludzi nie jest znane przy dawkach terapeutycznych.
06.0 INFORMACJE FARMACEUTYCZNE -
06.1 Substancje pomocnicze -
Dihydrat jednozasadowego fosforanu sodu
Dwuwodny fosforan disodowy
Chlorek sodu
Glicyna
Polisorbat 80
Woda do wstrzykiwań
Kwas solny (do regulacji pH)
Wodorotlenek sodu (do dostosowania pH)
06.2 Niezgodność "-
Ze względu na brak badań zgodności, tego produktu leczniczego nie wolno mieszać z innymi produktami leczniczymi.
06.3 Okres ważności "-
2 lata
06.4 Specjalne środki ostrożności przy przechowywaniu -
Przechowywać i transportować w stanie schłodzonym (2°C - 8°C). Ten zakres temperatur musi być ściśle przestrzegany do momentu podania pacjentowi.
W przypadku stosowania ambulatoryjnego lek można wyjąć z lodówki, bez wkładania go z powrotem, maksymalnie przez okres 3 dni w temperaturze nieprzekraczającej 25°C. Jeżeli lek nie został użyty do końca tego okresu, musi wyrzucić.
Nie zamrażać ani nie wstrząsać.
Przechowywać w oryginalnym opakowaniu w celu ochrony leku przed światłem.
06.5 Rodzaj opakowania bezpośredniego i zawartość opakowania -
Ampułko-strzykawki (szkło typu I), z zabezpieczeniem igły lub bez, z korkiem tłoka (guma teflonowa) zamknięte w blistrach.
Binocrit 1000 j.m./0,5 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każda ampułkostrzykawka zawiera 0,5 ml roztworu do wstrzykiwań.
Opakowania po 1 lub 6 strzykawek.
Binocrit 2000 j.m./1 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każda ampułkostrzykawka zawiera 1 ml roztworu do wstrzykiwań.
Opakowania po 1 lub 6 strzykawek.
Binocrit 3000 j.m./0,3 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każda ampułkostrzykawka zawiera 0,3 ml roztworu do wstrzykiwań.
Opakowania po 1 lub 6 strzykawek.
Binocrit 4000 j.m./0,4 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każda ampułkostrzykawka zawiera 0,4 ml roztworu do wstrzykiwań.
Opakowania po 1 lub 6 strzykawek.
Binocrit 5000 j.m./0,5 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każda ampułko-strzykawka zawiera 0,5 ml roztworu do wstrzykiwań.
Opakowania po 1 lub 6 strzykawek.
Binocrit 6000 j.m./0,6 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każda ampułko-strzykawka zawiera 0,6 ml roztworu do wstrzykiwań.
Opakowania po 1 lub 6 strzykawek.
Binocrit 7000 j.m./0,7 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każda ampułkostrzykawka zawiera 0,7 ml roztworu do wstrzykiwań.
Opakowania po 1 lub 6 strzykawek.
Binocrit 8000 j.m. / 0,8 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każda ampułkostrzykawka zawiera 0,8 ml roztworu do wstrzykiwań.
Opakowania po 1 lub 6 strzykawek.
Binocrit 9000 j.m. / 0,9 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każda ampułkostrzykawka zawiera 0,9 ml roztworu do wstrzykiwań.
Opakowania po 1 lub 6 strzykawek.
Binocrit 10 000 j.m./1 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każda ampułkostrzykawka zawiera 1 ml roztworu do wstrzykiwań.
Opakowania po 1 lub 6 strzykawek.
Binocrit 20 000 j.m./0,5 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każda ampułkostrzykawka zawiera 0,5 ml roztworu do wstrzykiwań.
Opakowania po 1, 4 lub 6 strzykawek.
Binocrit 30 000 j.m. / 0,75 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każda ampułkostrzykawka zawiera 0,75 ml roztworu do wstrzykiwań.
Opakowania po 1, 4 lub 6 strzykawek.
Binocrit 40 000 j.m./1 ml roztwór do wstrzykiwań w ampułko-strzykawce
Każda ampułkostrzykawka zawiera 1 ml roztworu do wstrzykiwań.
Opakowania po 1, 4 lub 6 strzykawek.
Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
06.6 Instrukcje użytkowania i obsługi -
Binocrit nie może być używany i należy go wyrzucić
• jeśli płyn jest zabarwiony lub widać w nim unoszące się cząsteczki
• jeśli plomba jest zerwana
• jeśli wiadomo lub przypuszcza się, że mogło zostać przypadkowo zamrożone lub
• jeśli wystąpiła awaria lodówki
Ampułko-strzykawki są gotowe do użycia (patrz punkt 4.2). Ampułko-strzykawki nie wolno potrząsać. Strzykawki są oznaczone wypukłą podziałką; umożliwia to w razie potrzeby częściowe użycie. Każda podziałka odpowiada objętości 0, 1 ml Produkt jest przeznaczony wyłącznie do jednorazowego użytku Pobrać tylko jedną dawkę preparatu Binocrit z każdej strzykawki i wyrzucić niepotrzebny roztwór przed wstrzyknięciem.
Używanie ampułko-strzykawki z osłoną zabezpieczającą igłę
Osłona zabezpieczająca igłę zakrywa igłę po wstrzyknięciu i zapobiega zranieniu się operatora. Urządzenie nie przeszkadza w normalnym używaniu strzykawki.Naciskać powoli i równomiernie tłok, aż do uwolnienia pełnej dawki i nie będzie można dalej wcisnąć tłoka. Kontynuując naciskanie tłoka, odciągnąć strzykawkę od pacjenta. Urządzenie zabezpieczające zakrywa igłę natychmiast po zwolnieniu tłoka.
Używanie ampułko-strzykawki bez osłony zabezpieczającej igłę
Podać dawkę zgodnie ze standardową procedurą.
Niewykorzystany lek i odpady pochodzące z tego leku należy usunąć zgodnie z lokalnymi przepisami.
07.0 POSIADACZ „POZWOLENIA NA DOPUSZCZENIE DO OBROTU” -
Sandoz GmbH
Biochemiestr. 10
A-6250 Kundl
Austria
08.0 NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU -
Binocrit 1000 j.m./0,5 ml roztwór do wstrzykiwań w ampułko-strzykawce
EU / 1/07/410/001 - 1000 j.m. / 0,5 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) podanie podskórne lub dożylne 0,5 ml (2000 j.m./ml) 1 ampułkostrzykawka - AIC n. 038190017 / E
EU / 1/07/410/002 - 1000 j.m. / 0,5 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) podanie podskórne lub dożylne 0,5 ml (2000 j.m./ml) 6 ampułkostrzykawek - AIC n. 038190029 / PL
EU / 1/07/410/027 - 1000 j.m. / 0,5 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) - podanie podskórne lub dożylne - 0,5 ml (2000 j.m./ml) 1 ampułkostrzykawka 0,5 ml z bezpiecznym urządzeniem na igłę - AIC n. 038190272 / E
EU / 1/07/410/028 - 1000 IU / 0,5 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) - podskórne podanie dożylne - 0,5 ml (2000 IU/ml) - 6 ampułko-strzykawek po 0,5 ml z igłą do urządzenia bezpieczeństwo - AIC nr 038190284 / E
Binocrit 2000 j.m./1 ml roztwór do wstrzykiwań w ampułko-strzykawce
EU / 1/07/410/003 - 2000 j.m. / 1,0 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) podanie podskórne lub dożylne 1,0 ml (2000 j.m./ml) 1 ampułkostrzykawka - AIC n. 038190031 / E
EU / 1/07/410/004 - 2000 IU / 1,0 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) Podanie podskórne lub dożylne 1,0 ml (2000 IU / ml) 6 ampułkostrzykawek - AIC n. 038190043 / E
EU / 1/07/410/029 - 2000IU / 1ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) - podanie podskórne lub dożylne - 1ml (2000IU/ml) 1 1ml ampułkostrzykawka z zabezpieczeniem igły - AIC N. 038190296 / E
EU / 1/07/410 / 030- 2000 IU / 0,5 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) - podanie dożylne podskórne - 1 ml (2000 IU / ml) - 6 ampułko-strzykawek po 1 ml z zabezpieczeniem igły urządzenie - AIC nr 038190308 / E
Binocrit 3000 j.m./0,3 ml roztwór do wstrzykiwań w ampułko-strzykawce
EU / 1/07/410/005 - 3000 j.m. / 0,3 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) podanie podskórne lub dożylne 0,3 ml (10000 j.m./ml) 1 ampułkostrzykawka - AIC n. 038190056 / PL
EU / 1/07/410/006 - 3000 j.m. / 0,3 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) podanie podskórne lub dożylne 0,3 ml (10000 j.m./ml) 6 ampułkostrzykawek - AIC n. 038190068 / E
EU / 1/07/410 / 031-3000IU / 0,3ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) - podanie podskórne lub dożylne - 0,3ml (10000IU/ml) 1 0,3ml ampułkostrzykawka z urządzeniem zabezpieczającym na igłę - AIC nr 038190310 / E
EU / 1/07/410/032 - 3000IU / 0,3ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) - podanie dożylne podskórne - 0,3ml (10000 IU/ml) - 6 ampułkostrzykawek 0,3ml z bezpieczną igłą - AIC Nr 038190322 / E
Binocrit 4000 j.m./0,4 ml roztwór do wstrzykiwań w ampułko-strzykawce
EU / 1/07/410/007 - 4000 j.m. / 0,4 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) podanie podskórne lub dożylne 0,4 ml (10000 j.m./ml) 1 ampułkostrzykawka - AIC n. 038190070 / PL
EU / 1/07/410/008 - 4000 j.m. / 0,4 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) podanie podskórne lub dożylne 0,4 ml (10000 j.m./ml) 6 ampułkostrzykawek - AIC n. 038190082 / E
EU / 1/07/410/033 - 4000 IU / 0,4 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) - podanie podskórne lub dożylne - 0,4 ml (10000 IU / ml) 1 0,4 ml ampułkostrzykawka z zabezpieczeniem na igłę - AIC nr 038190334 / E
EU / 1/07/410/034 - 4000 IU / 0,4 ml roztwór do wstrzykiwań w ampułko-strzykawce (szklanej) - podskórne podanie dożylne - 0,4 ml (10000 IU/ml) - 6 ampułko-strzykawek po 0,4 ml z bezpiecznym urządzeniem igła - AIC N. 038190346 / E
Binocrit 5000 j.m./0,5 ml roztwór do wstrzykiwań w ampułko-strzykawce
EU / 1/07/410/009 - 5000 j.m. / 0,5 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) podanie podskórne lub dożylne 0,5 ml (10000 j.m./ml) 1 ampułkostrzykawka - AIC n. 038190094 / PL
EU / 1/07/410/010 - 5000 j.m. / 0,5 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) podanie podskórne lub dożylne 0,5 ml (10000 j.m./ml) 6 ampułkostrzykawek - AIC n. 038190106 / E
EU / 1/07/410/035 - 5000 IU / 0,5 ml roztwór do wstrzykiwań w ampułko-strzykawce (szklanej) - dożylnie podskórnie - 0,5 ml (10000 IU/ml) - 1 0,5 ml ampułkostrzykawka z zabezpieczoną igłą - AIC nr 038190359 / E
EU / 1/07/410/036 - 5000 IU / 0,5 ml roztwór do wstrzykiwań w ampułko-strzykawce (szklanej) - dożylne podanie podskórne - 0,5 ml (10000 IU/ml) - 6 ampułko-strzykawek po 0,5 ml z bezpiecznym urządzeniem do igły -AIC N. 038190361 / E
Binocrit 6000 j.m./0,6 ml roztwór do wstrzykiwań w ampułko-strzykawce
EU / 1/07/410/011 - 6000 j.m. / 0,6 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) podanie podskórne lub dożylne 0,6 ml (10 000 j.m./ml) 1 ampułkostrzykawka - AIC n . 038190118 / E
EU / 1/07/410/012 - 6000 j.m. / 0,6 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) do podania podskórnego lub dożylnego 0,6 ml (10 000 j.m./ml) 6 ampułkostrzykawek - AIC n . 038190120 / E
EU / 1/07/410/037 - 6000 IU / 0,6 ml roztwór do wstrzykiwań w ampułko-strzykawce (szklanej) - podskórne podanie dożylne - 0,6 ml (10000 IU/ml) - 1 ampułko-strzykawka 0,6 ml z bezpiecznym urządzeniem igła - AIC N. 038190373 / E
EU / 1/07/410/038 - 6000 IU / 0,6 ml roztwór do wstrzykiwań w ampułko-strzykawce (szklanej) - podskórne podanie dożylne - 0,6 ml (10 000 IU/ml) - 6 ampułko-strzykawek po 0 ,6 ml z bezpieczną igłą - AIC N. 038190385 / E
Binocrit 7000 j.m./0,7 ml roztwór do wstrzykiwań w ampułko-strzykawce
EU / 1/07/410/017 - 7000 IU / 0,7 ml roztwór do wstrzykiwań w ampułko-strzykawce - podanie podskórne lub dożylne - ampułko-strzykawka (szklana) 0,7 ml (10000 IU/ml) 1 ampułko-strzykawka - AIC nr 038190171 / AND
EU / 1/07/410/018 - 7000 IU / 0,7 ml roztwór do wstrzykiwań w ampułko-strzykawce - podanie podskórne lub dożylne - ampułko-strzykawka (szklana) 0,7 ml (10000 IU/ml) 6 ampułkostrzykawek - AIC Nie 038190183 / AND
EU / 1/07/410/039 - 7000 IU / 0,7 ml roztwór do wstrzykiwań w ampułko-strzykawce (szklanej) - podanie podskórne lub dożylne - 0,7 ml (10000 IU / ml) 1 ampułko-strzykawka 0,7 ml z urządzeniem zabezpieczającym na igła - AIC N. 038190397 / E
EU / 1/07/410/040 - 7000 IU / 0,7 ml roztwór do wstrzykiwań w ampułko-strzykawce (szklanej) - podanie podskórne lub dożylne - 0,7 ml (10000 IU/ml) 6 ampułko-strzykawek po 0,7 ml z urządzeniem zabezpieczającym na igła - AIC N. 038190409 / E
Binocrit 8000 j.m. / 0,8 ml roztwór do wstrzykiwań w ampułko-strzykawce
EU / 1/07/410/013 - 8000 IU / 0,8 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) do podania podskórnego lub dożylnego 0,8 ml (10 000 IU / ml) 1 ampułkostrzykawka - AIC n . 038190132 / E
EU / 1/07/410/014 - 8000 IU / 0,8 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) do podania podskórnego lub dożylnego 0,8 ml (10 000 IU / ml) 6 ampułkostrzykawek - AIC n . 038190144 / E
EU / 1/07/410/041 - 8000 IU / 0,8 ml roztwór do wstrzykiwań w ampułko-strzykawce (szklanej) - podskórne podanie dożylne - 0,8 ml (10000 IU/ml) - 1 ampułko-strzykawka 0,8 ml z bezpiecznym urządzeniem igła - AIC N. 038190411 / E
EU / 1/07/410/042 - 8000 IU / 0,8 ml roztwór do wstrzykiwań w ampułko-strzykawce (szklanej) - podskórne podanie dożylne - 0,8 ml (10000 IU/ml) - 6 ampułko-strzykawek po 0,8 ml z bezpiecznym urządzeniem igła - AIC N. 038190423 / E
Binocrit 9000 j.m. / 0,9 ml roztwór do wstrzykiwań w ampułko-strzykawce
EU / 1/07/410/019 - 9000 j.m. / 0,9 ml roztwór do wstrzykiwań w ampułko-strzykawce - do podania podskórnego lub dożylnego ampułko-strzykawka (szklana) 0,9 ml (10000 j.m./ml) 1 ampułko-strzykawka - AIC nr 038190195 / AND
EU / 1/07/410/020 - 9000IU / 0,9 ml roztwór do wstrzykiwań w ampułko-strzykawce - podanie podskórne lub dożylne - ampułkostrzykawka (szklana) 0,9 ml (10000UI/ml) 6 ampułkostrzykawek - AIC Nie 038190207 / AND
EU / 1/07/410/043 - 9000 IU / 0,9 ml roztwór do wstrzykiwań w ampułko-strzykawce (szklanej) - podanie podskórne lub dożylne - 0,9 ml (10000 IU / ml) 1 ampułko-strzykawka 0,9 ml z urządzeniem zabezpieczającym na igła - AIC N. 038190435 / E
EU / 1/07/410/044 - 9000 IU / 0,9 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) - podanie podskórne lub dożylne - 0,9 ml (10000 IU / ml) 6 ampułko-strzykawek po 0,9 ml z urządzeniem zabezpieczającym na igła - AIC N. 038190447 / E
Binocrit 10 000 j.m./1 ml roztwór do wstrzykiwań w ampułko-strzykawce
EU / 1/07/410/015 - 10000 IU / 1,0 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) Podanie podskórne lub dożylne 1,0 ml (10000 IU / ml) 1 ampułkostrzykawka - AIC n. 038190157 / E
EU / 1/07/410/016 - 10000 IU / 1,0 ml roztwór do wstrzykiwań w ampułko-strzykawce (szklanej) podanie podskórne lub dożylne 1,0 ml (10000 IU/ml) 6 ampułko-strzykawek - AIC n. 038190169 / E
EU / 1/07/410/045 - 10000 IU / 1 ml roztwór do wstrzykiwań w ampułko-strzykawce (szklanej) - podskórne podanie dożylne - 1 ml (10000 IU / ml) - 1 ampułko-strzykawka 1 ml z urządzeniem zabezpieczającym do igły - AIC N . 038190450 / E
EU / 1/07/410/046 - 10000 IU / 1 ml roztwór do wstrzykiwań w ampułko-strzykawce (szklanej) - podskórne podanie dożylne - 1 ml (10000 IU / ml) - 6 ampułko-strzykawek po 1 ml z urządzeniem zabezpieczającym do igły - AIC N . 038190462 / E
Binocrit 20 000 j.m./0,5 ml roztwór do wstrzykiwań w ampułko-strzykawce
EU / 1/07/410/021 - 20 000 j.m. / 0,5 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) - podanie podskórne lub dożylne 0,5 ml (40 000 j.m./ml) 1 ampułkostrzykawka - AIC n. 038190219 / E
EU / 1/07/410/022 - 20 000 j.m. / 0,5 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) - podanie podskórne lub dożylne 0,5 ml (40 000 j.m./ml) 6 ampułkostrzykawek - AIC n. 038190221 / E
EU / 1/07/410/047 - 20000 IU / 0,5 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) - podanie podskórne lub dożylne - 0,5 ml (40000 IU / ml) 1 0,5 ml ampułkostrzykawka z zabezpieczeniem na igłę - AIC nr 038190474 / E
EU / 1/07/410/053 - 20 000 j.m. / 0,5 ml - roztwór do wstrzykiwań w ampułko-strzykawce - podanie podskórne lub dożylne - ampułko-strzykawka (szklana) 0,5 ml (40 000 j.m. / ml) - 4 ampułko-strzykawki strzykawki z zabezpieczeniem urządzenia do igły AIC: 038190536 / E
EU / 1/07/410/048 - 20000 IU / 0,5 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) - podanie podskórne lub dożylne - 0,5 ml (40000 IU / ml) 6 ampułko-strzykawek po 0,5 ml z urządzeniem zabezpieczającym na igła - AIC N. 038190486 / E
Binocrit 30 000 j.m. / 0,75 ml roztwór do wstrzykiwań w ampułko-strzykawce
EU / 1/07/410/023 - 30 000 IU / 0,75 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) - podanie podskórne lub dożylne 0,75 ml (40 000 IU/ml) 1 ampułkostrzykawka - AIC n. 038190233 / E
EU / 1/07/410/024 - 30 000 IU / 0,75 ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) - podanie podskórne lub dożylne 0,75 ml (40000 IU/ml) 6 ampułkostrzykawek - AIC n. 038190245 / E
EU / 1/07/410/049 - 30000IU / 0,75ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) - podanie podskórne lub dożylne - 0,75ml (40000IU/ml) 1 ampułko-strzykawka 0,75ml z urządzeniem zabezpieczającym do Sierpień - AIC N. 038190498 / E
EU / 1/07/410/054 - 30 000 IU / 0,75 ML - roztwór do wstrzykiwań w ampułko-strzykawce - podanie podskórne lub dożylne - ampułko-strzykawka (szklana) 0,75 ML (40 000 IU / ML) - 4 ampułko-strzykawki strzykawki z zabezpieczeniem urządzenia do igły AIC: 038190548 / E
EU / 1/07/410/050 - 30000IU / 0,75ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) - podanie podskórne lub dożylne - 0,75ml (40000UI/ml) 6 ampułko-strzykawek po 0,75ml z urządzeniem zabezpieczającym na igła - AIC nr 038190500 / E
Binocrit 40 000 j.m./1 ml roztwór do wstrzykiwań w ampułko-strzykawce
EU / 1/07/410/025 - 40 000 IU / 1,0 ml - roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) - podanie podskórne lub dożylne - 1,0 ml (40000 IU/ml) 1 ampułkostrzykawka - AIC n. 038190258 / E
EU / 1/07/410/026 - 40 000 IU/1,0 ml - roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) - podanie podskórne lub dożylne - 1,0 ml (40000 IU/ml) 6 ampułkostrzykawek - AIC n. 038190260 / E
EU / 1/07/410/051 - 40000UI / 1ml roztwór do wstrzykiwań w ampułkostrzykawce (szklanej) - podanie podskórne lub dożylne - 1ml (40000IU/ml) 1 1ml ampułkostrzykawka z zabezpieczeniem igły - AIC N. 038190512 / E
EU / 1/07/410/055 - 40 000 IU / 1,0 ML - Roztwór do wstrzykiwań w ampułko-strzykawce - Podanie podskórne lub dożylne - Ampułkostrzykawka (szklana) 1,0 ML (40 000 IU / ML) - 4 ampułko-strzykawki strzykawki z bezpieczną igłą do igły AIC: 038190551 / E
EU / 1/07/410/052 - 40000UI / 1ml roztwór do wstrzykiwań w ampułko-strzykawce (szklanej) - podanie podskórne lub dożylne - 1ml (40000IU/ml) 6 ampułko-strzykawek po 1ml z zabezpieczeniem na igłę - AIC N. 038190524 / E
09.0 DATA PIERWSZEGO ZEZWOLENIA LUB PRZEDŁUŻENIA ZEZWOLENIA -
Od pierwszego zezwolenia: 28 sierpnia 2007 r.
Data ostatniego przedłużenia: 18 czerwca 2012 r.
10.0 DATA ZMIAN TEKSTU -
10/2016