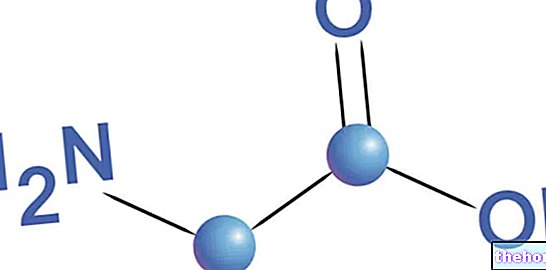
Składniki aktywne: Hydrokortyzon (fosforan sodu hydrokortyzonu)
CORTIVIS 0,3 ml krople do oczu
Dlaczego stosuje się Cortivis? Po co to jest?
Cortivis 0,3 ml krople do oczu, roztwór zawiera substancję czynną fosforan sodowy hydrokortyzonu. Fosforan sodowy hydrokortyzonu jest lekiem przeciwzapalnym należącym do grupy leków kortykosteroidowych.
Cortivis stosuje się w leczeniu chorób zapalnych i alergicznych przedniej części globu.
Przeciwwskazania Kiedy nie należy stosować Cortivis
Nie stosować leku Cortivis:
- Jeśli pacjent ma uczulenie na hydrokortyzon lub którykolwiek z pozostałych składników tego leku.
- Jeśli cierpisz na wysokie ciśnienie w oku.
- Jeśli masz „wirusową infekcję oka”.
- jeśli u pacjenta występuje „grzybicze (grzybicze) zakażenie oka” lub „zakażenie bakteryjne znane jako gruźlica
- Jeśli masz „infekcję oka”, która powoduje ropę, zapalenie brzegów powiek lub jęczmień.
Środki ostrożności dotyczące stosowania Informacje ważne przed zastosowaniem leku Cortivis
Przed rozpoczęciem stosowania leku Cortivis należy omówić to z lekarzem lub farmaceutą.
Stosowanie sterydów w stanach zapalnych rogówki (rogówki) pochodzenia wirusowego wymaga dużej ostrożności i może być dopuszczone tylko pod ścisłym nadzorem okulisty.
W chorobach powodujących ścieńczenie rogówki lub twardówki stosowanie miejscowych sterydów może spowodować perforację.
W przypadku braku poprawy klinicznej nie należy przedłużać stosowania kortykosteroidów, ponieważ może to przesłonić rozległość zakażenia ze względu na maskujące działanie steroidów. Ewentualną infekcję grzybiczą należy podejrzewać w przypadku owrzodzenia rogówki, w którym trwa lub było przedłużone leczenie steroidem.
Stosowanie kortykosteroidów nie powinno być powtarzane ani przedłużane bez odpowiedniej kontroli przez okulistę, aby wykluczyć wystąpienie poważnych działań niepożądanych, takich jak infekcje, powstawanie zaćmy lub zwiększone ciśnienie wewnętrzne w oku.
Należy zachować ostrożność podczas podawania kropli do oczu pacjentom w podeszłym wieku.
Interakcje Jakie leki lub pokarmy mogą zmienić działanie Cortivis
Należy powiedzieć lekarzowi lub farmaceucie, jeśli pacjent przyjmuje, ostatnio stosował lub może stosować jakiekolwiek inne leki.
Ostrzeżenia Ważne jest, aby wiedzieć, że:
Ciąża i karmienie piersią
Jeśli pacjentka jest w ciąży lub karmi piersią, podejrzewa, że może być w ciąży lub planuje mieć dziecko, powinna poradzić się lekarza lub farmaceuty przed zastosowaniem leku Cortivis.
Ciąża
Brak odpowiednich danych dotyczących miejscowego stosowania hydrokortyzonu fosforanu sodu u kobiet w ciąży. Badania na zwierzętach wykazały toksyczny wpływ na reprodukcję. CORTIVIS 0,3 ml krople do oczu, roztwór nie powinien być stosowany w okresie ciąży, chyba że jest to bezwzględnie konieczne.
Czas karmienia
Nie wiadomo, czy miejscowy fosforan sodowy hydrokortyzonu przenika do mleka ludzkiego.Wydzielanie fosforanu sodowego hydrokortyzonu po podaniu miejscowym nie było badane na zwierzętach.
Należy podjąć decyzję, czy przerwać karmienie piersią, czy przerwać leczenie preparatem CORTIVIS 0,3 ml, biorąc pod uwagę korzyści z karmienia piersią dla dziecka i korzyści z leczenia dla kobiety.
Prowadzenie i używanie maszyn
Cortivis 0,3 ml krople do oczu, roztwór nie ma wpływu na prowadzenie pojazdów i obsługę maszyn.
Dawkowanie i sposób stosowania Jak stosować Cortivis: Dawkowanie
Ten lek należy zawsze stosować zgodnie z zaleceniami lekarza lub farmaceuty. W razie wątpliwości skonsultuj się z lekarzem lub farmaceutą.
Zalecana dawka to 2 krople do oka 2 lub więcej razy dziennie, w zależności od ciężkości choroby.
Starsi mieszkańcy
Nie ma informacji sugerujących zmianę dawkowania u osób w podeszłym wieku, jednak należy zachować ostrożność, jeśli należysz do tej grupy pacjentów i powinieneś stosować ten lek.
Zwróć uwagę w przypadku osób starszych.
Nie należy stosować dawki podwójnej w celu uzupełnienia pominiętej dawki.
W przypadku konieczności przerwania leczenia należy natychmiast skontaktować się z lekarzem
Przedawkowanie Co zrobić, jeśli pacjent przyjął zbyt dużą dawkę leku Cortivis
W przypadku zastosowania większej niż zalecana dawki leku Cortivis należy natychmiast skontaktować się z lekarzem.
Skutki uboczne Jakie są skutki uboczne Cortivis
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Możliwe skutki uboczne to:
- zwiększone ciśnienie wewnątrz oka, które może powodować jaskrę;
- powstawanie zaćmy po długotrwałym leczeniu;
- rozwój lub pogorszenie opryszczki zwykłej lub grzybiczych infekcji bakteryjnych;
- opóźnione gojenie;
- bół głowy;
- obniżenie ciśnienia krwi;
- nieżyt nosa i zapalenie gardła.
Po długotrwałym stosowaniu mogą wystąpić poważne działania niepożądane (pogrubienie twardówki, rozszerzenie źrenicy, zwiotczenie powiek).
Przestrzeganie instrukcji zawartych w ulotce dołączonej do opakowania zmniejsza ryzyko wystąpienia działań niepożądanych
Zgłaszanie skutków ubocznych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie możliwe działania niepożądane niewymienione w tej ulotce, należy porozmawiać z lekarzem lub farmaceutą. Działania niepożądane można również zgłaszać bezpośrednio za pośrednictwem krajowego systemu zgłaszania pod adresem: www.agenziafarmaco.gov.it/it/responsabili Zgłaszanie działań niepożądanych może pomóc w uzyskaniu większej ilości informacji na temat bezpieczeństwa stosowania tego leku.
Wygaśnięcie i przechowywanie
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
Nie stosować tego leku po upływie terminu ważności zamieszczonego na pudełku po „Termin ważności”. Termin ważności odnosi się do ostatniego dnia tego miesiąca.
Termin ważności dotyczy produktu w nienaruszonym i prawidłowo przechowywanym opakowaniu.
Nie należy wyrzucać żadnych leków do kanalizacji ani domowych pojemników na odpadki. Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa.Pomoże to chronić środowisko.
Inne informacje
Co zawiera lek Cortivis
Substancją czynną jest fosforan sodu hydrokortyzonu.
Każdy pojemnik jednodawkowy zawiera 1,005 mg fosforanu sodowego hydrokortyzonu.
Pozostałe składniki to:
Sól sodowa kwasu hialuronowego, chlorek sodu, chlorek potasu, dwunastowodny dwuzasadowy fosforan sodu, dwuwodny jednozasadowy fosforan sodu, woda do wstrzykiwań.
Jak wygląda Cortivis i co zawiera opakowanie
Krople do oczu, roztwór 4 lub 6 saszetek zawierających 5 pojemników jednodawkowych po 0,33 ml.
Posiadacz pozwolenia na dopuszczenie do obrotu i producent.
Ulotka pakietu źródłowego: AIFA (Włoska Agencja Leków). Treść opublikowana w styczniu 2016 r. Przedstawione informacje mogą być nieaktualne.
Aby mieć dostęp do najbardziej aktualnej wersji, warto wejść na stronę AIFA (Włoskiej Agencji Leków). Zastrzeżenie i przydatne informacje.
01.0 NAZWA PRODUKTU LECZNICZEGO
CORTIVIS 0,3 ML KROPLE DO OCZU, ROZTWÓR
02.0 SKŁAD JAKOŚCIOWY I ILOŚCIOWY
Każdy pojemnik jednodawkowy zawiera:
Aktywna zasada
Fosforan sodowy hydrokortyzonu 1,005 mg.
Wykaz substancji pomocniczych, patrz punkt 6.1.
03.0 POSTAĆ FARMACEUTYCZNA
Krople do oczu, roztwór.
04.0 INFORMACJE KLINICZNE
04.1 Wskazania terapeutyczne
Zapalne i alergiczne schorzenia przedniej części gałki ocznej.
04.2 Dawkowanie i sposób podawania
Zaaplikować 2 krople (co odpowiada około 0,2 mg) do worka spojówkowego 2 lub więcej razy dziennie, w zależności od ciężkości choroby.
Starsi mieszkańcy
Nie ma informacji sugerujących zmianę dawkowania u osób w podeszłym wieku, jednak należy zachować ostrożność podczas podawania produktu leczniczego tej grupie pacjentów (patrz 4.4).
04.3 Przeciwwskazania
Nadwrażliwość na którykolwiek składnik produktu. Nadciśnienie oczne. Ostra opryszczka zwykła i choroby wirusowe rogówki w ostrej fazie wrzodziejącej, z wyjątkiem połączenia ze specyficznymi środkami chemioterapeutycznymi dla wirusa opryszczki, zapalenie spojówek z wrzodziejącym zapaleniem rogówki nawet w początkowej fazie. Gruźlica lub grzybica oka Ostre ropne zapalenie oka, ropne zapalenie spojówek oraz ropne i opryszczkowe zapalenie powiek, które mogą być maskowane lub zaostrzane przez leki przeciwzapalne.
04.4 Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania
Stosowanie sterydów w wirusowym opryszczkowym zapaleniu rogówki wymaga dużej ostrożności i może być dozwolone tylko pod ścisłym nadzorem okulisty.
W chorobach powodujących ścieńczenie rogówki lub twardówki stosowanie miejscowych sterydów może spowodować perforację.
W przypadku braku poprawy klinicznej nie należy przedłużać stosowania kortykosteroidów, ponieważ może to przesłonić rozległość zakażenia ze względu na maskujące działanie steroidów.
Ewentualną infekcję grzybiczą należy podejrzewać w przypadku owrzodzenia rogówki, w którym trwa lub było przedłużone leczenie steroidem.
Nie należy powtarzać ani przedłużać leczenia kortykosteroidami bez odpowiedniej kontroli, aby wykluczyć wystąpienie ciśnienia śródgałkowego i niepodejrzewanych zakażeń lub powstania zaćmy.
Należy zachować ostrożność podczas podawania kropli do oczu pacjentom w podeszłym wieku.
04.5 Interakcje z innymi produktami leczniczymi i inne formy interakcji
Nie są znane żadne interakcje.
04.6 Ciąża i laktacja
Brak odpowiednich danych dotyczących miejscowego stosowania hydrokortyzonu fosforanu sodu u kobiet w ciąży. Badania na zwierzętach wykazały szkodliwy wpływ na reprodukcję (patrz 5.3). CORTIVIS 0,3 ml krople do oczu, roztwór nie powinien być stosowany w okresie ciąży, chyba że jest to bezwzględnie konieczne.
Nie wiadomo, czy miejscowy fosforan sodowy hydrokortyzonu przenika do mleka ludzkiego.
Wydalanie fosforanu sodowego hydrokortyzonu po podaniu miejscowym nie było badane na zwierzętach.
Należy podjąć decyzję, czy kontynuować/przerwać karmienie piersią, czy też kontynuować/przerwać leczenie preparatem CORTIVIS 0,3 ml, biorąc pod uwagę korzyści z karmienia piersią dla dziecka i korzyści z leczenia dla kobiety.
04.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
CORTIVIS 0,3 ml krople do oczu, roztwór nie ma wpływu na zdolność prowadzenia pojazdów i obsługiwania maszyn.
04.8 Działania niepożądane
Podwyższone ciśnienie wewnątrzgałkowe z możliwym rozwojem jaskry; powstawanie zaćmy podtorebkowej tylnej po długotrwałym leczeniu; rozwój lub pogorszenie opryszczki zwykłej lub grzybiczych infekcji bakteryjnych; opóźnione gojenie; manifestacja, po długotrwałym podawaniu, poważnych skutków ubocznych, takich jak pogrubienie twardówki, rozszerzenie źrenic, rozluźnienie powiek.
Ponieważ po miejscowym zastosowaniu kortykosteroidów może wystąpić wchłanianie ogólnoustrojowe, mogą wystąpić ogólnoustrojowe działania niepożądane: ból głowy, niedociśnienie, nieżyt nosa i zapalenie gardła
04.9 Przedawkowanie
Nie zgłoszono żadnych przypadków przedawkowania.
05.0 WŁAŚCIWOŚCI FARMAKOLOGICZNE
05.1 Właściwości farmakodynamiczne
Kategoria terapeutyczna: przeciwzapalny.
Kod ATC: S01BA02.
Hydrokortyzon jest kortykosteroidem wytwarzanym przez nadnercza i ma właściwości przeciwzapalne.
Mechanizm działania na poziomie zapalenia gałki ocznej wynikałby z jej zdolności do indukowania syntezy lipokortyny, swoistego inhibitora fosfolipazy A2, blokując tym samym kaskadę kwasu arachidonowego i powstawanie czynników flogogennych, takich jak prostaglandyny, tromboksany i leukotrieny .
05.2 Właściwości farmakokinetyczne
Po podaniu do worka spojówkowego hydrokortyzon jest wchłaniany do cieczy wodnistej i może wystąpić wchłanianie ogólnoustrojowe. Jednakże, ponieważ dawka hydrokortyzonu w miejscowym preparacie okulistycznym jest znacznie niższa niż dawka stosowana ogólnoustrojowo, zwykle nie ma klinicznych dowodów na wchłanianie ogólnoustrojowe.
05.3 Przedkliniczne dane o bezpieczeństwie
Badania niekliniczne wykazały możliwość toksycznego wpływu na reprodukcję, ponieważ u myszy i królików leczonych kortykosteroidami stosowanymi do oka zgłaszano działanie teratogenne, takie jak rozszczep podniebienia i nieprawidłowości narządów płciowych.
06.0 INFORMACJE FARMACEUTYCZNE
06.1 Zaróbki
Sól sodowa kwasu hialuronowego, chlorek sodu, chlorek potasu, dwunastowodny dwuzasadowy fosforan sodu, dwuwodny jednozasadowy fosforan sodu, woda do wstrzykiwań.
06.2 Niezgodność
Nie są znane żadne niezgodności.
06.3 Okres ważności
2 lata.
06.4 Specjalne środki ostrożności przy przechowywaniu
Nic.
06.5 Rodzaj opakowania bezpośredniego i zawartość opakowania
Pudełko tekturowe zawierające 4 lub 6 zgrzewanych na gorąco torebek aluminiowych, z których każdy zawiera pasek 5 jednodawkowych pojemników z polietylenu o małej gęstości 0,33 ml.
06.6 Instrukcje użytkowania i obsługi
Nic.
07.0 PODMIOT POZWOLENIA NA DOPUSZCZENIE DO OBROTU
Medivis S.r.l. - Corso Italia, 171 - 95127 Katania - Włochy
08.0 NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
AIC nr. 038555013
AIC nr. 038555025
09.0 DATA PIERWSZEGO ZEZWOLENIA LUB PRZEDŁUŻENIA ZEZWOLENIA
21 października 2010
10.0 DATA ZMIAN TEKSTU
23 maja 2011