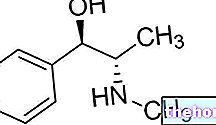
Składniki aktywne: Wildagliptyna
Galvus 50 mg tabletki
Wskazania Dlaczego stosuje się Galvus? Po co to jest?
Substancja czynna preparatu Galvus, wildagliptyna, należy do grupy leków zwanych doustnymi lekami przeciwcukrzycowymi.
Galvus stosuje się w leczeniu dorosłych pacjentów z cukrzycą typu 2. Stosuje się go, gdy nie można kontrolować cukrzycy wyłącznie za pomocą diety i ćwiczeń fizycznych.Pomaga on kontrolować poziom cukru we krwi.Lekarz zaleci sam lub razem Galvus.inne leki przeciwcukrzycowe już przyjmujesz, jeśli nie wykazano, że są one wystarczająco skuteczne w kontrolowaniu cukrzycy.
Cukrzyca typu 2 rozwija się, gdy organizm nie wytwarza wystarczającej ilości insuliny lub gdy wytwarzana przez organizm insulina nie działa tak, jak powinna.Może się również rozwinąć, gdy organizm wytwarza zbyt dużo glukagonu.
Insulina jest substancją, która pomaga obniżyć poziom cukru we krwi, zwłaszcza po posiłkach.Glukagon jest substancją, która uruchamia produkcję cukru przez wątrobę, powodując wzrost poziomu cukru we krwi.Trzustka produkuje obie te substancje.
Jak działa Galvus
Galvus działa, powodując, że trzustka produkuje więcej insuliny, a mniej glukagonu. Pomaga to kontrolować poziom cukru we krwi. Wykazano, że lek ten obniża poziom cukru we krwi. Pomoże to zapobiec powikłaniom związanym z cukrzycą. Nawet jeśli już teraz zaczniesz brać leki na cukrzycę, ważne jest, aby nadal przestrzegać zalecanej diety i / lub ćwiczeń.
Przeciwwskazania Kiedy nie należy stosować leku Galvus
Nie stosować leku Galvus:
- jeśli pacjent ma uczulenie na wildagliptynę lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6). Jeśli pacjent uważa, że może być uczulony na wildagliptynę lub którykolwiek z pozostałych składników leku Galvus, nie powinien przyjmować tego leku i powinien skontaktować się z lekarzem.
Środki ostrożności dotyczące stosowania Informacje ważne przed zastosowaniem leku Galvus
Przed rozpoczęciem stosowania leku Galvus . należy omówić to z lekarzem, farmaceutą lub pielęgniarką diabetologiczną
- jeśli u pacjenta występuje cukrzyca typu 1 (organizm nie wytwarza insuliny) lub jeśli u pacjenta występuje stan zwany cukrzycową kwasicą ketonową.
- jeśli pacjent przyjmuje lek przeciwcukrzycowy zwany sulfonylomocznikiem (jeśli przyjmuje się go razem z lekiem Galvus, lekarz może zmniejszyć dawkę sulfonylomocznika, aby uniknąć niskiego stężenia glukozy we krwi [hipoglikemia]).
- jeśli u pacjenta występuje umiarkowana lub ciężka choroba nerek (trzeba zastosować mniejszą dawkę leku Galvus).
- jeśli jesteś na dializie
- jeśli u pacjenta występuje choroba wątroby
- jeśli cierpisz na niewydolność serca
- jeśli masz lub kiedykolwiek miałeś chorobę trzustki
Jeśli pacjent przyjmował wcześniej wildagliptynę, ale musiał przerwać leczenie z powodu choroby wątroby, nie powinien przyjmować tego leku.
Zmiany skórne są częstym powikłaniem cukrzycy. Zaleca się przestrzeganie zaleceń dotyczących pielęgnacji skóry i stóp podanych przez lekarza lub pielęgniarkę, a także zwracanie szczególnej uwagi na powstawanie pęcherzy lub owrzodzeń podczas stosowania leku Galvus. W takim przypadku należy szybko skonsultować się z lekarzem.
Przed rozpoczęciem leczenia preparatem Galvus zostanie przeprowadzone badanie w celu oceny czynności wątroby, które będzie powtarzane co trzy miesiące przez pierwszy rok leczenia, a następnie okresowo. Ma to na celu jak najszybsze wykrycie oznak zwiększonej aktywności enzymów wątrobowych.
Dzieci i młodzież
Nie zaleca się stosowania leku Galvus u dzieci i młodzieży w wieku do 18 lat.
Interakcje Jakie leki lub pokarmy mogą modyfikować działanie leku Galvus
Należy powiedzieć lekarzowi lub farmaceucie, jeśli pacjent przyjmuje, ostatnio przyjmował lub może przyjmować jakiekolwiek inne leki.
Lekarz może chcieć zmienić dawkę leku Galvus, jeśli pacjent przyjmuje inne leki, takie jak:
- tiazydy lub inne leki moczopędne (zwane również tabletkami do oddawania moczu) - kortykosteroidy (zwykle stosowane w leczeniu stanów zapalnych)
- leki na tarczycę
- niektóre leki wpływające na układ nerwowy.
Ostrzeżenia Ważne jest, aby wiedzieć, że:
Ciąża i karmienie piersią
Jeśli pacjentka jest w ciąży lub karmi piersią, podejrzewa, że może być w ciąży lub planuje mieć dziecko, powinna poradzić się lekarza lub farmaceuty przed zastosowaniem tego leku.
Nie wolno stosować leku Galvus w okresie ciąży. Nie wiadomo, czy Galvus przenika do mleka matki. Nie należy stosować leku Galvus, jeśli pacjentka karmi piersią lub planuje karmić piersią.
Prowadzenie i używanie maszyn
W przypadku wystąpienia zawrotów głowy podczas przyjmowania leku Galvus nie należy prowadzić pojazdów ani obsługiwać maszyn.
Galvus zawiera laktozę
Galvus zawiera laktozę (cukier mleczny). Jeśli pacjent został poinformowany przez lekarza, że nie toleruje niektórych cukrów, powinien skontaktować się z lekarzem przed przyjęciem tego produktu leczniczego.
Dawka, sposób i czas podania Jak stosować Galvus: dawkowanie
Lek należy zawsze stosować zgodnie z zaleceniami lekarza. W razie wątpliwości skonsultuj się z lekarzem lub farmaceutą.
Ile wziąć i kiedy
Ilość Galvus, którą należy przyjąć, różni się w zależności od indywidualnych warunków. Lekarz poinformuje pacjenta, ile tabletek Galvus należy zażywać. Maksymalna dzienna dawka to 100 mg.
Zazwyczaj stosowana dawka leku Galvus to:
- 50 mg na dobę przyjmowane jako pojedyncza dawka rano, jeśli lek Galvus jest przyjmowany z innym lekiem o nazwie sulfonylomocznik.
- 100 mg na dobę przyjmowane jako 50 mg rano i 50 mg wieczorem w przypadku przyjmowania leku Galvus w monoterapii, z innym lekiem zwanym metforminą lub glitazonem, w skojarzeniu z metforminą i pochodną sulfonylomocznika lub z insuliną.
- 50 mg na dobę rano, jeśli u pacjenta występuje umiarkowana lub ciężka choroba nerek lub pacjent jest dializowany.
Jak zażywać Galvus
- Tabletki połknąć, popijając wodą.
Jak długo należy przyjmować lek Galvus
- Lek Galvus należy przyjmować codziennie, tak długo, jak zaleci lekarz. Być może będziesz musiał kontynuować to leczenie przez długi czas.
- Twój lekarz będzie regularnie sprawdzał Twój stan zdrowia, aby upewnić się, że leczenie przynosi oczekiwany efekt.
Pominięcie przyjęcia leku Galvus
Jeśli zapomnisz przyjąć dawkę tego leku, zażyj ją tak szybko, jak sobie o tym przypomnisz. Następnie przyjąć następną dawkę o zwykłej porze. Jeśli zbliża się pora przyjęcia następnej dawki, należy pominąć pominiętą dawkę.Nie należy stosować dawki podwójnej w celu uzupełnienia pominiętej tabletki.
Przerwanie stosowania leku Galvus
Nie należy przerywać przyjmowania leku Galvus, chyba że tak zaleci lekarz. Jeśli nie masz pewności, jak długo będziesz przyjmować ten lek, zapytaj lekarza.
Przedawkowanie Co zrobić, jeśli pacjent przyjął zbyt dużą dawkę leku Galvus
W przypadku zażycia zbyt wielu tabletek Galvus lub w przypadku zażycia leku przez inną osobę, należy natychmiast skontaktować się z lekarzem. Może być wymagana pomoc medyczna. Jeśli potrzebujesz udać się do lekarza lub do szpitala, zabierz ze sobą opakowanie.
Skutki uboczne Jakie są skutki uboczne Galvus
Jak każdy lek, lek ten może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Niektóre objawy wymagają natychmiastowej pomocy lekarskiej:
Należy przerwać przyjmowanie leku Galvus i natychmiast skontaktować się z lekarzem, jeśli wystąpi którekolwiek z poniższych działań niepożądanych:
- Obrzęk naczynioruchowy (rzadko: może dotyczyć nie więcej niż 1 na 1000 osób): Objawy obejmują obrzęk twarzy, języka lub gardła, trudności w przełykaniu, trudności w oddychaniu, nagłą wysypkę lub pokrzywkę, które mogą wskazywać na reakcję zwaną „obrzękiem naczynioruchowym”.
- Choroba wątroby (zapalenie wątroby) (rzadko): Objawy obejmują zażółcenie skóry i oczu, nudności, utratę apetytu lub ciemne zabarwienie moczu, które mogą wskazywać na chorobę wątroby (zapalenie wątroby).
- Zapalenie trzustki (zapalenie trzustki) (częstość nieznana). Objawy obejmują silny i uporczywy ból brzucha (w okolicy żołądka), który może rozciągać się na plecy, a także nudności i wymioty.
Inne skutki uboczne
U niektórych pacjentów podczas przyjmowania leku Galvus i metforminy wystąpiły następujące działania niepożądane:
- Często (mogą wystąpić u nie więcej niż 1 na 10 osób): drżenie, ból głowy, zawroty głowy, nudności, niski poziom glukozy we krwi.
- Niezbyt często (mogą dotyczyć do 1 na 100 osób): zmęczenie.
U niektórych pacjentów podczas przyjmowania leku Galvus i sulfonylomocznika wystąpiły następujące działania niepożądane:
- Często: drżenie, ból głowy, zawroty głowy, osłabienie, niski poziom glukozy we krwi.
- Niezbyt często: zaparcia.
- Bardzo rzadko (mogą dotyczyć do 1 na 10 000 osób): ból gardła, katar.
U niektórych pacjentów podczas przyjmowania leku Galvus i glitazonu wystąpiły następujące działania niepożądane:
- Często: przyrost masy ciała, obrzęk rąk, kostek lub stóp (obrzęk).
- Niezbyt często: ból głowy, osłabienie, niski poziom glukozy we krwi.
U niektórych pacjentów podczas stosowania samego leku Galvus wystąpiły następujące działania niepożądane:
- Często: zawroty głowy.
- Niezbyt często: ból głowy, zaparcia, obrzęk rąk, kostek lub stóp (obrzęk), ból stawów, niski poziom glukozy we krwi.
- Bardzo rzadko: ból gardła, katar, gorączka.
U niektórych pacjentów podczas przyjmowania leku Galvus, metforminy i sulfonylomocznika wystąpiły następujące działania niepożądane:
- Często: zawroty głowy, drżenie, osłabienie, niski poziom glukozy we krwi, nadmierne pocenie się.
U niektórych pacjentów podczas przyjmowania leku Galvus i insuliny (z metforminą lub bez) wystąpiły następujące działania niepożądane:
- Często: ból głowy, dreszcze, nudności (mdłości), niski poziom glukozy we krwi, zgaga.
- Niezbyt często: biegunka, wzdęcia.
Podczas wprowadzania do obrotu tego leku zgłaszano również następujące działania niepożądane:
- Częstość nieznana (nie może być określona na podstawie dostępnych danych): swędząca wysypka, zapalenie trzustki, miejscowe złuszczanie się skóry lub pęcherze, ból mięśni.
Zgłaszanie skutków ubocznych
Jeśli wystąpią jakiekolwiek działania niepożądane, należy porozmawiać z lekarzem, farmaceutą lub pielęgniarką diabetologiczną, w tym wszelkie możliwe działania niepożądane niewymienione w tej ulotce.Można również zgłaszać działania niepożądane bezpośrednio za pośrednictwem krajowego systemu zgłaszania wymienionego w załączniku V. Zgłaszanie działań niepożądanych możesz pomóc dostarczyć więcej informacji na temat bezpieczeństwa tego leku.
Wygaśnięcie i przechowywanie
- Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci.
- Nie stosować tego leku po upływie terminu ważności zamieszczonego na blistrze i pudełku po „EXP” / „EXP”. Termin ważności odnosi się do ostatniego dnia tego miesiąca.
- Przechowywać w oryginalnym opakowaniu w celu ochrony przed wilgocią.
- Nie używać opakowania Galvus, które jest uszkodzone lub nosi ślady ingerencji.
Wygaśnięcie "> Inne interakcje
Co zawiera Galvus
- Substancją czynną jest wildagliptyna. Każda tabletka zawiera 50 mg wildagliptyny.
- Pozostałe składniki to: laktoza bezwodna, celuloza mikrokrystaliczna, glikolan sodowy skrobi (typ A) i stearynian magnezu.
Opis wyglądu leku Galvus i co zawiera opakowanie
Tabletki Galvus 50 mg są okrągłe, płaskie, białe do lekko żółtawego, z napisem „NVR” po jednej stronie i „FB” po drugiej stronie.
Tabletki Galvus 50 mg są dostępne w opakowaniach zawierających 7, 14, 28, 30, 56, 60, 90, 112, 180 lub 336 tabletek oraz w opakowaniach zbiorczych zawierających 3 kartony, z których każde zawiera 112 tabletek.
Nie wszystkie wielkości opakowań mogą być sprzedawane w Twoim kraju.
Ulotka pakietu źródłowego: AIFA (Włoska Agencja Leków). Treść opublikowana w styczniu 2016 r. Przedstawione informacje mogą być nieaktualne.
Aby mieć dostęp do najbardziej aktualnej wersji, warto wejść na stronę AIFA (Włoskiej Agencji Leków). Zastrzeżenie i przydatne informacje.
01.0 NAZWA PRODUKTU LECZNICZEGO -
GALVUS 50 MG TABLETKI
02.0 SKŁAD JAKOŚCIOWY I ILOŚCIOWY -
Każda tabletka zawiera 50 mg wildagliptyny.
Substancja pomocnicza o znanym działaniu: każda tabletka zawiera 47,82 mg laktozy (bezwodnej).
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
03.0 POSTAĆ FARMACEUTYCZNA -
Tablet.
Okrągła (średnica 8 mm), biała do lekko żółtawej, płaska tabletka ze ściętymi krawędziami.
Litery „NVR” są wytłoczone z jednej strony, a „FB” z drugiej.
04.0 INFORMACJE KLINICZNE -
04.1 Wskazania terapeutyczne -
Vildagliptyna jest wskazana w leczeniu cukrzycy typu 2 u dorosłych:
W monoterapii
- u pacjentów niedostatecznie kontrolowanych wyłącznie dietą i ćwiczeniami fizycznymi, u których leczenie metforminą jest nieodpowiednie z powodu przeciwwskazań lub nietolerancji.
W podwójnej terapii doustnej w połączeniu z:
- metformina, u pacjentów z niedostateczną kontrolą glikemii pomimo podania maksymalnej tolerowanej dawki samej metforminy,
- pochodną sulfonylomocznika, u pacjentów z niedostateczną kontrolą glikemii pomimo podania maksymalnej tolerowanej dawki sulfonylomocznika i u których leczenie metforminą jest nieodpowiednie z powodu przeciwwskazań lub nietolerancji,
- tiazolidynodion u pacjentów z niewystarczającą kontrolą glikemii, u których wskazane jest zastosowanie tiazolidynodionu.
W potrójnej terapii doustnej w połączeniu z:
- sulfonylomocznik i metformina, gdy dieta i ćwiczenia związane z podwójną terapią tymi lekami nie zapewniają odpowiedniej kontroli glikemii.
Vildagliptyna jest również wskazana do stosowania w skojarzeniu z insuliną (z metforminą lub bez), gdy dieta i wysiłek fizyczny w połączeniu ze stałą dawką insuliny nie zapewniają odpowiedniej kontroli glikemii.
04.2 Dawkowanie i sposób podawania -
Dawkowanie
Dorośli ludzie
W przypadku stosowania samodzielnie, w skojarzeniu z metforminą, w skojarzeniu z tiazolidynodionem, w skojarzeniu z metforminą i pochodną sulfonylomocznika lub w skojarzeniu z insuliną (z metforminą lub bez), zalecana dawka dobowa wildagliptyny wynosi 100 mg, podawana w jednej dawce. 50 mg rano i 50 mg wieczorem.
W przypadku stosowania w terapii podwójnej w skojarzeniu z sulfonylomocznikiem zalecana dawka wildagliptyny wynosi 50 mg raz na dobę, podawana rano. W tej populacji pacjentów wildagliptyna w dawce 100 mg na dobę nie była bardziej skuteczna niż wildagliptyna w dawce 50 mg raz na dobę.
W przypadku stosowania w skojarzeniu z pochodną sulfonylomocznika można rozważyć zmniejszenie dawki sulfonylomocznika w celu zmniejszenia ryzyka hipoglikemii.
Nie zaleca się dawek powyżej 100 mg.
W przypadku pominięcia dawki leku Galvus należy ją przyjąć, gdy tylko pacjent sobie o tym przypomni.
Nie należy przyjmować podwójnej dawki tego samego dnia.
Nie ustalono bezpieczeństwa i skuteczności wildagliptyny w potrójnej terapii doustnej w skojarzeniu z metforminą i tiazolidynodionem.
Dodatkowe informacje dla poszczególnych populacji pacjentów
Osoby w podeszłym wieku (≥ 65 lat)
Nie ma konieczności dostosowania dawki u pacjentów w podeszłym wieku (patrz również punkty 5.1 i 5.2).
Upośledzona czynność nerek
Nie ma konieczności dostosowania dawki u pacjentów z łagodnymi zaburzeniami czynności nerek (luz kreatynina ≥ 50 ml/min). U pacjentów z umiarkowanymi lub ciężkimi zaburzeniami czynności nerek lub schyłkową niewydolnością nerek (ESRD) zalecana dawka produktu Galvus wynosi 50 mg raz na dobę (patrz również punkty 4.4, 5.1 i 5.2).
Upośledzona czynność wątroby
Preparatu Galvus nie należy stosować u pacjentów z zaburzeniami czynności wątroby, w tym u pacjentów, u których przed leczeniem aktywność aminotransferazy alaninowej (AlAT) lub asparaginianowej (AspAT) przekracza trzykrotnie górną granicę normy (GGN) (patrz również punkty 4.4 i 5.2).
Populacja pediatryczna
Nie zaleca się stosowania leku Galvus u dzieci i młodzieży (
Sposób podawania
Stosowanie doustne
Galvus można przyjmować z posiłkiem lub bez posiłku (patrz również punkt 5.2).
04.3 Przeciwwskazania -
Nadwrażliwość na substancję czynną lub na którąkolwiek substancję pomocniczą wymienioną w punkcie 6.1.
04.4 Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania -
Ogólny
Galvus nie zastępuje insuliny u pacjentów insulinozależnych.Galvus nie powinien być stosowany u pacjentów z cukrzycą typu 1 ani w leczeniu cukrzycowej kwasicy ketonowej.
Upośledzona czynność nerek
Doświadczenie u pacjentów poddawanych hemodializie z ESRD jest ograniczone, dlatego produkt Galvus należy stosować ostrożnie u tych pacjentów (patrz również punkty 4.2, 5.1 i 5.2).
Upośledzona czynność wątroby
Produktu Galvus nie należy stosować u pacjentów z zaburzeniami czynności wątroby, w tym u pacjentów, u których aktywność AlAT lub AspAT przed leczeniem przekraczała 3x GGN (patrz również punkty 4.2 i 5.2).
Monitorowanie enzymów wątrobowych
Zgłaszano rzadkie przypadki zaburzeń czynności wątroby (w tym zapalenia wątroby). W tych przypadkach pacjenci byli na ogół bezobjawowi, bez następstw klinicznych, a wyniki testów czynności wątroby powróciły do normy po przerwaniu leczenia. Testy czynności wątroby należy wykonać przed rozpoczęciem leczenia produktem Galvus, aby poznać wartość wyjściową pacjenta. Podczas leczenia preparatem Galvus czynność wątroby należy kontrolować co trzy miesiące w pierwszym roku leczenia, a następnie okresowo. Pacjenci, u których wystąpi podwyższony poziom transaminaz, powinni zostać poddani ponownej ocenie czynności wątroby w celu potwierdzenia wyników, a następnie częstymi próbami czynności wątroby, aż do powrotu nieprawidłowości do normy. Jeśli wzrost AspAT lub AlAT utrzymuje się na poziomie 3-krotności górnej granicy normy lub powyżej, zaleca się przerwanie leczenia produktem Galvus.
Po przerwaniu leczenia Galvus i normalizacji parametrów czynności wątroby, nie należy wznawiać leczenia Galvus.
Niewydolność serca
Badanie kliniczne wildagliptyny u pacjentów w klasach czynnościowych I-III New York Heart Association (NYHA) wykazało, że leczenie wildagliptyną nie było związane ze zmianami w czynności lewej komory lub pogorszeniem istniejącej zastoinowej niewydolności serca (CHF) w porównaniu z placebo. doświadczenie u pacjentów w klasie czynnościowej III wg NYHA leczonych wildagliptyną jest nadal ograniczone, a wyniki nie są jednoznaczne (patrz punkt 5.1).
Nie ma doświadczenia ze stosowaniem wildagliptyny w badaniach klinicznych u pacjentów z IV klasą czynnościową wg NYHA i dlatego nie zaleca się jej stosowania u tych pacjentów.
Schorzenia skóry
W nieklinicznych badaniach toksykologicznych zgłaszano zmiany skórne na kończynach małp, w tym pęcherze i owrzodzenia (patrz punkt 5.3). Chociaż w badaniach klinicznych nie zaobserwowano „zwiększonej częstości występowania zmian skórnych”, doświadczenie u pacjentów ze skórnymi powikłaniami cukrzycowymi było ograniczone. Ponadto pojawiły się doniesienia po wprowadzeniu do obrotu o pęcherzowych i złuszczających się zmianach skórnych. Zgodnie z rutynową opieką nad pacjentem z cukrzycą zaleca się zatem monitorowanie wszelkich chorób skóry, takich jak pęcherze i owrzodzenia.
Ostre zapalenie trzustki
Stosowanie wildagliptyny wiązało się z ryzykiem rozwoju ostrego zapalenia trzustki.Pacjentów należy poinformować o charakterystycznych objawach ostrego zapalenia trzustki.
W przypadku podejrzenia zapalenia trzustki wildagliptynę należy odstawić; w przypadku potwierdzenia ostrego zapalenia trzustki nie należy wznawiać stosowania wildagliptyny. Należy zachować ostrożność u pacjentów z ostrym zapaleniem trzustki w wywiadzie.
Hipoglikemia
Wiadomo, że sulfonylomoczniki powodują hipoglikemię. Pacjenci otrzymujący wildagliptynę w skojarzeniu z sulfonylomocznikiem mogą być narażeni na ryzyko hipoglikemii. W związku z tym można rozważyć zastosowanie mniejszej dawki sulfonylomocznika w celu zmniejszenia ryzyka hipoglikemii.
Substancje pomocnicze
Tabletki zawierają laktozę. Pacjenci z rzadką dziedziczną nietolerancją galaktozy, niedoborem laktazy typu Lapp lub zespołem złego wchłaniania glukozy-galaktozy nie powinni przyjmować tego leku.
04.5 Interakcje z innymi produktami leczniczymi i inne formy interakcji -
Wildagliptyna ma niski potencjał interakcji w połączeniu z innymi produktami leczniczymi. Ponieważ wildagliptyna nie jest substratem enzymu cytochromu P (CYP) 450 i nie hamuje ani nie indukuje enzymów CYP 450, interakcje z substancjami czynnymi będącymi substratami, inhibitorami lub induktorami tych enzymów są mało prawdopodobne.
Połączenie z pioglitazonem, metforminą i glibenklamidem
Wyniki badań przeprowadzonych z tymi doustnymi lekami przeciwcukrzycowymi nie wykazały klinicznie istotnych interakcji farmakokinetycznych.
Digoksyna (substrat glikoproteiny p), warfaryna (substrat CYP2C9)
Badania kliniczne przeprowadzone z udziałem zdrowych osób nie wykazały klinicznie istotnych interakcji farmakokinetycznych. Jednak dowody te nie zostały potwierdzone w populacji referencyjnej.
Skojarzenie z amlodypiną, ramiprylem, walsartanem lub simwastatyną
Badania interakcji typu lek-lek przeprowadzono z użyciem amlodypiny, ramiprylu, walsartanu i symwastatyny u zdrowych osób. W badaniach tych nie zaobserwowano klinicznie istotnych interakcji farmakokinetycznych po jednoczesnym podaniu z wildagliptyną.
Podobnie jak w przypadku innych doustnych leków przeciwcukrzycowych, działanie hipoglikemizujące wildagliptyny może być osłabiane przez niektóre substancje czynne, w tym tiazydy, kortykosteroidy, leki na tarczycę i sympatykomimetyki.
04.6 Ciąża i karmienie piersią -
Ciąża
Brak odpowiednich danych dotyczących stosowania wildagliptyny u kobiet w ciąży Badania na zwierzętach wykazały szkodliwy wpływ na reprodukcję dużych dawek (patrz punkt 5.3). Potencjalne ryzyko dla ludzi nie jest znane. Ze względu na brak danych dotyczących ludzi, Galvus nie powinien być stosowany podczas ciąża.
Czas karmienia
Nie wiadomo, czy wildagliptyna przenika do mleka ludzkiego. Badania na zwierzętach wykazały przenikanie wildagliptyny do mleka.Galvus nie powinien być stosowany w okresie laktacji.
Płodność
Nie przeprowadzono badań dotyczących wpływu produktu Galvus na płodność u ludzi (patrz punkt 5.3).
04.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn -
Nie przeprowadzono badań dotyczących zdolności prowadzenia pojazdów i obsługiwania maszyn.Pacjenci, u których jako działanie niepożądane występują zawroty głowy, powinni unikać prowadzenia pojazdów i obsługiwania maszyn.
04.8 Działania niepożądane -
Podsumowanie profilu bezpieczeństwa
Dane dotyczące bezpieczeństwa uzyskano od 3784 pacjentów otrzymujących dawki dobowe wildagliptyny 50 mg (raz na dobę) lub 100 mg (50 mg dwa razy na dobę lub 100 mg raz na dobę) w badaniach kontrolowanych trwających co najmniej 12 tygodni. Spośród tych pacjentów 2264 otrzymywało samą wildagliptynę, a 1520 otrzymywało wildagliptynę w skojarzeniu z innym lekiem. 2682 pacjentów leczono wildagliptyną w dawce 100 mg na dobę (50 mg dwa razy na dobę lub 100 mg raz na dobę), a 1102 pacjentów leczono wildagliptyną w dawce 50 mg raz na dobę.
Większość działań niepożądanych w tych badaniach klinicznych miała łagodny i przemijający charakter i nie wymagała przerwania leczenia.Nie stwierdzono związku między działaniami niepożądanymi a wiekiem, pochodzeniem etnicznym, czasem ekspozycji lub dawką dobową.
Zgłaszano rzadkie przypadki zaburzeń czynności wątroby (w tym zapalenia wątroby). W tych przypadkach pacjenci byli na ogół bezobjawowi, bez następstw klinicznych, a wyniki testów czynności wątroby powróciły do normy po przerwaniu leczenia. Na podstawie danych z kontrolowanych badań dotyczących monoterapii lub terapii dodanej trwających do 24 tygodni, częstość występowania podwyższonej aktywności AlAT lub AspAT ≥ 3 razy powyżej górnej granicy normy (sklasyfikowana jako obecna w co najmniej 2 kolejnych kontrolach lub podczas wizyty końcowej podczas leczenia) wynosiły odpowiednio 0,2%, 0,3% i 0,2% dla wildagliptyny 50 mg raz na dobę, wildagliptyny 50 mg dwa razy na dobę i wszystkich leków porównawczych.Podwyższenie aktywności aminotransferaz było na ogół bezobjawowe, nie postępujące i nie było związane z cholestazą ani żółtaczką.
Rzadkie przypadki obrzęku naczynioruchowego były zgłaszane po zastosowaniu wildagliptyny, z częstością podobną do grupy kontrolnej.Większość przypadków zgłoszono, gdy wildagliptyna była podawana w skojarzeniu z inhibitorem enzymu angiotensyny (inhibitor ACE). Większość zdarzeń miała umiarkowane nasilenie i ustępowała podczas leczenia wildagliptyną.
Tabela działań niepożądanych
Działania niepożądane zgłaszane u pacjentów, którzy otrzymywali Galvus w badaniach z podwójnie ślepą próbą w monoterapii i terapii dodanej, są wymienione poniżej dla każdego wskazania według klasyfikacji układów i narządów oraz bezwzględnej częstości występowania. Częstotliwości są zdefiniowane jako bardzo częste (≥1/10), częste (≥1/100,
Połączenie z metforminą
Tabela 1 Działania niepożądane zgłaszane u pacjentów, którzy otrzymywali Galvus 100 mg na dobę w skojarzeniu z metforminą w badaniach z podwójnie ślepą próbą (N = 208)
Opis wybranych działań niepożądanych
W kontrolowanych badaniach klinicznych przeprowadzonych z zastosowaniem kombinacji wildagliptyna 100 mg na dobę + metformina, nie zgłoszono wycofań z powodu działań niepożądanych ani w grupie wildagliptyny 100 mg na dobę + metformina, ani w grupie placebo + metformina. często u pacjentów otrzymujących wildagliptynę w dawce 100 mg na dobę w skojarzeniu z metforminą (1%) i niezbyt często u pacjentów otrzymujących placebo + metforminę (0,4%). W ramionach wildagliptyny nie zgłoszono żadnych poważnych zdarzeń hipoglikemicznych.
W badaniach klinicznych masa ciała nie zmieniła się w stosunku do wartości wyjściowej po dodaniu wildagliptyny w dawce 100 mg na dobę do metforminy (odpowiednio +0,2 kg i -1,0 kg dla wildagliptyny i placebo).
Badania kliniczne trwające do ponad 2 lat nie wykazały żadnych dodatkowych sygnałów dotyczących bezpieczeństwa ani nieprzewidzianych zagrożeń, gdy wildagliptyna była połączona z metforminą.
Połączenie z sulfonylomocznikiem
Tabela 2 Działania niepożądane zgłaszane u pacjentów, którzy otrzymali 50 mg produktu Galvus w skojarzeniu z pochodną sulfonylomocznika w badaniach z podwójnie ślepą próbą (N = 170)
Opis wybranych działań niepożądanych
W kontrolowanych badaniach klinicznych przeprowadzonych z zastosowaniem kombinacji wildagliptyna 50 mg + pochodne sulfonylomocznika, całkowita częstość odstawienia z powodu działań niepożądanych wynosiła 0,6% w grupie wildagliptyny 50 mg + pochodnej sulfonylomocznika w porównaniu do 0% w grupie otrzymującej placebo + sulfonylomocznik.
W badaniach klinicznych, gdy wildagliptyna w dawce 50 mg raz na dobę była dodawana do glimepirydu, częstość występowania hipoglikemii wynosiła 1,2% w porównaniu z 0,6% w przypadku placebo + glimepirydu.
W badaniach klinicznych masa ciała nie zmieniła się w stosunku do wartości wyjściowej po dodaniu wildagliptyny w dawce 50 mg na dobę do glimepirydu (odpowiednio -0,1 kg i -0,4 kg dla wildagliptyny i placebo).
Skojarzenie z tiazolidynodionem
Tabela 3 Działania niepożądane zgłaszane u pacjentów otrzymujących 100 mg preparatu Galvus na dobę w skojarzeniu z tiazolidynodionem w badaniach z podwójnie ślepą próbą (N = 158)
Opis wybranych działań niepożądanych
W kontrolowanych badaniach klinicznych przeprowadzonych ze skojarzeniem wildagliptyna 100 mg na dobę + tiazolidynodion, zarówno w grupie wildagliptyny 100 mg na dobę + tiazolidynodion, jak i placebo + tiazolidynodion, nie zgłoszono przypadków wycofania leku z powodu działań niepożądanych. niezbyt często u pacjentów, którzy otrzymywali wildagliptynę + pioglitazon (0,6%), podczas gdy było to częste u pacjentów otrzymujących placebo + pioglitazon (1,9%). W ramionach wildagliptyny nie zgłoszono żadnych poważnych zdarzeń hipoglikemicznych. W badaniach dodatkowych z pioglitazonem bezwzględny przyrost masy ciała po zastosowaniu placebo i 100 mg preparatu Galvus na dobę wynosił odpowiednio 1,4 i 2,7 kg.
Częstość występowania obrzęków obwodowych po dodaniu wildagliptyny w dawce 100 mg na dobę do terapii podstawowej pioglitazonem w maksymalnej dawce (45 mg raz na dobę) wynosiła 7,0% w porównaniu z 2,5% w przypadku samego pioglitazonu.
Monoterapia
Tabela 4 Działania niepożądane zgłaszane u pacjentów, którzy otrzymywali Galvus 100 mg na dobę w monoterapii w badaniach z podwójnie ślepą próbą (N = 1855)
Opis wybranych działań niepożądanych
Ponadto w kontrolowanych badaniach klinicznych przeprowadzonych z zastosowaniem wildagliptyny podawanej w monoterapii, ogólna częstość odstawienia z powodu działań niepożądanych nie była większa u pacjentów leczonych wildagliptyną w dawce 100 mg na dobę (0,3%) w porównaniu z pacjentami otrzymującymi placebo (0,6%) lub lek porównawczy ( 0,5%).
W porównawczych kontrolowanych badaniach monoterapii hipoglikemia występowała niezbyt często i była zgłaszana u 0,4% (7 z 1855) pacjentów leczonych wildagliptyną w dawce 100 mg na dobę w porównaniu z 0,2% (2 z 1082) pacjentów w grupie otrzymującej lek porównawczy lub placebo, bez zgłoszone poważne lub poważne zdarzenia.
W badaniach klinicznych masa ciała nie zmieniła się w stosunku do wartości wyjściowej, gdy wildagliptyna w dawce 100 mg na dobę była podawana w monoterapii (odpowiednio -0,3 kg i -1,3 kg dla wildagliptyny i placebo).
Połączenie z metforminą i sulfonylomocznikiem
Tabela 5 Działania niepożądane zgłaszane u pacjentów, którzy otrzymywali Galvus 50 mg dwa razy na dobę w skojarzeniu z metforminą i sulfonylomocznikiem (N = 157)
Opis wybranych działań niepożądanych
Nie było wycofań z powodu działań niepożądanych zgłoszonych w grupie leczonej wildagliptyna + metformina + glimepiryd w porównaniu z 0,6% w grupie leczonej placebo + metformina + glimepiryd.
Częstość występowania hipoglikemii była powszechna w obu leczonych grupach (5,1% w grupie wildagliptyna + metformina + glimepiryd w porównaniu z 1,9% w grupie placebo + metformina + glimepiryd).
W grupie wildagliptyny zgłoszono jeden przypadek ciężkiej hipoglikemii.
Pod koniec badania wpływ na średnią masę ciała był neutralny (+0,6 kg w grupie wildagliptyny i -0,1 kg w grupie placebo).
Związek z insuliną
Tabela 6 Działania niepożądane zgłaszane u pacjentów, którzy otrzymywali Galvus 100 mg na dobę w skojarzeniu z insuliną (z metforminą lub bez) w badaniach z podwójnie ślepą próbą (N = 371)
Opis wybranych działań niepożądanych
W kontrolowanych badaniach klinicznych z zastosowaniem połączenia wildagliptyny 50 mg dwa razy na dobę z insuliną, z metforminą lub bez, ogólna częstość odstawienia z powodu działań niepożądanych wynosiła 0,3% w grupie leczonej wildagliptyną i nie było wycofań w grupie placebo.
Częstość występowania hipoglikemii była podobna w obu leczonych grupach (14,0% w grupie wildagliptyny w porównaniu z 16,4% w grupie placebo).Dwóch pacjentów w grupie wildagliptyny i 6 pacjentów w grupie placebo doświadczyło ciężkiej hipoglikemii.
Pod koniec badania wpływ na średnią masę ciała był neutralny (+0,6 kg od wartości wyjściowej w grupie wildagliptyny i brak zmiany masy w grupie placebo).
Doświadczenie postmarketingowe
Tabela 7 Działania niepożądane po wprowadzeniu do obrotu
Zgłaszanie podejrzewanych działań niepożądanych
Zgłaszanie podejrzewanych działań niepożądanych występujących po dopuszczeniu produktu leczniczego do obrotu jest ważne, ponieważ umożliwia ciągłe monitorowanie stosunku korzyści do ryzyka produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem krajowego systemu zgłaszania.
04.9 Przedawkowanie -
Informacje na temat przedawkowania wildagliptyny są ograniczone.
Objawy
Informacje na temat prawdopodobnych objawów przedawkowania uzyskano z badania tolerancji polegającego na zwiększaniu dawki u zdrowych osób leczonych produktem Galvus przez 10 dni. Przy dawce 400 mg wystąpiły trzy przypadki bólu mięśni i pojedyncze przypadki łagodnych i przemijających parestezji, gorączki, obrzęku i przemijającego wzrostu poziomu lipazy. Przy dawce 600 mg u jednego pacjenta wystąpił obrzęk stóp i dłoni oraz podwyższony poziom fosfokinazy kreatynowej (CPK), aminotransferazy asparaginianowej (AST), białka kreatywnego (CRP) i mioglobiny. U trzech innych osób wystąpił obrzęk stopy, w dwóch przypadkach parestezje. Wszystkie objawy i nieprawidłowości laboratoryjne ustąpiły bez leczenia po odstawieniu badanego leku.
Leczenie
W przypadku przedawkowania zalecane jest leczenie wspomagające. Wildagliptyny nie można usunąć za pomocą hemodializy. Jednak główny metabolit pochodzący z hydrolizy (LAY 151) może być eliminowany przez hemodializę.
05.0 WŁAŚCIWOŚCI FARMAKOLOGICZNE -
05.1 "Właściwości farmakodynamiczne -
Grupa farmakoterapeutyczna: Leki stosowane w cukrzycy, inhibitory dipeptydylopeptydazy 4 (DPP-4), kod ATC: A10BH02
Wildagliptyna należy do klasy leków modulujących wysepki trzustkowe i jest silnym i selektywnym inhibitorem DPP-4.
Mechanizm akcji
Podawanie wildagliptyny powoduje szybkie i całkowite zahamowanie aktywności DPP-4, co prowadzi do zwiększenia endogennych poziomów na czczo i po posiłku GLP-1 (peptyd glukagonopodobny-1) i GIP (polipeptyd insulinotropowy zależny od glukozy).
Efekty farmakodynamiczne
Zwiększając endogenne poziomy inkretyn, wildagliptyna zwiększa wrażliwość komórek beta na glukozę, co skutkuje poprawą wydzielania insuliny zależnego od glukozy. Leczenie wildagliptyną w dawce 50-100 mg na dobę u pacjentów z cukrzycą typu 2 znacząco poprawiło się i znacznik funkcja komórek beta, w tym HOMA-b (Homeostasis Model Assessment -b), stosunek proinsuliny do insuliny oraz pomiary reaktywności komórek beta w teście tolerancji posiłków z częstym pobieraniem próbek. U osób bez cukrzycy (normalny poziom glukozy we krwi) wildagliptyna nie stymuluje wydzielania insuliny ani nie obniża poziomu glukozy.
Poprzez zwiększenie endogennego poziomu GLP-1 wildagliptyna zwiększa również wrażliwość komórek alfa na glukozę, co skutkuje odpowiednim wydzielaniem glukagonu dla ilości glukozy.
Wzrost stosunku insulina/glukagon w hiperglikemii spowodowany wzrostem poziomu inkretyny powoduje zmniejszenie wytwarzania glukozy na czczo i poposiłkowej w wątrobie, co skutkuje zmniejszeniem stężenia glukozy we krwi.
W leczeniu wildagliptyną nie obserwuje się znanego wpływu zwiększonych poziomów GLP-1, które spowalniają opróżnianie żołądka.
Skuteczność kliniczna i bezpieczeństwo
Ponad 15 000 pacjentów z cukrzycą typu 2 wzięło udział w badaniach klinicznych z podwójnie ślepą próbą, kontrolowanych placebo lub substancją czynną, trwających do ponad 2 lat. W badaniach tych wildagliptynę podawano ponad 9000 pacjentom w dawkach dobowych 50 mg raz na dobę, 50 mg dwa razy na dobę lub 100 mg raz na dobę. Ponad 5000 mężczyzn i ponad 4000 kobiet otrzymywało wildagliptynę w dawce 50 mg raz na dobę lub 100 mg na dobę. Ponad 1900 pacjentów, którzy otrzymywali wildagliptynę w dawce 50 mg raz na dobę lub 100 mg na dobę, było w wieku ≥ 65 lat.W badaniach tych wildagliptynę podawano w monoterapii pacjentom z nieleczoną wcześniej cukrzycą typu 2 lub w skojarzeniu pacjentom z niedostatecznie kontrolowaną glikemią za pomocą innych leków przeciwcukrzycowych. produkty.
Ogólnie rzecz biorąc, wildagliptyna poprawiała kontrolę glikemii, gdy podawana była samodzielnie lub w skojarzeniu z metforminą, pochodną sulfonylomocznika i tiazolidynodionem, co odzwierciedla klinicznie istotne zmniejszenie „HbA1c w stosunku do wartości wyjściowych w”punkt końcowy badanie (patrz Tabela 8).
W badaniach klinicznych wielkość zmniejszenia HbA1c po zastosowaniu wildagliptyny była większa u pacjentów z wyższymi wyjściowymi wartościami HbA1c.
W 52-tygodniowym, podwójnie zaślepionym badaniu kontrolowanym wildagliptyna (50 mg dwa razy na dobę) zmniejszyła wyjściową wartość HbA1c o -1% w porównaniu do -1,6% osiąganych po zastosowaniu metforminy (miareczkowanej do 2 g/dobę). leczonych wildagliptyną zgłaszali znacznie mniejszą częstość występowania działań niepożądanych ze strony przewodu pokarmowego niż osoby leczone metforminą.
W 24-tygodniowym, podwójnie zaślepionym badaniu kontrolowanym wildagliptynę (50 mg dwa razy na dobę) porównywano z rozyglitazonem (8 mg raz na dobę). U pacjentów ze średnią wyjściową wartością HbA1c 8,7% średnie zmniejszenie wyniosło -1,20% dla wildagliptyny i -1,48% dla rozyglitazonu. Pacjenci, którzy otrzymywali rozyglitazon, odnotowali średni przyrost masy ciała (+1,6 kg), podczas gdy ci, którzy otrzymywali wildagliptynę, nie odnotowali przyrostu masy ciała (-0,3 kg). Częstość występowania obrzęków obwodowych była mniejsza w grupie wildagliptyny niż w grupie rozyglitazonu (odpowiednio 2,1% w porównaniu z 4,1%).
W 2-letnim badaniu klinicznym wildagliptyna (50 mg dwa razy na dobę) była porównywana z gliklazydem (do 320 mg/dobę). Po dwóch latach średnie zmniejszenie HbA1c wyniosło -0,5% dla wildagliptyny i -0,6% dla glikazydu w porównaniu ze średnią wyjściową HbA1c wynoszącą 8,6%. Nie osiągnięto równoważności statystycznej. Wildagliptyna była związana z mniejszą liczbą epizodów hipoglikemii (0,7%) niż glikazyd (1,7%).
W 24-tygodniowym badaniu klinicznym wildagliptyna (50 mg dwa razy na dobę) była porównywana z pioglitazonem (30 mg raz na dobę) u pacjentów z niedostateczną kontrolą glikemii za pomocą metforminy (średnia dawka dobowa: 2020 mg). W porównaniu z wyjściową wartością HbA1c wynoszącą 8,4%, średnie zmniejszenie wyniosło -0,9% dla wildagliptyny w skojarzeniu z metforminą i -1,0% dla pioglitazonu w skojarzeniu z metforminą. zaobserwowano w porównaniu do +0,3 kg obserwowanego u osób otrzymujących wildagliptynę w skojarzeniu z metforminą.
W 2-letnim badaniu klinicznym wildagliptyna (50 mg dwa razy na dobę) była porównywana z glimepirydem (do 6 mg/dobę – średnia dawka po 2 latach: 4,6 mg) u pacjentów leczonych metforminą (średnia dawka dobowa: 1894 mg). Po roku średnie zmniejszenie HbA1c wyniosło -0,4% w przypadku wildagliptyny w skojarzeniu z metforminą i -0,5% w przypadku glimepirydu w skojarzeniu z metforminą, w porównaniu ze średnią wyjściową HbA1c wynoszącą 7,3%. Zmiana masy ciała wyniosła -0,2 kg po wildagliptynie w porównaniu do +1,6 kg po glimepirydzie. Częstość występowania hipoglikemii była istotnie niższa w grupie wildagliptyny (1,7%) niż w grupie glimepirydu (16,2%).W punkcie końcowym badania (2 lata), w obu grupach leczenia, HbA1c była podobna do wartości wyjściowych utrzymały się zmiany masy ciała i różnice w hipoglikemii.
W 52-tygodniowym badaniu wildagliptyna (50 mg dwa razy na dobę) była porównywana z gliklazydem (średnia dawka dobowa: 229,5 mg) u pacjentów z niedostateczną kontrolą glikemii za pomocą metforminy (dawka początkowa metforminy 1928 mg na dobę). Po roku średnie zmniejszenie HbA1c wyniosło -0,81% w przypadku wildagliptyny w skojarzeniu z metforminą (średnia początkowa wartość HbA1c 8,4%) i -0,85% w przypadku gliklazydu w skojarzeniu z metforminą (średnia początkowa wartość HbA1c 8,5%) ); osiągnięto równoważność statystyczną (95% CI: -0,11 - 0,20). Zmiana masy ciała wyniosła +0,1 kg po zastosowaniu wildagliptyny w porównaniu do przyrostu masy ciała o +1,4 kg po zastosowaniu gliklazydu.
Skuteczność kombinacji wildagliptyny i metforminy o ustalonej proporcji (miareczkowanej stopniowo do dawki 50 mg/500 mg dwa razy na dobę lub 50 mg/1000 mg dwa razy na dobę) jako terapii oceniano w 24-tygodniowym badaniu. denova).
HbA1c obniżyła się o -1,82% przy stosowaniu wildagliptyny/metforminy 50 mg/1000 mg dwa razy na dobę, o -1,61% przy stosowaniu wildagliptyny/metforminy 50 mg/500 mg dwa razy na dobę, o -1, 36% przy stosowaniu metforminy 1000 mg dwa razy na dobę i -1,09 % pacjentów przyjmujących wildagliptynę w dawce 50 mg dwa razy na dobę, począwszy od średniej wyjściowej wartości HbA1c wynoszącej 8,6%, ≥10,0% było bardziej widoczne.
Przeprowadzono 24-tygodniowe, podwójnie zaślepione, randomizowane, wieloośrodkowe, kontrolowane placebo badanie w celu oceny wpływu leczenia wildagliptyny 50 mg raz na dobę w porównaniu z placebo u 515 pacjentów z cukrzycą typu 2 i zaburzeniami czynności nerek. ciężka (N = 221). Odpowiednio 68,8% i 80,5% pacjentów z umiarkowanymi i ciężkimi zaburzeniami czynności nerek było leczonych insuliną (odpowiednio średnia dawka dobowa 56 jednostek i 51,6 jednostek) na początku badania. U pacjentów z umiarkowanymi zaburzeniami czynności nerek wildagliptyna znacząco obniżyła HbA1c w porównaniu z placebo (różnica -0,53%) ze średniej wartości wyjściowej wynoszącej 7,9%.U pacjentów z ciężkimi zaburzeniami czynności nerek wildagliptyna znacząco obniżyła HbA1c w porównaniu z placebo (różnica -0,56%). ), począwszy od średniej wartości wyjściowej 7,7%.
Przeprowadzono 24-tygodniowe, randomizowane, podwójnie zaślepione, kontrolowane placebo badanie z udziałem 318 pacjentów w celu oceny skuteczności i bezpieczeństwa wildagliptyny (50 mg dwa razy na dobę) w skojarzeniu z metforminą (≥1500 mg na dobę) i glimepirydem (≥4 mg Wildagliptyna w skojarzeniu z metforminą i glimepirydem istotnie obniżała HbA1c w porównaniu z placebo
Skorygowane o placebo średnie zmniejszenie HbA1c ze średniej wartości wyjściowej 8,8% wyniosło -0,76%.
Przeprowadzono 24-tygodniowe, randomizowane, podwójnie zaślepione, kontrolowane placebo badanie z udziałem 449 pacjentów w celu oceny skuteczności i bezpieczeństwa wildagliptyny (50 mg dwa razy na dobę) w skojarzeniu ze stałą dawką insuliny bazowej lub gotowej mieszanki (średnia dawka dobowa 41). jednostek), z jednoczesnym stosowaniem metforminy (n = 276) lub bez metforminy (n = 173). Wildagliptyna w połączeniu z insuliną znacząco obniżyła HbA1c w porównaniu z placebo. W populacji ogólnej, skorygowana o placebo średnia redukcja HbA1c ze średniej wyjściowej HbA1c 8,8% wyniosła -0,72%. W podgrupach leczonych insuliną z metforminą lub bez metforminy średnie, skorygowane o placebo zmniejszenie HbA1c wyniosło odpowiednio -0,63% i -0,84%. Częstość występowania hipoglikemii w populacji ogólnej wynosiła odpowiednio 8,4% i 7,2% w grupie wildagliptyny i placebo.U pacjentów otrzymujących wildagliptynę nie zaobserwowano przyrostu masy ciała (+0,2 kg), podczas gdy u pacjentów otrzymujących placebo zaobserwowano zmniejszenie masy ciała (-0,7 kg).
W innym 24-tygodniowym badaniu z udziałem pacjentów z bardziej zaawansowaną cukrzycą typu 2 niewystarczająco kontrolowaną insuliną (krótki i dłuższy czas działania, średnia dawka insuliny 80 j.m./dobę) średnie zmniejszenie HbA1c po zastosowaniu wildagliptyny (50 mg dwa razy na dobę) było dodana do insuliny była statystycznie i istotnie większa niż w przypadku placebo + insulina (0,5% vs. 0,2%). Częstość występowania hipoglikemii była mniejsza w grupie wildagliptyny niż w grupie placebo (22,9% vs 29,6%).
Przeprowadzono 52-tygodniowe, wieloośrodkowe, randomizowane badanie z podwójnie ślepą próbą u pacjentów z cukrzycą typu 2 i zastoinową niewydolnością serca (klasa czynnościowa I-III wg NYHA) w celu oceny wpływu wildagliptyny w dawce 50 mg dwa razy na dobę (n = 128) w porównaniu z placebo (N = 126) na frakcji wyrzutowej lewej komory (LVEF). Wildagliptyna nie jest związana ze zmianą czynności lewej komory lub pogorszeniem wcześniej istniejącej CHF. Oceniane zdarzenia sercowo-naczyniowe były ogólnie zrównoważone. w przypadku stosowania wildagliptyny wystąpiło więcej zdarzeń sercowych niż u pacjentów otrzymujących placebo, jednakże istniały odchylenia w początkowym ryzyku sercowo-naczyniowym na korzyść placebo, a liczba zdarzeń była niska, co uniemożliwiało ostateczne wnioskowanie. Wildagliptyna istotnie obniżyła HbA1c w porównaniu z placebo (różnica 0,6 %) od wartości średnia wartość wyjściowa 7,8% w 16. tygodniu. W podgrupie klasy III wg NYHA spadek HbA1c był mniejszy (różnica 0,3%), ale wniosek ten jest ograniczony ze względu na małą liczbę pacjentów (N = 44). Częstość występowania hipoglikemii w całej populacji wynosiła odpowiednio 4,7% i 5,6% w grupie wildagliptyny i placebo.
Ryzyko sercowo-naczyniowe
Przeprowadzono metaanalizę 25 badań klinicznych III fazy trwających ponad 2 lata niezależnie i prospektywnie ocenianych zdarzeń sercowo-naczyniowych. Analiza ta wykazała, że leczenie wildagliptyną nie było związane ze zwiększonym ryzykiem sercowo-naczyniowym w porównaniu z porównaniami. Złożony punkt końcowy – udowodnione zdarzenia sercowo-naczyniowe i mózgowo-naczyniowe (CCV) [ostry zespół wieńcowy (ACS), przemijający napad niedokrwienny (z dowodami na zawał serca w obrazowaniu), udar mózgu lub zgon z powodu CCV] – był podobny dla wildagliptyny w porównaniu z kombinacją porównania aktywny i placebo [współczynnik ryzyka Mantela-Haenszela 0,84 (95% przedział ufności 0,63-1,12)]. Łącznie 99 z 8956 pacjentów w grupie wildagliptyny zgłosiło zdarzenie w porównaniu z 91 z 6061 pacjentów w grupie porównawczej.
Tabela 8 Kluczowe wyniki dotyczące skuteczności wildagliptyny w kontrolowanych placebo badaniach monoterapii i badaniach uzupełniających (pierwotna skuteczność w populacji ITT – zamiar leczenia)
Populacja pediatryczna
Europejska Agencja Leków uchyliła obowiązek przedstawienia wyników badań wildagliptyny we wszystkich podgrupach populacji pediatrycznej z cukrzycą typu 2 (informacje dotyczące stosowania u dzieci, patrz punkt 4.2).
05.2 "Właściwości farmakokinetyczne -
Wchłanianie
Wildagliptyna po podaniu doustnym na czczo jest szybko wchłaniana, osiągając maksymalne stężenie w osoczu po 1,7 godziny. Pokarm nieznacznie opóźnia (o 2,5 godziny) czas do osiągnięcia maksymalnego stężenia w osoczu, ale nie zmienia całkowitej ekspozycji (AUC).Podawanie wildagliptyny z pokarmem powoduje zmniejszenie Cmax (19%).L Jednak zakres zmiany nie jest klinicznie znaczące, więc Galvus można przyjmować niezależnie od jedzenia. Całkowita biodostępność wynosi 85%.
Dystrybucja
Wiązanie wildagliptyny z białkami osocza jest niskie (9,3%), a wildagliptyna rozkłada się równomiernie między osocze i czerwone krwinki. Po podaniu dożylnym średnia objętość dystrybucji wildagliptyny allo stan stabilny (Vss) wynosi 71 litrów, co sugeruje dystrybucję pozanaczyniową.
Biotransformacja
U ludzi metabolizm jest główną drogą eliminacji wildagliptyny i stanowi 69% dawki.Główny metabolit (LAY 151) jest nieaktywny farmakologicznie i jest produktem hydrolizy grupy cyjanowej i stanowi 57% dawki. z produktów glukuronidu (BQS867) i hydrolizy amidów (4% dawki). Dane in vitro na mikrosomach ludzkiej nerki sugerują, że nerki mogą być jednym z głównych czynników hydrolizy wildagliptyny do jej głównego nieaktywnego metabolitu, LAY 151. Według badań DPP-4 częściowo przyczynia się do hydrolizy wildagliptyny in vivo przeprowadzone na szczurach wolnych od DPP-4. Wildagliptyna nie jest metabolizowana w policzalnym stopniu przez enzymy CYP 450. W związku z tym oczekuje się, że jednoczesne podawanie produktów leczniczych będących inhibitorami i (lub) induktorami CYP 450 nie wpływa na klirens metaboliczny wildagliptyny. in vitro wykazali, że wildagliptyna nie hamuje/indukuje enzymów CYP 450. Dlatego jest mało prawdopodobne, aby wildagliptyna wpływała na klirens metaboliczny produktów leczniczych metabolizowanych przez CYP 1A2, CYP 2C8, CYP 2C9, CYP 2C19, CYP 2D6, CYP 2E1 lub CYP 3A4 / 5 , przy jednoczesnym podawaniu.
Eliminacja
Po podaniu doustnym wildagliptyny znakowanej 14C około 85% dawki jest wydalane z moczem, a 15% z kałem. Po podaniu doustnym wydalanie przez nerki niezmienionej wildagliptyny wynosi 23% dawki. luz całkowite wartości wildagliptyny w osoczu i nerkach wynoszą odpowiednio 41 i 13 l / godzinę. Po podaniu dożylnym średni okres półtrwania w fazie eliminacji wynosi około 2 h. Po podaniu doustnym okres półtrwania w fazie eliminacji wynosi około 3 godziny.
Liniowość / Nieliniowość
W zakresie dawek terapeutycznych Cmax wildagliptyny i pole pod krzywą zależności stężenia w osoczu od czasu (AUC) zwiększają się w przybliżeniu proporcjonalnie do dawki.
Specyficzne grupy pacjentów
Seks
Nie zaobserwowano klinicznie istotnych różnic w farmakokinetyce wildagliptyny między zdrowymi mężczyznami i kobietami w „szerokim zakresie wieku i wskaźnika masy ciała (BMI). Nie ma to wpływu na hamowanie DPP-4 przez wildagliptynę.” ze względu na płeć.
Starsi mieszkańcy
U zdrowych osób w podeszłym wieku (≥ 70 lat) całkowita ekspozycja na wildagliptynę (100 mg raz na dobę) wzrosła o 32%, przy 18% wzroście maksymalnego stężenia w osoczu w porównaniu ze zdrowymi młodymi osobami (18 Jednak zmiany te nie są brane pod uwagę Wiek nie ma wpływu na hamowanie DPP-4 przez wildagliptynę.
Upośledzona czynność wątroby
Wpływ zaburzeń czynności wątroby na farmakokinetykę wildagliptyny badano u pacjentów z łagodnymi, umiarkowanymi i ciężkimi zaburzeniami czynności wątroby, na podstawie skali Child-Pugh (w zakresie od 6 dla łagodnych do 12 dla ciężkich), w porównaniu ze zdrowymi osobami. z łagodnymi i umiarkowanymi zaburzeniami czynności wątroby, ekspozycja na wildagliptynę po podaniu pojedynczej dawki jest zmniejszona (odpowiednio o 20% i 8%), natomiast u pacjentów z ciężkimi zaburzeniami czynności wątroby ekspozycja na wildagliptynę jest zwiększona o 22%. ) w ekspozycji na wildagliptynę wynosi ≥30%, co nie jest uważane za klinicznie istotne. Nie stwierdzono korelacji między ciężkością choroby wątroby a zmianami w ekspozycji na wildagliptynę.
Upośledzona czynność nerek
Przeprowadzono otwarte badanie z zastosowaniem dawek wielokrotnych w celu oceny farmakokinetyki niższej dawki terapeutycznej wildagliptyny (50 mg raz na dobę) u pacjentów z różnym stopniem przewlekłej niewydolności nerek określonej na podstawie klirensu kreatyniny (łagodny: 50 do
Wildagliptyna została usunięta przez hemodializę w ograniczonym zakresie (3% podczas 3-4 godzinnej hemodializy rozpoczynającej się 4 godziny po podaniu).
Grupy etniczne
Ograniczone dane sugerują, że rasa nie ma większego wpływu na farmakokinetykę wildagliptyny.
05.3 Przedkliniczne dane o bezpieczeństwie -
Opóźnienia przewodzenia impulsów wewnątrzsercowych obserwowano u psów po podaniu dawki bez efektu 15 mg/kg (7-krotność ekspozycji u ludzi w oparciu o Cmax).
U szczurów i myszy zaobserwowano akumulację pienistych makrofagów pęcherzykowych w płucach. Dawka niepowodująca efektu wynosiła 25 mg/kg (5-krotność ekspozycji u ludzi na podstawie AUC) u szczurów i 750 mg/kg (142-krotność ekspozycji u ludzi) u myszy. U psów obserwowano objawy żołądkowo-jelitowe, szczególnie miękkie stolce, śluzowate stolce, biegunkę oraz, przy większych dawkach, krew w stolcu. Nie ustalono poziomu braku efektów.
W konwencjonalnych badaniach genotoksyczności in vitro I in vivo wildagliptyna nie była mutagenna. U szczurów badanie płodności i wczesnego rozwoju embrionalnego nie wykazało, że wildagliptyna powoduje upośledzenie płodności, zdolności reprodukcyjnej lub wczesnego rozwoju embrionalnego. Toksyczność zarodkowo-płodowa oceniano u szczurów i królików. U szczurów zaobserwowano zwiększoną częstość występowania pływających żeber w związku ze zmniejszeniem parametrów masy ciała matki, przy dawce nie wywołującej efektu 75 mg/kg (10-krotność ekspozycji u ludzi). wskazujące na opóźnienie rozwoju, zaobserwowano tylko w obecności ciężkiej toksyczności matczynej, przy dawce nie wywołującej efektu 50 mg/kg (9-krotność ekspozycji u ludzi).Przeprowadzono badanie rozwoju przed- i pourodzeniowego na szczurach. tylko w połączeniu z toksycznością matczyną ≥ 150 mg / kg i obejmującą przejściową redukcję masy ciała i zmniejszoną aktywność motoryczną w pokoleniu F1.
Przeprowadzono dwuletnie badanie rakotwórczości u szczurów z dawkami doustnymi do 900 mg/kg (około 200-krotność ekspozycji u ludzi przy maksymalnej zalecanej dawce). Nie zaobserwowano zwiększenia częstości występowania nowotworów przypisywanych wildagliptynie.Przeprowadzono kolejne 2-letnie badanie rakotwórczości na myszach stosujących dawki doustne do 1000 mg/kg.Zaobserwowano wzrost częstości występowania gruczolakoraków piersi. odpowiednio 500 mg/kg (59-krotność ekspozycji u ludzi) i 100 mg/kg (16-krotność ekspozycji u ludzi). Na podstawie braku genotoksyczności wildagliptyny i jej głównego metabolitu, rozwoju guzów u jednego gatunku i wszystkich innych, nie uznano, że zwiększona częstość występowania tych guzów u myszy stanowi istotne ryzyko dla ludzi. .
W 13-tygodniowym badaniu toksykologicznym na małpach cynomolgus zmiany skórne zgłaszano po dawkach ≥ 5 mg/kg/dobę. Zmiany były konsekwentnie zlokalizowane na kończynach (ręce, stopy, uszy i ogon). Przy dawce 5 mg/kg/dobę (w przybliżeniu równoważnej ludzkiemu AUC po ekspozycji na dawkę 100 mg) obserwowano jedynie pęcherzyki. Ustąpiły one pomimo kontynuowania leczenia i nie były związane z nieprawidłowościami histopatologicznymi. Przy dawkach ≥ 20 mg/kg/dobę (około 3-krotność AUC u ludzi po ekspozycji na dawkę 100 mg) zaobserwowano złuszczanie i łuszczenie się skóry, strupów i owrzodzeń ogona, z powiązanymi zmianami histopatologicznymi. Zmiany martwicze ogona obserwowano przy dawkach ≥ 80 mg/kg/dobę.
W ciągu 4-tygodniowego okresu rekonwalescencji zmiany skórne nie ustępowały u małp leczonych dawką 160 mg/kg/dobę.
06.0 INFORMACJE FARMACEUTYCZNE -
06.1 Substancje pomocnicze -
Bezwodna laktoza
Celuloza mikrokrystaliczna
Glikolan sodowy skrobi (typ A)
Stearynian magnezu
06.2 Niezgodność "-
Nieistotne.
06.3 Okres ważności "-
3 lata
06.4 Specjalne środki ostrożności przy przechowywaniu -
Przechowywać w oryginalnym opakowaniu w celu ochrony przed wilgocią.
06.5 Rodzaj opakowania bezpośredniego i zawartość opakowania -
Blister aluminium / aluminium (PA / Al / PVC // Al)
Dostępne w opakowaniach zawierających 7, 14, 28, 30, 56, 60, 90, 112, 180 lub 336 tabletek oraz w opakowaniach zbiorczych zawierających 336 (3 opakowania po 112) tabletek.
Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
06.6 Instrukcje użytkowania i obsługi -
Brak specjalnych instrukcji.
07.0 POSIADACZ „POZWOLENIA NA DOPUSZCZENIE DO OBROTU” -
Novartis Europharm Limited
Frimley Business Park
Camberley GU16 7SR
Wielka Brytania
08.0 NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU -
UE / 1/07/414 / 001-010
UE / 1/07/414/018
038144010
038144022
038144034
038144046
038144059
038144061
038144073
038144085
038144097
038144109
038144186
09.0 DATA PIERWSZEGO ZEZWOLENIA LUB PRZEDŁUŻENIA ZEZWOLENIA -
Data pierwszego zezwolenia: 26 września 2007 r.
Data ostatniego przedłużenia: 26 września 2012 r.
10.0 DATA ZMIAN TEKSTU -
DCCE Kwiecień 2015












-cos-sintomi-cause-e-gravidanza.jpg)