Jest to droga metaboliczna, która składa się z kilku faz: cholesterol jest transportowany z tkanek obwodowych do wątroby najpierw przez układ limfatyczny, a następnie przez krwioobieg. Głównymi składnikami biorącymi udział w odwrotnym transporcie cholesterolu są HDL, ABCA1 oraz apo A-I.
pozajelitowe lub wątrobowe komórki obwodowe nie są zdolne do degradacji nadmiaru cholesterolu; dlatego, aby utrzymać homeostazę komórkową, niezbędna jest obecność mechanizmu odpowiedzialnego za usuwanie cholesterolu.
Ten mechanizm mający na celu odzyskanie przez wątrobę nadmiaru cholesterolu obwodowego nazywany jest „odwróconym transportem cholesterolu” (RCT: zwrotny transport cholesterolu).
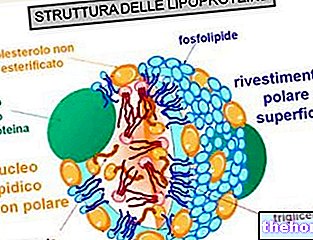
(fosfolipidy i cholesterol), co prowadzi do gromadzenia się i generowania dojrzałych cząstek HDL.Prekursory HDL
Pierwszy etap transportu zwrotnego cholesterolu polega na wytwarzaniu przez jelita i wątrobę dyskoidalnych prekursorów HDL, które eksponują na swojej powierzchni apoproteiny (głównie ApoA-I).
W ten sposób uwalniane są cząsteczki prekursorowe HDL zwane pre-B-HDL, które zawierają bardzo małe ilości cholesterolu i lipidów, zwłaszcza fosfolipidów. Obecność tych cząsteczek prekursorowych na poziomie obwodowym sprzyja przenoszeniu nadmiaru wolnego cholesterolu (FC) - wyciekającego z komórek tkanek obwodowych - do apo AI, poprzez interwencję transportera błonowego zwanego kasetą wiążącą ATP A1 (ABCA1).
Transporter ten jest zlokalizowany na powierzchni komórki oraz w błonach aparatu Golgiego i może transportować lipidy z aparatu Golgiego do błony komórkowej, ułatwiając w ten sposób ich wypływ.
W tym momencie, gdy tylko wolny cholesterol wchodzi do natywnego HDL, interweniuje enzym osocza pochodzenia wątrobowego, zwany acylotransferazą lecytyny-cholesterolu osocza lub prościej LCAT; enzym ten przekształca wolny cholesterol włączony do pre-B-HDL w estry cholesterolu, przekształcając pre-B-HDL w ich dojrzałą formę α-HDL; w praktyce ciągła akumulacja cholesterolu w rdzeniu lipoproteinowym przekształca dyskoidalne HDL w kuliste i pulchne cząstki, które mogą dalej pozyskiwać apoproteiny z cząstek lipoproteinowych bogatych w triglicerydy i łączyć się ze sobą.
W całym procesie kluczową rolę odgrywa apolipoproteina AI, stymulująca zarówno aktywność transportera ABCA1, jak i LCAT.Ponieważ ApoAI jest najczęściej reprezentowaną apolipoproteiną w HDL, jej stężenie w osoczu jest bezpośrednio związane z poziomem cholesterolu HDL.
UWAGA: proces estryfikacji jest niezbędny, aby zapobiec ponownej dyfuzji cholesterolu z HDL do błony komórkowej; mechanizm ten wykorzystuje kwas tłuszczowy w pozycji dwa obecny w cząsteczkach fosfatydylocholiny.
Proces estryfikacji za pośrednictwem LCAT przekształca następnie cząsteczki pre-B-HDL w ich „dojrzały” kulisty kształt α-HDL. Te lipoproteiny są następnie transportowane do wątroby, gdzie uwalniają cholesterol dwoma różnymi drogami.
Pierwsza droga wątrobowa
W pierwszym przypadku HDL bogaty w zestryfikowany cholesterol przenosi ten lipid do lipoprotein bogatych w triglicerydy (lipoproteiny o bardzo niskiej i niskiej gęstości), które są następnie przechwytywane przez wątrobę przez specyficzne receptory (LDL-R) i usuwane z krążenia.
Celem jest przeniesienie cholesterolu obwodowego do wątroby przez układ receptorów LDL, a następnie „wyładowanie” HDL z nadmiaru cholesterolu na poziomie obwodowym, aby ponownie stał się dostępny do przyjęcia go z tkanek; Zubożając cholesterol, HDL akceptują w zamian trójglicerydy, a dzieje się to dzięki białku przenoszącemu estry cholesterolu (CETP).
Zadaniem tego białka jest zatem sprzyjanie redystrybucji i równowadze estrów cholesterolu i trójglicerydów pomiędzy lipoproteinami HDL, LDL, IDL, VLDL, chylomikronami i pozostałościami chylomikronów, co w efekcie końcowym prowadzi do wzbogacenia w trójglicerydy HDL, kosztem estrów cholesterolu i zmniejszeniem wielkości HDL.
Druga trasa wątrobowa
Drugi szlak obejmuje wątrobowe receptory SR-B1 dla HDL bogatego w zestryfikowany cholesterol, przy braku jednoczesnej degradacji części białkowej HDL, która jest następnie zawracana. W praktyce enzym ten pozwala na opróżnienie HDL z ich zawartości i regenerację nowych pre-B-HDL.
Część HDL i ApoA-I ulega jednak internalizacji i degradacji na poziomie lizosomalnym, zarówno w komórkach wątroby, jak i nerek. Wychwyt, w którym pośredniczy SR-B1, jest bardziej wydajny dzięki aktywności lipazy wątrobowej, zdolnej do przebudowy HDL poprzez hydrolizę powierzchniowych fosfolipidów i umożliwienia przepływu estryfikowanego cholesterolu z rdzenia lipoproteinowego w kierunku błony komórkowej (przypuszcza się, że między innymi , że ApoE jest również zaangażowana w selektywny wychwyt, ponieważ myszy z niedoborem genu ApoE wykazują zmniejszenie skuteczności tego szlaku.) SR-BI jest wyrażany głównie w wątrobie, nadnerczach i jajnikach.