Składniki aktywne: kwas alendronowy
Bonasol 70 mg co tydzień roztwór doustny
Dlaczego stosuje się Bonasol? Po co to jest?
Roztwór doustny Bonasol należy do grupy leków niehormonalnych zwanych bisfosfonianami. Roztwór doustny Bonasol stosuje się do:
- Zapobiega utracie masy kostnej (osteoporozie), która występuje u kobiet po menopauzie i pomaga w odbudowie kości.
- Zmniejsz ryzyko złamań kręgów i biodra.
Lekarz przepisał roztwór doustny Bonasol w celu leczenia osteoporozy i zmniejszenia ryzyka złamań kręgów i szyjki kości udowej.
Czym jest osteoporoza?
Osteoporoza to ścieńczenie i osłabienie kości. Występuje często u kobiet po menopauzie. W okresie menopauzy jajniki przestają wytwarzać żeński hormon estrogen, który pomaga w utrzymaniu zdrowych szkieletów kobiet. W rezultacie dochodzi do utraty masy kostnej i osłabienia kości. Im wcześniej kobieta wejdzie w menopauzę, tym większe ryzyko osteoporozy.
Osteoporoza zwykle początkowo nie daje żadnych objawów. Jednak nieleczona może spowodować złamania kości. Chociaż takie złamania zwykle powodują ból, złamania kręgów mogą również pozostać niezauważone, dopóki nie spowodują obniżenia wzrostu. Złamania kości mogą wystąpić podczas zwykłych codziennych czynności, takich jak podnoszenie ciężarów, lub w wyniku drobnych urazów, które zazwyczaj nie powodują złamań normalnych kości. Złamania kości zwykle występują w biodrze, kręgosłupie lub nadgarstku i mogą być nie tylko bolesne, ale mogą również prowadzić do poważnych problemów, takich jak np. wygięcie pleców (garb) i ograniczenie zakresu ruchu.
Jak można leczyć osteoporozę?
Osteoporozę można leczyć i nigdy nie jest za późno na rozpoczęcie leczenia.Alendronian nie tylko zapobiega utracie masy kostnej, ale także pomaga odbudować utraconą tkankę kostną oraz zmniejsza ryzyko złamań kręgów i kości biodrowych.
Oprócz leczenia preparatem Bonasol Oral Solution, lekarz może zasugerować zmianę stylu życia dla własnego dobra, na przykład:
Rzucanie palenia. Wydaje się, że palenie zwiększa tempo utraty masy kostnej, a co za tym idzie, może zwiększać ryzyko złamań.
Wykonywanie ćwiczeń. Podobnie jak mięśnie, kości również potrzebują ćwiczeń, aby były silne i zdrowe. Przed rozpoczęciem jakiegokolwiek programu ćwiczeń skonsultuj się z lekarzem.
Przyjmując zbilansowaną dietę. Lekarz może doradzić prawidłową dietę lub poinformować, czy należy przyjmować jakiekolwiek suplementy (zwłaszcza wapń i witaminę D).
Przeciwwskazania Kiedy nie należy stosować preparatu Bonasol
Nie należy przyjmować roztworu doustnego Bonasol:
- jeśli u pacjenta stwierdzono uczulenie (nadwrażliwość) na alendronian lub którykolwiek z pozostałych składników leku Bonasol 70 mg roztwór doustny (patrz punkt 6: Inne informacje).
- jeśli u pacjenta występują problemy z przełykiem (przewód łączący usta z żołądkiem), takie jak zwężenie lub trudności w połykaniu płynów
- jeśli lekarz powiedział pacjentowi, że ma niski poziom wapnia we krwi;
- jeśli nie jesteś w stanie stać lub siedzieć prosto przez co najmniej 30 minut.Jeśli uważasz, że którekolwiek z powyższych dotyczy Ciebie, nie przyjmuj rozwiązania. Najpierw porozmawiaj z lekarzem i postępuj zgodnie z jego instrukcjami.
Środki ostrożności dotyczące stosowania Informacje ważne przed zastosowaniem leku Bonasol
Zachowaj szczególną ostrożność stosując roztwór doustny Bonasol
Przed przyjęciem leku Bonasol roztwór doustny ważne jest, aby poinformować lekarza, jeśli:
- masz problemy z nerkami
- cierpią na jakiekolwiek alergie
- masz problemy z połykaniem lub trawieniem
- Twój lekarz powiedział Ci, że masz przełyk Barretta (zaburzenie związane ze zmianami w komórkach wyściełających dolny przełyk)
- mają niski poziom wapnia we krwi
- masz chorobę dziąseł
- zaplanował „usunięcie zęba
Przed leczeniem roztworem doustnym Bonasol należy rozważyć badanie stomatologiczne, jeśli występuje którykolwiek z następujących stanów:
- cierpią na raka
- przechodzisz chemioterapię lub radioterapię
- on jest na sterydoterapii
- nie podlega rutynowej opiece stomatologicznej
- cierpią na choroby dziąseł
W trakcie leczenia należy wykonywać profilaktyczną opiekę stomatologiczną, zgodnie z zaleceniami lekarza stomatologa.
Może wystąpić podrażnienie, zapalenie lub owrzodzenie przełyku (przewodu łączącego jamę ustną z żołądkiem), któremu często towarzyszą objawy, takie jak ból w klatce piersiowej, zgaga lub trudności lub ból w przełykaniu, zwłaszcza jeśli po przyjęciu leku Bonasol pacjent leży na plecach. roztwór doustny Te działania niepożądane mogą się nasilić, jeśli pacjenci będą kontynuować przyjmowanie roztworu doustnego Bonasol po wystąpieniu tych objawów.
Interakcje Jakie leki lub pokarmy mogą modyfikować działanie Bonasol
Suplementy wapnia, środki zobojętniające sok żołądkowy i niektóre leki doustne mogą zakłócać wchłanianie preparatu Bonasol Oral Solution, gdy są przyjmowane w tym samym czasie.
Dlatego ważne jest, aby postępować zgodnie z instrukcjami podanymi w punkcie 3. JAK STOSOWAĆ BONASOL W ROZTWORZE DOUSTNYM.
Należy powiedzieć lekarzowi lub farmaceucie, jeśli pacjent przyjmuje lub ostatnio przyjmował jakiekolwiek inne leki, w tym leki wydawane bez recepty.
Przyjmowanie roztworu doustnego Bonasol z jedzeniem i piciem
Jedzenie i napoje (w tym woda mineralna) mogą wpływać na skuteczność roztworu doustnego Bonasol przyjmowane jednocześnie z lekiem.Dlatego ważne jest, aby postępować zgodnie z instrukcjami podanymi w punkcie 3. JAK STOSOWAĆ BONASOL W ROZTWORZE DOUSTNYM.
Ostrzeżenia Ważne jest, aby wiedzieć, że:
Stosowanie u dzieci i młodzieży
Nie należy podawać roztworu doustnego Bonasol dzieciom i młodzieży.
Ciąża i karmienie piersią
Roztwór doustny Bonasol jest przeznaczony do stosowania wyłącznie przez kobiety po menopauzie.
Nie należy przyjmować roztworu doustnego Bonasol w przypadku podejrzenia ciąży lub karmienia piersią.
Przed zażyciem jakiegokolwiek leku należy zasięgnąć porady lekarza lub farmaceuty.
Prowadzenie i używanie maszyn
Podczas stosowania alendronianu zgłaszano działania niepożądane (w tym niewyraźne widzenie, zawroty głowy oraz ból kości, mięśni lub stawów, nawet silny), które mogą wpływać na zdolność prowadzenia pojazdów i obsługiwania maszyn. . MOŻLIWE EFEKTY UBOCZNE).
Ważne informacje o niektórych składnikach roztworu doustnego Bonasol
Ten lek zawiera 0,15% obj. etanolu (alkoholu), tj. do 115 mg na dawkę, co odpowiada 3 ml piwa i 1,3 ml wina na dawkę.
Zawiera również żółcień pomarańczową (E110), parahydroksybenzoesany metylu i propylu (E218, E216), które mogą powodować reakcje alergiczne (czasami opóźnione). Alergia częściej występuje u osób uczulonych na aspirynę. W razie wątpliwości należy skonsultować się z lekarzem lub farmaceutą.
Dawka, sposób i czas podawania Jak stosować Bonasol: dawkowanie
Roztwór doustny Bonasol należy zawsze przyjmować zgodnie z zaleceniami lekarza. W razie wątpliwości skonsultuj się z lekarzem lub farmaceutą.
Zazwyczaj stosowana dawka to jedna jednostka dawki 70 mg (100 ml) raz w tygodniu.
Aby upewnić się, że odniesiesz największe korzyści z roztworu doustnego Bonasol, postępuj zgodnie z poniższymi instrukcjami.
Wybierz dzień tygodnia, który najbardziej Ci odpowiada, zgodnie ze swoimi harmonogramami. Przyjmuj roztwór doustny Bonasol raz w tygodniu w wybrany dzień.
Bardzo ważne jest, aby postępować zgodnie z poniższymi instrukcjami, aby roztwór doustny Bonasol dotarł do żołądka tak szybko, jak to możliwe i zminimalizować możliwość podrażnienia przełyku (kanał między ustami a żołądkiem).
- Rano, po przebudzeniu, należy przyjąć Bonasol roztwór doustny, przed przyjęciem jakiegokolwiek posiłku, napoju lub innego leku.
- Wypij całą zawartość jednej butelki, a następnie co najmniej 30 ml (jedna szósta szklanki) wody z kranu.Można wypić więcej wody z kranu.
- Nie popijać wodą mineralną (niegazowaną lub gazowaną), kawą, herbatą, sokiem owocowym ani mlekiem.
- Nie kładź się, ale trzymaj tułów w pozycji pionowej (siedząc, stojąc lub chodząc) przez co najmniej 30 minut po przyjęciu roztworu. Nie kładź się, dopóki nie zjesz pierwszego posiłku w ciągu dnia.
- Nie należy przyjmować roztworu doustnego Bonasol przed snem ani przed porannym wstaniem z łóżka.
- Jeśli wystąpią trudności lub ból podczas przełykania, nowy początek bólu w klatce piersiowej lub zgaga lub nasilenie istniejącej zgagi, należy porozmawiać z lekarzem.
- Po przyjęciu roztworu doustnego Bonasol należy odczekać co najmniej 30 minut przed przyjęciem pierwszego posiłku, napoju lub pierwszego leku danego dnia, w tym leków zobojętniających, suplementów wapnia i witamin. Roztwór doustny Bonasol jest skuteczny tylko na pusty żołądek.
Pominięcie przyjęcia leku Bonasol roztwór doustny
Jeśli zapomnisz przyjąć dawkę, zażyj ją rano następnego dnia po pominięciu.Nie przyjmuj dwóch dawek tego samego dnia. Wznów przyjmowanie cotygodniowej dawki w wybranym dniu, zgodnie z harmonogramem początkowym.
Przerwanie stosowania leku Bonasol roztwór doustny
Ważne jest, aby kontynuować przyjmowanie roztworu doustnego Bonasol tak długo, jak zaleci to lekarz. Roztwór doustny Bonasol może leczyć osteoporozę tylko wtedy, gdy pacjent nadal przyjmuje lek.
W przypadku dalszych pytań dotyczących stosowania tego leku należy zwrócić się do lekarza lub farmaceuty.
Przedawkowanie Co zrobić w przypadku przyjęcia zbyt dużej dawki leku Bonasol
W przypadku omyłkowego przyjęcia zbyt dużej ilości roztworu, należy wypić szklankę mleka i natychmiast skontaktować się z lekarzem. Nie wywoływać wymiotów i nie kłaść się.
Skutki uboczne Jakie są skutki uboczne Bonasol
Jak każdy lek, roztwór doustny Bonasol może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Do opisu częstotliwości zgłaszanych działań niepożądanych stosuje się następujące terminy:
Bardzo często (występujące u co najmniej 1 na 10 leczonych pacjentów)
- Często (występujące u więcej niż 1 na 100 i mniej niż 1 na 10 leczonych pacjentów)
- Niezbyt często (występujące u więcej niż 1 na 1000 i mniej niż 1 na 100 leczonych pacjentów)
- Rzadko (występujące u więcej niż 1 na 10 000 i mniej niż 1 na 1000 leczonych pacjentów)
- Bardzo rzadko (występujące u mniej niż 10 000 leczonych pacjentów)
Pospolity:
- zgaga; trudności lub ból w przełykaniu; wrzody przełyku (kanał między jamą ustną a żołądkiem), które mogą powodować ból w klatce piersiowej, pieczenie lub trudności lub ból w przełykaniu
- ból kości, mięśni i/lub stawów
- ból brzucha; dyskomfort w żołądku lub odbijanie po posiłkach; zaparcie; uczucie pełności lub wzdęcia w żołądku; biegunka; bębnica;
- bół głowy
- zaburzenia smaku
Niezwykły:
- mdłości; On wymiotował
- podrażnienie lub zapalenie przełyku (kanał między jamą ustną a żołądkiem)
- taborety ciemne lub smoliste
- wysypka; swędzenie; zaczerwienienie skóry
- łysienie
Rzadki:
- reakcje alergiczne, takie jak pokrzywka; obrzęk twarzy, warg, języka i (lub) gardła, który może powodować trudności w oddychaniu lub połykaniu
- objawy niskiego poziomu wapnia w surowicy, takie jak skurcze lub skurcze mięśni i / lub mrowienie w palcach lub wokół ust
- wrzody żołądka lub trawienne (czasami ciężkie lub z towarzyszącym krwawieniem)
- zwężenie przełyku (kanał między jamą ustną a żołądkiem)
- problemy ze szczęką związane z opóźnionym gojeniem i infekcją, często po „wyrwaniu zęba”.
- niewyraźne widzenie, ból oka lub zaczerwienienie
- wysypka nasilona przez światło
- silny ból kości, mięśni i (lub) stawów
- owrzodzenia w jamie ustnej po żuciu lub ssaniu tabletek
- przejściowe objawy grypopodobne, takie jak ból mięśni, ogólne złe samopoczucie, czasami z towarzyszącą gorączką, szczególnie na początku leczenia
Bardzo rzadkie:
- ciężkie reakcje skórne
Po wprowadzeniu produktu do obrotu zgłaszano następujące działania niepożądane (częstość nieznana):
- zawroty głowy
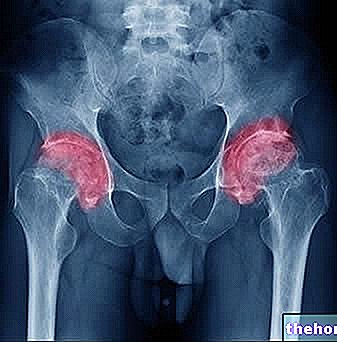
- obrzęk stawów, złamanie biodra u pacjentów leczonych alendronianem przez dłuższy czas Ból biodra, osłabienie lub uczucie dyskomfortu mogą być wczesnymi objawami możliwego złamania biodra.
- zmęczenie, obrzęk rąk lub nóg
Badania laboratoryjne:
Bardzo często: Łagodne i przemijające zmniejszenie stężenia wapnia i fosforanów w surowicy, zwykle w normalnym zakresie.
Rzadko może wystąpić nietypowe złamanie kości udowej, szczególnie u pacjentów długotrwale leczonych z powodu osteoporozy. W przypadku odczuwania bólu, osłabienia lub dyskomfortu w obrębie uda, biodra lub pachwiny należy skontaktować się z lekarzem, ponieważ może to być wczesnym wskazaniem możliwego złamanie kości udowej.
Natychmiast zgłoś te lub inne nietypowe objawy swojemu lekarzowi lub farmaceucie. Przydatne może być zanotowanie manifestowanego objawu, kiedy wystąpił i czas jego trwania.
Jeśli którykolwiek z objawów niepożądanych nasili się lub wystąpią jakiekolwiek objawy niepożądane niewymienione w tej ulotce, należy poinformować o tym lekarza lub farmaceutę.
Wygaśnięcie i przechowywanie
Przechowywać w miejscu niedostępnym i niewidocznym dla dzieci.
Nie stosować roztworu doustnego Bonasol po upływie terminu ważności zamieszczonego na pudełku i butelce. Termin ważności odnosi się do ostatniego dnia miesiąca.
Przechowywać w temperaturze poniżej 25 ° C
Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa, co pomoże chronić środowisko.
Termin ">Inne informacje
Co zawiera roztwór doustny Bonasol
Aktywna zasada
Substancją czynną jest trójwodny alendronian sodu. Każde 100 ml roztworu zawiera 70 mg kwasu alendronianowego w postaci trójwodnego alendronianu sodu.
Substancje pomocnicze
- guma ksantanowa (E415),
- cyklaminian sodu (E952),
- sukraloza (E955),
- Żółcień pomarańczowa FCF (E110),
- Parahydroksybenzoesan metylu (E218),
- Parahydroksybenzoesan propylu (E216)
- Aromat pomarańczowy zawierający etanol i butylohydroksyanizol,
- Woda oczyszczona.
Jak wygląda roztwór doustny Bonasol i co zawiera opakowanie
Bonasol 70 mg roztwór doustny jest roztworem o barwie pomarańczowej.
Jest dostępny w przezroczystych butelkach z politereftalanu etylenu (PET) z zamknięciem zabezpieczającym przed manipulacją w opakowaniach po 1, 2, 4 i 12 butelek.
Każda butelka zawiera 100 ml roztworu i jest przeznaczona wyłącznie do jednorazowego użytku.
Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
Ulotka pakietu źródłowego: AIFA (Włoska Agencja Leków). Treść opublikowana w styczniu 2016 r. Przedstawione informacje mogą być nieaktualne.
Aby mieć dostęp do najbardziej aktualnej wersji, warto wejść na stronę AIFA (Włoskiej Agencji Leków). Zastrzeżenie i przydatne informacje.
01.0 NAZWA PRODUKTU LECZNICZEGO -
BONASOL 70 MG TYGODNIOWY ROZTWÓR DOUSTNY
02.0 SKŁAD JAKOŚCIOWY I ILOŚCIOWY -
Każda pojedyncza dawka 100 ml zawiera 70 mg alendronianu (w postaci 91,35 mg trójwodnego alendronianu sodu).
Substancje pomocnicze:
Każda dawka (100 ml) zawiera 80 mg parahydroksybenzoesanu metylu (E218), 20 mg parahydroksybenzoesanu propylu (E216) i 6 mg żółcieni pomarańczowej (E110).
Pełny wykaz substancji pomocniczych, patrz punkt 6.1
03.0 POSTAĆ FARMACEUTYCZNA -
Rozwiązanie doustne.
Pomarańczowy opalizujący roztwór.
04.0 INFORMACJE KLINICZNE -
04.1 Wskazania terapeutyczne -
Leczenie osteoporozy u kobiet po menopauzie.
Alendronian zmniejsza ryzyko złamań kręgów i biodra.
04.2 Dawkowanie i sposób podawania -
Dawkowanie
Do podawania doustnego.
Zalecana dawka to jedna dawka jednostkowa 70 mg (100 ml) raz w tygodniu.
Nie ustalono optymalnego czasu trwania leczenia bisfosfonianami osteoporozy.Konieczność kontynuacji leczenia powinna być okresowo oceniana u każdego pacjenta z osobna w oparciu o korzyści i potencjalne ryzyko związane z leczeniem osteoporozy. Bonasol 70 mg roztwór doustny raz w tygodniu, szczególnie po 5 lub więcej latach użytkowania.
Sposób podawania
Aby umożliwić odpowiednią absorpcję alendronianu.
Bonasol 70 mg co tydzień roztwór doustny należy go przyjąć co najmniej 30 minut przed spożyciem jakiegokolwiek posiłku, napoju lub leku danego dnia, w towarzystwie wyłącznie wody z kranu. Inne napoje (w tym woda mineralna), pokarmy i leki prawdopodobnie zmniejszają wchłanianie alendronianu (patrz punkt 4.5).
Ułatwienie przejścia przez żołądek, zmniejszając w ten sposób możliwość miejscowego i przełykowego podrażnienia oraz wszelkich działań niepożądanych (patrz punkt 4.4)
• Pacjenci nie powinni kłaść się, dopóki nie zjedzą czegoś, co powinno nastąpić co najmniej 30 minut po przyjęciu roztworu.
• Pacjenci nie powinni kłaść się przez co najmniej 30 minut po zażyciu Bonasol 70 mg co tydzień roztwór doustny.
• Bonasol 70 mg co tydzień roztwór doustny należy go połykać tylko rano, wstając z łóżka, jako pojedynczą dawkę 100 ml (cała zawartość fiolki), a następnie co najmniej 30 ml wody z kranu. Dozwolone jest pobranie większej ilości wody z kranu.
• Bonasol 70 mg co tydzień roztwór doustny nie należy go przyjmować przed snem ani przed wstaniem z łóżka rano.
Pacjenci powinni przyjmować suplementy wapnia i witaminy D, jeśli ich dieta jest niewystarczająca (patrz punkt 4.4).
Stosowanie u pacjentów w podeszłym wieku: Badania kliniczne nie wykazały żadnych związanych z wiekiem różnic w profilach skuteczności lub bezpieczeństwa alendronianu, dlatego nie ma konieczności dostosowania dawki u pacjentów w podeszłym wieku.
Stosować w przypadku uszkodzenia nerek: Nie ma konieczności dostosowania dawkowania u pacjentów ze współczynnikiem przesączania kłębuszkowego (GFR) większym niż 35 ml/min. Nie zaleca się podawania alendronianu pacjentom z zaburzeniami czynności nerek, gdy GFR wynosi poniżej 35 ml/min ze względu na brak doświadczenia w tym zakresie.
Stosowanie u dzieci i młodzieży: Nie zaleca się stosowania alendronianu u dzieci i młodzieży w wieku poniżej 18 lat ze względu na niewystarczające dane dotyczące bezpieczeństwa i skuteczności w stanach związanych z osteoporozą u dzieci (patrz również punkt 5.1).
Alendronian nie był badany w leczeniu osteoporozy wywołanej glikokortykosteroidami.
04.3 Przeciwwskazania -
• Choroby przełyku i inne czynniki, które opóźniają opróżnianie przełyku, takie jak zwężenie i achalazja
• Niezdolność do stania lub siedzenia prosto przez co najmniej 30 minut
• Nadwrażliwość na alendronian lub którąkolwiek z jego substancji pomocniczych
• Hipokalcemia
• Pacjenci, którzy mają trudności z połykaniem płynów
• Pacjenci zagrożeni aspiracją
Patrz również punkt 4.4 „Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania”.
04.4 Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania -
Działania niepożądane wpływające na górny odcinek przewodu pokarmowego
Cotygodniowy roztwór doustny Bonasol może powodować miejscowe podrażnienie błony śluzowej górnego odcinka przewodu pokarmowego. Ponieważ istnieje możliwość zaostrzenia choroby podstawowej, należy zachować ostrożność podając Bonasol raz w tygodniu pacjentom z problemami górnego odcinka przewodu pokarmowego, takimi jak dysfagia, choroba przełyku, zapalenie żołądka, dwunastnicy lub wrzody, lub pacjentom, którzy przebyli niedawno rok) poważnej choroby przewodu pokarmowego, takiej jak choroba wrzodowa lub czynne krwawienie z przewodu pokarmowego, lub po przebytym zabiegu chirurgicznym górnego odcinka przewodu pokarmowego (z wyjątkiem pyloplastyki) (patrz punkt 4.3). alendronian indywidualnie.
U pacjentów przyjmujących alendronian zgłaszano reakcje przełyku (czasami ciężkie i wymagające hospitalizacji), takie jak zapalenie przełyku, wrzody i nadżerki przełyku, po których rzadko następuje zwężenie przełyku. Dlatego lekarz powinien zwrócić szczególną uwagę na pojawienie się jakichkolwiek oznak lub objawów wskazujących na możliwą reakcję przełyku i zalecić pacjentowi przerwanie leczenia alendronianem i zwrócenie się o pomoc lekarską w przypadku wystąpienia objawów podrażnienia przełyku, takich jak dysfagia. ból zamostkowy lub nowa lub nasilająca się zgaga.
Ryzyko poważnych działań niepożądanych dotyczących przełyku jest większe u pacjentów, którzy nie przyjmują alendronianu prawidłowo i (lub) kontynuują przyjmowanie alendronianu po wystąpieniu objawów sugerujących podrażnienie przełyku. Bardzo ważne jest, aby pacjent był dobrze zaznajomiony i rozumiany, jak przyjmować produkt leczniczy (patrz punkt 4.2 „Dawkowanie i sposób podawania"). Pacjentów należy pouczyć, że nieprzestrzeganie tych instrukcji może zwiększyć ryzyko problemów z przełykiem.
Chociaż w dużych badaniach klinicznych nie zaobserwowano zwiększonego ryzyka, zgłaszano rzadkie (po wprowadzeniu produktu do obrotu) przypadki wrzodów żołądka i dwunastnicy, niektóre ciężkie i związane z powikłaniami.
Martwica kości żuchwy/szczęki
Przypadki martwicy kości szczęki, zwykle związane z ekstrakcją zęba i (lub) miejscowym zakażeniem (w tym zapaleniem kości i szpiku), obserwowano u pacjentów z nowotworem leczonych według schematów terapeutycznych obejmujących bisfosfoniany podawane głównie dożylnie. Wielu z tych pacjentów było również leczonych chemioterapią i kortykosteroidami. Zgłaszano również martwicę kości szczęki u pacjentów z osteoporozą leczonych doustnymi bisfosfonianami.
Podczas oceny indywidualnego ryzyka rozwoju martwicy kości szczęki należy wziąć pod uwagę następujące czynniki ryzyka:
• siła działania bisfosfonianu (maksymalna dla kwasu zoledronowego), droga podania (patrz powyżej) i dawka skumulowana
• nowotwory, chemioterapia, radioterapia, kortykosteroidy, palenie
• historia chorób zębów, złej higieny jamy ustnej, chorób przyzębia, inwazyjnych zabiegów stomatologicznych i źle dopasowanych protez
Przed rozpoczęciem leczenia bisfosfonianami doustnymi u pacjentów o złym stanie uzębienia należy rozważyć badanie stomatologiczne z odpowiednimi profilaktycznymi zabiegami stomatologicznymi.
W trakcie leczenia pacjenci ci powinni w jak największym stopniu unikać inwazyjnych zabiegów stomatologicznych. U pacjentów, u których podczas terapii bisfosfonianami rozwinie się martwica kości szczęki, chirurgia stomatologiczna może pogorszyć ich stan. W przypadku pacjentów wymagających zabiegu stomatologicznego brak jest danych sugerujących, że przerwanie leczenia bisfosfonianami może zmniejszyć ryzyko wystąpienia martwicy kości szczęki.Ocena kliniczna lekarza powinna kierować programem postępowania każdego pacjenta.na podstawie indywidualnej oceny ryzyka/ stosunek korzyści.
W trakcie leczenia bisfosfonianami należy zachęcać wszystkich pacjentów do dbania o higienę jamy ustnej, poddawania się okresowym przeglądom stomatologicznym i zgłaszania wszelkich objawów w obrębie jamy ustnej, takich jak ruchomość, ból czy obrzęk zębów.
Ból mięśniowo-szkieletowy
U pacjentów leczonych bisfosfonianami zgłaszano ból kości, stawów i mięśni. Po wprowadzeniu produktu do obrotu objawy te rzadko były ciężkie i (lub) prowadziły do niesprawności (patrz punkt „4.8). Czas do wystąpienia objawów wahał się od jednego dnia do kilku miesięcy po rozpoczęciu leczenia.Większość pacjentów zgłaszała złagodzenie objawów po odstawieniu leku.Podgrupa pacjentów doświadczyła nawrotu objawów po odstawieniu tego samego leku lub innego bisfosfonianu.
Nietypowe złamania kości udowej
Zgłaszano nietypowe złamania podkrętarzowe i trzonu kości udowej, głównie u pacjentów długotrwale leczonych bisfosfonianami z powodu osteoporozy.Te krótkie złamania poprzeczne lub skośne mogą wystąpić w dowolnym miejscu kości udowej, od miejsca tuż poniżej krętarza mniejszego do powyżej linii nadkłykciowej. występują samoistnie lub po minimalnym urazie, a niektórzy pacjenci odczuwają ból uda lub pachwiny, często związany z wynikami badań obrazowych i radiograficznymi objawami złamań przeciążeniowych, na tygodnie lub miesiące przed wystąpieniem złamań przeciążeniowych. Złamania są często dwustronne; dlatego u pacjentów leczonych bisfosfonianami, u których doszło do złamania trzonu kości udowej, należy zbadać drugą kość udową. Odnotowano również ograniczone gojenie się tych złamań. U pacjentów z podejrzeniem atypowego złamania kości udowej należy rozważyć przerwanie leczenia bisfosfonianami do czasu oceny pacjenta na podstawie indywidualnego stosunku korzyści do ryzyka.
Podczas leczenia bisfosfonianami należy doradzić pacjentom, aby zgłaszali wszelkie bóle w obrębie uda, biodra lub pachwiny, a każdego pacjenta wykazującego takie objawy należy zbadać pod kątem niecałkowitego złamania kości udowej.
Reakcje skórne
Po wprowadzeniu produktu do obrotu zgłaszano rzadkie przypadki ciężkich reakcji skórnych, w tym zespół Stevensa Johnsona i toksyczne martwicze oddzielanie się naskórka.
Pominięta dawka
Pacjentów należy poinformować, że w przypadku pominięcia dawki: Bonasol 70 mg roztwór doustny, powinni przyjąć pojedynczą dawkę jednostkową (100 ml) rano po dniu, w którym zdadzą sobie sprawę, że zapomnieli. Nie powinni przyjmować dwóch dawek tego samego dnia, ale powinni wznowić przyjmowanie pojedynczej dawki jednostkowej na tydzień, jak pierwotnie zaplanowano na wybrany dzień.
Uszkodzenie nerek
Nie zaleca się stosowania alendronianu u pacjentów z zaburzeniami czynności nerek z GFR poniżej 35 ml/min (patrz punkt 4.2).
Metabolizm kostny i mineralny
Oprócz niedoboru estrogenów i wieku należy wziąć pod uwagę inne przyczyny osteoporozy.
Hipokalcemię należy wyrównać przed rozpoczęciem leczenia alendronianem (patrz punkt 4.3) Należy również skutecznie leczyć inne zaburzenia metabolizmu minerałów (takie jak niedobór witaminy D i niedoczynność przytarczyc). Pacjentów z tymi stanami klinicznymi należy monitorować. hipokalcemia podczas cotygodniowego leczenia preparatem Bonasol.
Ze względu na pozytywny wpływ alendronianu na zwiększenie mineralizacji kości, może wystąpić zmniejszenie stężenia wapnia i fosforanów w surowicy, szczególnie u pacjentów przyjmujących glikokortykosteroidy, u których wchłanianie wapnia może być zmniejszone. Zazwyczaj redukcje te są skromne i bezobjawowe. Istnieją jednak rzadkie doniesienia o objawowej hipokalcemii, czasami ciężkiej, które występowały u osób z predysponującymi stanami (takimi jak niedoczynność przytarczyc, niedobór witaminy D i zaburzenia wchłaniania wapnia). Szczególnie ważne jest zapewnienie odpowiedniej podaży wapnia i witaminy D u pacjentów leczonych glikokortykosteroidami.
Substancje pomocnicze
Ten produkt leczniczy zawiera 0,15% objętości w etanolu (alkoholu), tj. do 115 mg na dawkę, co odpowiada 3 ml piwa lub 1,3 ml wina na dawkę. Jest szkodliwy dla alkoholików. Należy o tym pamiętać w przypadku grup wysokiego ryzyka, takich jak pacjenci cierpiący na choroby wątroby lub epilepsję.
Bonasol 70 mg co tydzień roztwór doustny zawiera barwnik żółcień pomarańczową (E110), parahydroksybenzoesan metylu (E218) i parahydroksybenzoesan propylu (E216), które mogą powodować reakcje alergiczne.
04.5 Interakcje z innymi produktami leczniczymi i inne formy interakcji -
W przypadku jednoczesnego przyjmowania pokarmów i napojów (w tym wody mineralnej), suplementów wapnia, środków zobojętniających sok żołądkowy i innych leków podawanych doustnie prawdopodobnie zaburzają wchłanianie alendronianu, dlatego pacjenci powinni odczekać co najmniej 30 minut przed przyjęciem alendronianu. doustne przyjmowanie jakiegokolwiek innego produktu leczniczego (patrz punkty 4.2 i 5.2).
Nie można przewidzieć innych interakcji z produktami leczniczymi o znaczeniu klinicznym. W badaniach klinicznych niektórzy pacjenci otrzymywali estrogen (dopochwowo, przezskórnie lub doustnie) podczas otrzymywania alendronianu. Nie zaobserwowano działań niepożądanych związanych z jednoczesnym stosowaniem tych leków.
Ponieważ stosowanie NLPZ wiąże się z podrażnieniem przewodu pokarmowego, należy zachować szczególną ostrożność, gdy te produkty lecznicze są przyjmowane jednocześnie z alendronianem.
Chociaż nie przeprowadzono specyficznych badań interakcji, alendronian był stosowany w badaniach klinicznych w połączeniu z szeroką gamą powszechnie stosowanych produktów leczniczych, nie dając dowodów na klinicznie istotne działania niepożądane.
04.6 Ciąża i karmienie piersią -
Ciąża
Brak lub ograniczone dane dotyczące stosowania alendronianu u kobiet w ciąży. Badania na zwierzętach wykazały szkodliwy wpływ na reprodukcję. Alendronian podawany ciężarnym samicom szczurów powodował dystocję związaną z hipokalcemią u matek (patrz punkt 5.3).
Bonasol 70mg Weekly Oral Solution nie powinien być stosowany w okresie ciąży.
Czas karmienia
Nie wiadomo, czy alendronian przenika do mleka ludzkiego u ludzi.Nie można wykluczyć zagrożenia dla noworodka/dziecka. Alendronianu nie należy stosować u kobiet karmiących piersią.
Płodność
Bisfosfoniany są wbudowywane w macierz kostną, z której są stopniowo uwalniane na przestrzeni lat. Ilość bisfosfonianów wbudowywanych do kości dorosłych, a zatem ilość dostępna do uwolnienia do krążenia ogólnego, jest bezpośrednio związana z dawką i czasem stosowania bisfosfonianów (patrz punkt 5.2).Brak danych dotyczących ryzyka dla płodu u ludzi. Istnieje jednak teoretyczne ryzyko uszkodzenia płodu, głównie układu kostnego, jeśli kobieta zajdzie w ciążę po ukończeniu kuracji bisfosfonianami. Nie badano wpływu na ryzyko takich zmiennych, jak czas od zaprzestania leczenia bisfosfonianami do poczęcia, rodzaj zastosowanego bisfosfonianu i droga podania (dożylna lub doustna).
04.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn -
Alendronian nie ma wpływu lub ma nieistotny wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn, jednak niektóre działania niepożądane zgłaszane podczas stosowania alendronianu mogą wpływać na zdolność niektórych pacjentów do prowadzenia pojazdów i obsługiwania maszyn. Indywidualne reakcje na cotygodniowy roztwór doustny Bonasol mogą być różne (patrz punkt 4.8).
04.8 Działania niepożądane -
W rocznym badaniu z udziałem kobiet po menopauzie z osteoporozą, ogólny profil bezpieczeństwa alendronianu w tabletkach podawanych co tydzień (n = 519) i alendronianu 10 mg/dobę (n = 370) był podobny.
W dwóch trzyletnich badaniach o praktycznie identycznym projekcie u kobiet po menopauzie (alendronian 10 mg: n = 196; placebo: n = 397), ogólne profile bezpieczeństwa alendronianu 10 mg/dobę i placebo były podobne.
Zdarzenia niepożądane zgłaszane przez badaczy jako prawdopodobnie, prawdopodobnie lub zdecydowanie związane z lekiem przedstawiono w poniższej tabeli, gdy w badaniu rocznym wystąpiły u ≥ 1% w którejkolwiek grupie leczenia lub gdy w badaniach trzyletnich wystąpiły u ≥ 1% pacjentów leczonych alendronianem w dawce 10 mg/dobę i z większą częstością niż obserwowana u pacjentów otrzymujących placebo:
Podczas badań klinicznych i (lub) stosowania po wprowadzeniu do obrotu zgłaszano również następujące działania niepożądane:
Częstość występowania zdefiniowano w następujący sposób: [Bardzo często (≥1/10), Często (≥1/100,
Zaburzenia układu immunologicznego:
Rzadko: reakcje nadwrażliwości, w tym pokrzywka i obrzęk naczynioruchowy
Zaburzenia metabolizmu i odżywiania:
Rzadko: objawowa hipokalcemia, często związana ze stanami predysponującymi (patrz punkt 4.4)
Zaburzenia układu nerwowego:
Często: ból głowy, zawroty głowy †
Niezbyt często: zaburzenia smaku †
Zaburzenia oka:
Niezbyt często: zapalenie oka (zapalenie błony naczyniowej oka, zapalenie twardówki, zapalenie nadtwardówki)
Zaburzenia ucha i błędnika:
Często: zawroty głowy †
Zaburzenia żołądkowo-jelitowe:
Często: ból brzucha, niestrawność, zaparcia, biegunka, wzdęcia, owrzodzenie przełyku*, dysfagia*, wzdęcie brzucha, kwaśne odbijanie
Niezbyt często: nudności, wymioty, zapalenie żołądka, zapalenie przełyku*, nadżerki przełyku*, smoliste stolce †
Rzadko: zwężenie przełyku*, owrzodzenie części ustnej gardła*, perforacja, owrzodzenie, krwawienie z górnego odcinka przewodu pokarmowego (patrz punkt 4.4)
Zaburzenia skóry i tkanki podskórnej:
Często: łysienie †, świąd †
Niezbyt często: wysypka, rumień
Rzadko: Wysypka z nadwrażliwością na światło, ciężkie reakcje skórne, w tym zespół Stevensa-Johnsona i toksyczna nekroliza naskórka ‡
Zaburzenia układu mięśniowo-szkieletowego:
Bardzo często: bóle mięśniowo-szkieletowe (kości, mięśni lub stawów) † (patrz punkt 4.4)
Często: obrzęk stawów †
Rzadko: U pacjentów leczonych bisfosfonianami zgłaszano przypadki martwicy kości szczęki. Większość z tych doniesień dotyczy pacjentów onkologicznych, ale przypadki wystąpiły również u pacjentów leczonych z powodu osteoporozy. Zwykle martwica kości szczęki wiąże się z ekstrakcją zęba i / lub miejscową infekcją (w tym zapaleniem kości i szpiku). Rozpoznanie raka, chemioterapia, radioterapia, terapia kortykosteroidami i zła higiena jamy ustnej są również uważane za czynniki ryzyka; silny ból mięśniowo-szkieletowy (kości, mięśni lub stawów) (patrz punkt 4.4), atypowe złamania podkrętarzowe i trzonu kości udowej (działanie niepożądane klasy bisfosfonianów) || oraz złamania przeciążeniowe bliższego trzonu kości udowej (patrz punkt 4.4).
Zaburzenia ogólne i stany w miejscu podania:
Często: astenia †, obrzęki obwodowe †
Niezbyt często: objawy przemijające jak w przypadku odpowiedzi ostrej fazy (bóle mięśni, złe samopoczucie i rzadko gorączka), zazwyczaj związane z rozpoczęciem leczenia†.
† Częstość w badaniach klinicznych była podobna w obu grupach otrzymujących lek i placebo.
* Patrz rozdziały 4.2 i 4.4
‡ To działanie niepożądane zidentyfikowano podczas monitorowania po wprowadzeniu do obrotu. Częstość występowania „rzadkich” oszacowano na podstawie odpowiednich badań klinicznych.
|| Zgłoszone podczas doświadczeń po wprowadzeniu do obrotu.
Zgłaszanie podejrzewanych działań niepożądanych
Zgłaszanie podejrzewanych działań niepożądanych występujących po dopuszczeniu produktu leczniczego do obrotu jest ważne, ponieważ umożliwia ciągłe monitorowanie stosunku korzyści do ryzyka produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem krajowego systemu zgłaszania. .agenziafarmaco.gov.it/it/responsabili.
04.9 Przedawkowanie -
Objawy
Przedawkowanie doustne może prowadzić do hipokalcemii, hipofosfatemii i działań niepożądanych ze strony górnego odcinka przewodu pokarmowego, takich jak rozstrój żołądka, zgaga, zapalenie przełyku, zapalenie żołądka lub wrzody.
Leczenie
Brak konkretnych danych dotyczących leczenia przedawkowania alendronianu. W przypadku przedawkowania należy podać mleko lub leki zobojętniające wiążące się z alendronianem Ze względu na ryzyko podrażnienia przełyku nie należy wywoływać wymiotów, a pacjenta należy trzymać w pozycji pionowej.
05.0 WŁAŚCIWOŚCI FARMAKOLOGICZNE -
05.1 "Właściwości farmakodynamiczne -
Grupa farmakoterapeutyczna: produkty lecznicze stosowane w leczeniu chorób kości, bisfosfoniany.
Kod ATC: M05B A04.
Mechanizm akcji
Substancja czynna zawarta w tygodniowym roztworze doustnym Bonasol, alendronian (w postaci trójwodnego alendronianu), jest bisfosfonianem o działaniu przeciw osteoklastycznym, który nie ma bezpośredniego wpływu na tworzenie kości. Badania przedkliniczne wykazały, że alendronian jest preferencyjnie zlokalizowany w miejscach aktywnej resorpcji.Aktywność jest zahamowana, ale rekrutacja i adhezja osteoklastów nie ulega zmianie.Tkanka kostna utworzona podczas leczenia alendronianem jest jakościowo normalna.
Skuteczność kliniczna i bezpieczeństwo
Leczenie osteoporozy pomenopauzalnej
Osteoporozę definiuje się jako BMD kręgosłupa lub biodra, które jest o 2,5 SD mniejsze niż średnia wartość w normalnej młodej populacji, lub jako historia wcześniejszego złamania osteoporotycznego, niezależnie od BMD.
Równoważność terapeutyczna alendronianu 70 mg raz w tygodniu (n = 519) i alendronianu 10 mg / dobę (n = 370) wykazano w rocznym wieloośrodkowym badaniu kobiet po menopauzie z osteoporozą. wartości początkowe wynosiły 5,1% (95% CI: 4,8, 5,4%) w grupie 70 mg raz w tygodniu i 5,4% (95% CI: 5,0, 5,8%) w grupie 10 mg dziennie Średni wzrost BMD wyniósł 2,3% i 2,9% na szyjce kości udowej i 2,9% i 3,1% na biodrze odpowiednio w grupach 70 mg raz na tydzień i 10 mg raz na dobę. Obie grupy były również podobne pod względem wzrostu wartości DMO w innych okręgach kostnych.
Wpływ alendronianu na masę kostną i częstość złamań u kobiet po menopauzie badano w dwóch wstępnych badaniach skuteczności o identycznym projekcie (n = 994) oraz w Fracture Intervention Trial (FIT: n = 6459).
We wstępnych badaniach skuteczności średnie zwiększenie gęstości mineralnej kości (BMD) po podaniu alendronianu w dawce 10 mg/dobę w porównaniu z placebo po trzech latach wyniosło 8,8%, 5,9% i 7,8%.% w kręgosłupie, szyjce kości udowej i krętarzu. . BMD całego organizmu również znacząco wzrosło.48% zmniejszenie (alendronian 3,2% vs placebo 6,2%) zaobserwowano w liczbie pacjentów leczonych alendronianem, z jednym lub więcej złamaniami kręgów w porównaniu z pacjentami, którzy otrzymywali placebo.
W ciągu dwuletniego przedłużenia tych badań BMD nadal rosło w kręgosłupie i krętarzu oraz pozostawała stabilna w szyjce kości udowej i całym ciele.
FIT składał się z dwóch kontrolowanych placebo badań z użyciem alendronianu (5 mg dziennie przez dwa lata i 10 mg dziennie przez dodatkowy rok lub dwa):
• FIT 1: Trzyletnie badanie z udziałem 2027 pacjentów, którzy mieli co najmniej jedno złamanie kręgu (kompresyjne) na początku badania. W tym badaniu alendronian podawany codziennie zmniejszył częstość występowania ≥ 1 nowego złamania kręgu o 47% (alendronian 7,9% w porównaniu z placebo 15,0%).Ponadto zaobserwowano statystycznie istotne zmniejszenie częstości złamań szyjki kości udowej (1,1% vs 2,2%, redukcja o 51%).
• FIT 2: czteroletnie badanie 4432 pacjentów z niską masą kostną, ale bez złamań kręgów na początku badania. W tym badaniu zaobserwowano istotną różnicę w analizie podgrup kobiet z osteoporozą (37% całej badanej populacji, z osteoporozą zdefiniowaną powyżej) pod względem częstości występowania złamań szyjki kości udowej (alendronian 1,0% vs placebo 2,2%, zmniejszenie o 56 %) oraz w częstości występowania ≥ 1 złamania kręgu (2,9% vs 5,8%, redukcja o 50%).
Dane laboratoryjne
W badaniach klinicznych zgłoszono bezobjawowe, łagodne i przemijające zmniejszenie stężenia wapnia i fosforanów w surowicy odpowiednio u około 18% i 10% pacjentów otrzymujących alendronian w dawce 10 mg/dobę, w porównaniu z około 12% i 3% pacjentów otrzymujących placebo. . Jednak częstość występowania redukcji wapnia w surowicy do
Populacja pediatryczna
Alendronian badano u niewielkiej liczby pacjentów w wieku poniżej 18 lat z wrodzoną łamliwością kości.Wyniki są niewystarczające, aby uzasadnić stosowanie alendronianu u dzieci z wrodzoną łamliwością kości.
05.2 "Właściwości farmakokinetyczne -
Wchłanianie
W porównaniu z referencyjną dawką dożylną, średnia biodostępność alendronianu po podaniu doustnym u kobiet wynosiła 0,64% dla dawek od 5 do 70 mg podawanych po całonocnym poszczeniu i na dwie godziny przed standardowym śniadaniem.Podobnie biodostępność zmniejszyła się do około 0,46% i 0,39% po podaniu alendronianu jedną godzinę lub pół przed standardowym śniadaniem. W badaniach dotyczących osteoporozy alendronian był skuteczny, gdy był podawany co najmniej 30 minut przed pierwszym posiłkiem lub napojem w ciągu dnia.
Biodostępność była znikoma, gdy alendronian był podawany z lub w ciągu dwóch godzin od standardowego śniadania.Jednoczesne podawanie alendronianu i kawy lub soku pomarańczowego zmniejszyło jego biodostępność o około 60%.
U zdrowych osób prednizon podawany doustnie (20 mg 3 razy na dobę przez pięć dni) nie powodował klinicznie istotnych zmian w biodostępności alendronianu po podaniu doustnym (średni wzrost o 20% do 44%).
Dystrybucja
Badania na szczurach wykazały, że po dożylnym podaniu 1 mg/kg alendronian początkowo dystrybuowany do tkanek miękkich, ulega szybkiej redystrybucji do kości lub jest wydalany z moczem. ma co najmniej 28 litrów.
Stężenia produktu leczniczego w osoczu po podaniu doustnych dawek terapeutycznych są zbyt niskie, aby można je było wykryć analitycznie (białko osocza wynosi około 78%.
Biotransformacja
Zarówno u ludzi, jak iu zwierząt nie ma dowodów na to, że alendronian jest metabolizowany.
Eliminacja
Po podaniu pojedynczej dawki dożylnej alendronianu znakowanego [14C] około 50% wchłoniętej radioaktywności zostało wydalone z moczem w ciągu 72 godzin, aw kale wykryto niewielką lub żadną radioaktywność. Po podaniu pojedynczej dawki dożylnej 10 mg, klirens nerkowy alendronianu wynosił 71 ml/min, a klirens ogólnoustrojowy nie przekraczał 200 ml/min.Stężenie w osoczu spadło o ponad 95% w ciągu sześciu godzin od podania dożylnego. okres półtrwania u ludzi oszacowano na ponad dziesięć lat, co odzwierciedla uwalnianie alendronianu ze szkieletu.
U szczurów wydalanie alendronianu przez nerki nie zachodzi poprzez układy transportu kwasowo-zasadowego, dlatego nie oczekuje się, że na tym poziomie u ludzi będzie on zakłócał eliminację innych produktów leczniczych.
Uszkodzenie nerek
Badania przedkliniczne wykazują, że produkt leczniczy, który nie osiada w kościach, jest szybko wydalany z moczem.U zwierząt po długotrwałym podawaniu dawek skumulowanych do 35 mg/kg nie stwierdzono nasycenia wychwytu przez dostępnych, jest prawdopodobne, że, podobnie jak u zwierząt, wydalanie alendronianu przez nerki może być zmniejszone u pacjentów z zaburzeniami czynności nerek.W związku z tym można spodziewać się nieco większej akumulacji alendronianu w kościach na poziomie kości u pacjentów z zaburzeniami czynności nerek ( patrz punkt 4.2 „Dawkowanie i sposób podawania”).
05.3 Przedkliniczne dane o bezpieczeństwie -
Dane niekliniczne wynikające z konwencjonalnych badań farmakologicznych dotyczących bezpieczeństwa, toksyczności po podaniu wielokrotnym, genotoksyczności i potencjalnego działania rakotwórczego nie ujawniają żadnego szczególnego zagrożenia dla ludzi.Badania na szczurach wykazały, że leczenie alendronianem w czasie ciąży wiąże się z dystocją związaną z hipokalcemią u matek podczas porodu. W badaniach u szczurów, którym podawano największe dawki, częstość występowania niepełnego skostnienia płodu była częstsza. Znaczenie tych obserwacji dla ludzi nie jest znane.
06.0 INFORMACJE FARMACEUTYCZNE -
06.1 Substancje pomocnicze -
guma ksantanowa (E415),
cyklaminian sodu (E952),
sukraloza (E955),
żółcień pomarańczowa FCF (E110),
parahydroksybenzoesan metylu (E218),
parahydroksybenzoesan propylu (E216),
aromat pomarańczowy zawierający etanol i butylohydroksyanizol,
woda oczyszczona.
06.2 Niezgodność "-
Nieistotne.
06.3 Okres ważności "-
2 lata.
06.4 Specjalne środki ostrożności przy przechowywaniu -
Przechowywać w temperaturze poniżej 25°C.
06.5 Rodzaj opakowania bezpośredniego i zawartość opakowania -
Przezroczysta butelka z politereftalanu etylenu (PET) z zamknięciem zabezpieczającym przed manipulacją, z wkładką z polietylenu o niskiej gęstości, w opakowaniach po 1,2, 4 i 12 butelek. Każda butelka zawiera 100 ml roztworu.
Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
06.6 Instrukcje użytkowania i obsługi -
Wyłącznie do jednorazowego użytku.
Brak specjalnych instrukcji dotyczących utylizacji.
07.0 POSIADACZ „POZWOLENIA NA DOPUSZCZENIE DO OBROTU” -
Bruno Farmaceutici S.p.A.
Via delle Ande, 15
00144 Rzym
08.0 NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU -
BONASOL 70 mg roztwór doustny - 1 butelka PET: 040622019
BONASOL 70 mg roztwór doustny - 2 butelki PET: 040622021
BONASOL 70 mg roztwór doustny - 4 butelki PET: 040622033
BONASOL 70 mg roztwór doustny - 12 butelek PET: 040622045
09.0 DATA PIERWSZEGO ZEZWOLENIA LUB PRZEDŁUŻENIA ZEZWOLENIA -
26 sierpnia 2011
10.0 DATA ZMIAN TEKSTU -
Lipiec 2016