Składniki aktywne: Azelastine (chlorowodorek azelastyny), Fluticasone (propionian flutykazonu)
Dymista 137 mikrogramów / 50 mikrogramów na dawkę
Wskazania Dlaczego stosuje się Dymista? Po co to jest?
Dymista zawiera dwa aktywne składniki: chlorowodorek azelastyny i propionian flutykazonu.
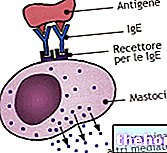
- Chlorowodorek azelastyny należy do grupy farmakoterapeutycznej leków przeciwhistaminowych. Leki przeciwhistaminowe działają poprzez blokowanie działania substancji takich jak histamina, które organizm wytwarza w wyniku reakcji alergicznej, zmniejszając tym samym objawy alergicznego nieżytu nosa.
- Propionian flutykazonu należy do grupy farmakoterapeutycznej kortykosteroidów, które zmniejszają stan zapalny.
Dymista jest stosowana w celu łagodzenia objawów umiarkowanego do ciężkiego sezonowego i całorocznego alergicznego nieżytu nosa, gdy stosowanie samego leku przeciwhistaminowego lub samego kortykosteroidu donosowego nie jest wystarczające.
Sezonowy lub całoroczny alergiczny nieżyt nosa to reakcje alergiczne na substancje takie jak pyłki (katar sienny), roztocza, pleśń, kurz lub zwierzęta domowe.
Dymista łagodzi objawy alergii, takie jak nadmierna produkcja śluzu z nosa, katar, kichanie, swędzenie nosa czy zatkany nos.
Przeciwwskazania Kiedy nie należy stosować Dymisty
Nie używaj Dymisty:
- jeśli pacjent ma uczulenie na chlorowodorek azelastyny lub propionian flutykazonu lub którykolwiek z pozostałych składników tego leku (wymienionych w punkcie 6).
Środki ostrożności dotyczące stosowania Informacje ważne przed zastosowaniem leku Dymista
Przed rozpoczęciem stosowania leku Dymista należy omówić to z lekarzem lub farmaceutą:
- jeśli niedawno miałaś operację nosa
- jeśli kiedykolwiek wystąpiła „zakażenie nosa”. Zakażenia dróg oddechowych należy leczyć lekami przeciwbakteryjnymi lub przeciwgrzybiczymi. Jeśli pacjent otrzymał lek na „zakażenie nosa”, można nadal stosować lek Dymista w leczeniu alergii
- jeśli u pacjenta występuje gruźlica lub „nieleczona infekcja”
- jeśli pacjent miał zaburzenia widzenia lub miał w przeszłości podwyższone ciśnienie w oku, jaskrę i (lub) zaćmę. Jeśli te warunki dotyczą Ciebie, będziesz ściśle monitorowany podczas korzystania z Dymista
- jeśli u pacjenta występują zaburzenia czynności nadnerczy. Należy zachować szczególną ostrożność podczas zmiany leczenia kortykosteroidami ogólnoustrojowymi na lek Dymista
- jeśli u pacjenta występuje ciężka choroba wątroby. Twoje ryzyko wystąpienia ogólnoustrojowych skutków ubocznych jest wyższe.
W takich przypadkach lekarz zdecyduje, czy możesz stosować Dymista, czy nie.
Ważne jest, aby przyjmować dawkę zgodnie ze wskazaniami w punkcie 3 poniżej lub zgodnie z zaleceniami lekarza. Leczenie większymi niż zalecane dawkami wziewnych kortykosteroidów może powodować zahamowanie czynności kory nadnerczy, co może powodować utratę masy ciała, zmęczenie, osłabienie mięśni, niski poziom cukru we krwi, pragnienie słonych pokarmów, bóle stawów, depresję i ciemne zabarwienie skóry. Jeśli takie stany wystąpią, lekarz może zalecić inny lek w sytuacjach stresowych lub w przypadku planowego zabiegu chirurgicznego.
Aby uniknąć zahamowania czynności kory nadnerczy, lekarz zaleci najmniejszą dawkę, która może skutecznie kontrolować objawy nieżytu nosa.
Przyjmowane przez długi czas glikokortykosteroidy wziewne (takie jak Dymista) mogą powodować spowolnienie wzrostu u dzieci i młodzieży. Lekarz będzie regularnie sprawdzał wzrost dziecka i upewniał się, że przyjmuje najmniejszą możliwą skuteczną dawkę.
Jeśli nie masz pewności, czy którykolwiek z powyższych stanów dotyczy Ciebie, przed zastosowaniem leku Dymista porozmawiaj ze swoim lekarzem lub farmaceutą. Dzieci Nie zaleca się stosowania tego leku u dzieci w wieku poniżej 12 lat.
Interakcje Jakie leki lub pokarmy mogą modyfikować działanie leku Dymista
Należy powiedzieć lekarzowi lub farmaceucie, jeśli pacjent przyjmuje, ostatnio przyjmował lub może przyjmować jakiekolwiek inne leki.
Zapytaj swojego lekarza lub farmaceutę o poradę:
- jeśli pacjent przyjmuje leki stosowane w leczeniu wirusa HIV, takie jak Ritonavir
- jeśli pacjent przyjmuje leki stosowane w leczeniu zakażeń grzybiczych, takie jak ketokonazol.
Ostrzeżenia Ważne jest, aby wiedzieć, że:
Ciąża i karmienie piersią
Jeśli pacjentka jest w ciąży lub karmi piersią, podejrzewa, że może być w ciąży lub planuje mieć dziecko, powinna poradzić się lekarza lub farmaceuty przed zastosowaniem leku Dymista.
Prowadzenie i używanie maszyn
Dymista ma znikomy wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn. Bardzo rzadko może wystąpić zmęczenie lub zawroty głowy, zarówno z powodu samej choroby, jak i stosowania leku Dymista.W takich przypadkach należy unikać prowadzenia pojazdów lub obsługiwania maszyn.Należy mieć świadomość, że spożywanie alkoholu może nasilać te objawy.
Dymista zawiera chlorek benzalkoniowy
Może powodować podrażnienie błony śluzowej nosa i skurcz oskrzeli. Poproś lekarza lub farmaceutę o poradę, jeśli źle się poczujesz podczas stosowania sprayu
Dawka, sposób i czas podawania Jak stosować Dymista: dawkowanie
Lek Dymista należy zawsze stosować zgodnie z zaleceniami lekarza. W razie wątpliwości skonsultuj się z lekarzem lub farmaceutą.
Niezbędne jest regularne stosowanie Dymisty, aby osiągnąć pełne korzyści terapeutyczne.
Unikać kontaktu z oczami.
Dorośli i młodzież (od 12 roku życia)
- Zalecana dawka to jedno „dmuchnięcie do każdego nozdrza rano i wieczorem.
Stosowanie u dzieci poniżej 12 roku życia
- Nie zaleca się stosowania tego leku u dzieci w wieku poniżej 12 lat.
Stosowanie u pacjentów z niewydolnością nerek i wątroby
- Brak danych dotyczących pacjentów z niewydolnością nerek i wątroby.
Sposób podawania
Do inhalacji.
Przeczytaj informacje zawarte w tej ulotce i postępuj zgodnie z instrukcjami.
INSTRUKCJA UŻYCIA
Przygotowanie sprayu
- Delikatnie potrząsaj fiolką przez 5 sekund, przechylając ją w dół i w górę, a następnie zdejmij nasadkę ochronną (patrz Rycina 1).
- Przy pierwszym użyciu aerozolu do nosa należy zalać pompkę, rozpylając produkt w powietrzu.
- Załaduj pompkę, umieszczając dwa palce po obu stronach pompki rozpylającej i połóż kciuk na podstawie fiolki.
- Naciśnij i zwolnij pompkę 6 razy, aż pojawi się drobna mgiełka (patrz rysunek 2).
- Pompa jest teraz naładowana i gotowa do użycia.
- Jeśli aerozol do nosa nie był używany przez ponad 7 dni, należy ponownie napełnić pompkę, naciskając i zwalniając pompkę.
Stosowanie sprayu
- Delikatnie potrząsać fiolką przez około 5 sekund, przechylając ją w dół i w górę, a następnie zdjąć nasadkę ochronną (patrz rysunek 1)
- Wydmuchaj nos, aby oczyścić nozdrza.
- Trzymaj głowę pochyloną w dół w kierunku stóp. Nie odchylaj głowy do tyłu.
- Trzymaj fiolkę pionowo i delikatnie włóż końcówkę rozpylającą do jednego nozdrza.
- Zamknij drugie nozdrze jednym palcem, naciśnij szybko jeden raz i jednocześnie wykonaj delikatny wdech (patrz Rysunek 3).
- Oddychaj ustami.
- Powtórz tę samą procedurę dla drugiego nozdrza.
- Wykonać delikatny wdech, nie odchylając głowy do tyłu po wydaniu, aby zapobiec przedostaniu się leku do gardła i nieprzyjemnemu smakowi (patrz rysunek 4).
- Po każdym użyciu wytrzyj końcówkę sprayu do sucha ręcznikiem papierowym lub czystą szmatką, a następnie załóż z powrotem nasadkę ochronną.
Ważne jest, aby przyjmować dawkę zgodnie z zaleceniami lekarza. Używaj tylko ilości zalecanej przez lekarza.
Czas trwania leczenia
Dymista przeznaczona jest do długotrwałego użytkowania. Czas trwania leczenia musi odpowiadać okresowi, w którym występują objawy alergii.
Przedawkowanie Co zrobić w przypadku przyjęcia zbyt dużej dawki leku Dymista
Zastosowanie większej niż zalecana dawki Dymisty
Jeśli wstrzykniesz zbyt dużo tego leku do nosa, prawdopodobnie nie będziesz mieć żadnych problemów. Jeśli jesteś zaniepokojony lub jeśli przez dłuższy czas stosowałeś dawki wyższe niż zalecane, skontaktuj się z lekarzem. W przypadku przypadkowego połknięcia Dymisty, zwłaszcza przez dziecko, należy jak najszybciej skontaktować się z lekarzem lub najbliższym szpitalnym oddziałem ratunkowym.
Pominięcie zastosowania Dymisty
Użyj aerozolu do nosa, gdy tylko sobie o tym przypomnisz, a następną dawkę zażyj jak zwykle. Nie należy stosować dawki podwójnej w celu uzupełnienia pominiętej dawki.
Przerwanie stosowania leku Dymista
Nie należy przerywać stosowania Dymisty bez konsultacji z lekarzem, ponieważ zagraża to powodzeniu leczenia.
W przypadku dalszych pytań dotyczących stosowania tego leku należy zwrócić się do lekarza lub farmaceuty.
Skutki uboczne Jakie są skutki uboczne Dymisty?
Jak każdy lek, Dymista może powodować działania niepożądane, chociaż nie u każdego one wystąpią.
Bardzo częste działania niepożądane (mogą wystąpić u więcej niż 1 na 10 pacjentów):
- krwotok z nosa
Częste działania niepożądane (mogą wystąpić u 1 na 10 pacjentów):
- bół głowy
- gorzki smak w ustach, zwłaszcza jeśli odchylasz głowę do tyłu podczas używania aerozolu do nosa. Powinno szybko zniknąć, jeśli popijesz napój bezalkoholowy przez kilka minut po zastosowaniu tego leku
- nieprzyjemny zapach
Niezbyt częste działania niepożądane (mogą wystąpić u 1 na 100 osób):
- lekkie podrażnienie wnętrza nosa, może powodować lekkie pieczenie, swędzenie lub kichanie
- suchość nosa, kaszel, suchość gardła lub podrażnienie gardła
Rzadkie działania niepożądane (mogą wystąpić u 1 na 1000 osób):
- suchość w ustach
Bardzo rzadkie działania niepożądane (mogą wystąpić nie częściej niż u 1 na 10 000 pacjentów):
- zawroty głowy lub senność
- zaćma, jaskra lub zwiększone ciśnienie w oku, powodujące utratę wzroku i (lub) zaczerwienienie i ból oczu. Te działania niepożądane zgłaszano po długotrwałym leczeniu flutykazonu propionianem w aerozolu do nosa.
- uszkodzenie skóry i błony śluzowej nosa
- uczucie mdłości, zmęczenia, zmęczenia lub osłabienia
- wysypka, swędząca lub zaczerwieniona skóra, wypukłe swędzące guzki
- skurcz oskrzeli (zwężenie dróg oddechowych w płucach)
Natychmiast uzyskaj pomoc medyczną, jeśli zauważysz którykolwiek z następujących objawów:
- obrzęk twarzy, warg, języka lub gardła, który może powodować trudności w połykaniu/oddychaniu i nagły początek wysypki skórnej. Mogą to być objawy ciężkiej reakcji alergicznej. Uwaga: taka ewentualność jest bardzo rzadka.
Ogólnoustrojowe działania niepożądane (działania niepożądane dotyczące całego organizmu) mogą wystąpić, gdy lek ten jest stosowany w dużych dawkach przez długi czas.Działania te mogą się różnić u poszczególnych pacjentów i pomiędzy różnymi preparatami kortykosteroidów (patrz punkt 2) Działania te są znacznie mniej prawdopodobne. wystąpią w przypadku stosowania kortykosteroidów w aerozolu do nosa niż w przypadku przyjmowania kortykosteroidów doustnie. Kortykosteroidy stosowane do nosa mogą wpływać na normalne wytwarzanie hormonów w organizmie, szczególnie w przypadku stosowania dużych dawek przez długi czas.U dzieci i młodzieży to działanie niepożądane może powodować spowolnienie wzrostu.
W rzadkich przypadkach podczas długotrwałego podawania wziewnych glikokortykosteroidów obserwowano zmniejszenie gęstości kości (osteoporozę).
Zgłaszanie skutków ubocznych
Jeśli wystąpią jakiekolwiek objawy niepożądane, w tym wszelkie możliwe działania niepożądane niewymienione w tej ulotce, należy porozmawiać z lekarzem lub farmaceutą. Działania niepożądane można również zgłaszać bezpośrednio za pośrednictwem krajowego systemu zgłaszania pod adresem www.agenziafarmaco.gov.it/it/responsabili Zgłaszanie działań niepożądanych może pomóc w uzyskaniu większej ilości informacji na temat bezpieczeństwa stosowania tego leku.
Wygaśnięcie i przechowywanie
Lek należy przechowywać w miejscu niewidocznym i niedostępnym dla dzieci. Nie stosować tego leku po upływie terminu ważności zamieszczonego na etykiecie fiolki i pudełku po „EXP”.Termin ważności oznacza ostatni dzień podanego miesiąca.
Nie przechowywać w lodówce ani nie zamrażać.
Okres ważności po pierwszym otwarciu: Wyrzucić niewykorzystany lek po 6 miesiącach od pierwszego otwarcia aerozolu do nosa.
Nie należy wyrzucać żadnych leków do kanalizacji ani domowych pojemników na odpadki. Należy zapytać farmaceutę, jak usunąć leki, których się już nie używa.Pomoże to chronić środowisko.
Skład i postać farmaceutyczna
Co zawiera Dymista
Substancjami czynnymi są: chlorowodorek azelastyny i propionian flutykazonu.
Każdy gram zawiesiny zawiera 1000 mikrogramów chlorowodorku azelastyny i 365 mikrogramów propionianu flutykazonu.
Każde rozpylenie (0,14 g) dostarcza 137 mikrogramów chlorowodorku azelastyny (= 125 mikrogramów azelastyny) i 50 mikrogramów propionianu flutykazonu.
Pozostałe składniki to: wersenian disodowy, glicerol, celuloza mikrokrystaliczna, karmeloza sodowa, polisorbat 80, roztwór chlorku benzalkoniowego, alkohol fenyloetylowy i woda oczyszczona.
Opis wyglądu Dymisty i zawartości opakowania
Dymista jest białą, jednorodną zawiesiną.
Dymista jest dostępny w fiolce z bursztynowego szkła, wyposażonej w pompkę rozpylającą, aplikator i nasadkę ochronną.
Fiolka 10 ml zawiera 6,4 g zawiesiny aerozolu do nosa (co najmniej 28 rozpyleń). Fiolka 25 ml zawiera 23 g zawiesiny aerozolu do nosa (co najmniej 120 rozpyleń).
Dymista pojawia się w:
opakowania zawierające 1 fiolkę z 6,4 g aerozolu do nosa, zawiesina
opakowania zawierające 1 fiolkę z 23 g aerozolu do nosa, zawiesina
opakowania zbiorcze zawierające 10 fiolek, z których każda zawiera 6,4 g aerozolu do nosa, zawiesina
opakowania zbiorcze zawierające 3 fiolki, z których każda zawiera 23 g aerozolu do nosa, zawiesina
Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
Ulotka pakietu źródłowego: AIFA (Włoska Agencja Leków). Treść opublikowana w styczniu 2016 r. Przedstawione informacje mogą być nieaktualne.
Aby mieć dostęp do najbardziej aktualnej wersji, warto wejść na stronę AIFA (Włoskiej Agencji Leków). Zastrzeżenie i przydatne informacje.
01.0 NAZWA PRODUKTU LECZNICZEGO
DYMISTA 137 MCG / 50 MCG DO DOZOWANIA SPRAYU DO NOSA, ZAWIESZENIA
02.0 SKŁAD JAKOŚCIOWY I ILOŚCIOWY
Każdy gram zawiesiny zawiera 1000 mcg chlorowodorku azelastyny i 365 mcg propionianu flutykazonu.
Jedna dostawa (0,14 g) zawiera 137 mcg chlorowodorku azelastyny (= 125 mcg azelastyny) i 50 mcg propionianu flutykazonu.
Substancje pomocnicze o znanym działaniu:
dawka dostarczona do jednorazowej aplikacji (0,14 g) zawiera 0,014 mg chlorku benzalkoniowego.
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
03.0 POSTAĆ FARMACEUTYCZNA
Aerozol do nosa, zawiesina.
Biała, jednorodna zawiesina.
04.0 INFORMACJE KLINICZNE
04.1 Wskazania terapeutyczne
Łagodzenie objawów umiarkowanego do ciężkiego sezonowego i całorocznego alergicznego nieżytu nosa, gdy monoterapia donosowymi lekami przeciwhistaminowymi lub glikokortykosteroidami nie jest uważana za wystarczającą.
04.2 Dawkowanie i sposób podawania
Dawkowanie
Aby osiągnąć pełne korzyści terapeutyczne, niezbędne jest regularne stosowanie.
Unikać kontaktu z oczami.
Dorośli i młodzież (od 12 roku życia)
Jedna „dostawa do każdego nozdrza dwa razy dziennie (rano i wieczorem).
Dzieci poniżej 12 roku życia
Nie zaleca się stosowania preparatu Dymista u dzieci w wieku poniżej 12 lat, ponieważ bezpieczeństwo i skuteczność w tej populacji pacjentów nie zostały jeszcze ustalone.
Starsi mieszkańcy
W tej populacji pacjentów nie jest wymagana modyfikacja dawki.
Niewydolność nerek i wątroby
Brak danych dotyczących pacjentów z niewydolnością nerek i wątroby.
Czas trwania leczenia
Dymista przeznaczona jest do długotrwałego użytkowania.
Czas trwania leczenia musi odpowiadać okresowi ekspozycji na alergeny.
Sposób podawania
Dymista jest przeznaczona wyłącznie do inhalacji.
Instrukcja użycia
Przygotowanie sprayu:
Fiolkę należy delikatnie potrząsać przez około 5 sekund, przechylając ją w dół i w górę, a następnie zdjąć nasadkę ochronną.Przed pierwszym użyciem Dymisty należy sześciokrotnie nacisnąć i zwolnić pompkę.Jeżeli Dymista nie była używana dłużej niż 7 dni, pompę należy ponownie naładować, naciskając ją i zwalniając.
Stosowanie sprayu:
Fiolkę należy delikatnie potrząsać przez około 5 sekund, przechylając ją w dół i w górę, a następnie zdjąć nasadkę ochronną.
Po wydmuchaniu nosa rozpyl zawiesinę raz do każdego nozdrza, trzymając głowę pochyloną w dół. Po użyciu należy osuszyć końcówkę sprayu i ponownie założyć nasadkę ochronną.
04.3 Przeciwwskazania
Nadwrażliwość na substancje czynne lub na którąkolwiek substancję pomocniczą wymienioną w punkcie 6.1.
04.4 Specjalne ostrzeżenia i odpowiednie środki ostrożności dotyczące stosowania
U pacjentów, którym podawano flutykazonu propionian i rytonawir, zgłaszano klinicznie istotne interakcje lekowe, powodujące ogólnoustrojowe działanie kortykosteroidów, takie jak zespół Cushinga i zahamowanie czynności kory nadnerczy. W związku z tym należy unikać jednoczesnego podawania propionianu flutykazonu i rytonawiru, chyba że potencjalne korzyści dla pacjenta przewyższają ryzyko ogólnoustrojowych działań niepożądanych kortykosteroidów (patrz punkt 4.5).
Działanie ogólnoustrojowe wziewnych kortykosteroidów może wystąpić, zwłaszcza gdy są one przepisywane w dużych dawkach przez dłuższy czas. Mogą one różnić się u poszczególnych pacjentów i między różnymi preparatami kortykosteroidowymi, ale ich występowanie jest znacznie mniej prawdopodobne niż kortykosteroidów doustnych. Potencjalne działania ogólnoustrojowe mogą obejmować zespół Cushinga, cechy Cushinga, zahamowanie czynności kory nadnerczy, opóźnienie wzrostu u dzieci i młodzieży, zaćmę, jaskrę i rzadziej szereg skutków psychologicznych lub behawioralnych, w tym nadpobudliwość psychoruchową, zaburzenia snu, lęk, depresję lub agresję (szczególnie u dzieci).
Dymista podlega intensywnemu metabolizmowi pierwszego przejścia, dlatego ogólnoustrojowa ekspozycja na donosowe propionian flutykazonu prawdopodobnie zwiększy się u pacjentów z ciężką chorobą wątroby.Stan ten może skutkować zwiększoną częstością występowania ogólnoustrojowych działań niepożądanych.
Dlatego zaleca się ostrożność w leczeniu tych pacjentów.
Leczenie większymi niż zalecane dawkami wziewnych kortykosteroidów może skutkować klinicznie istotną supresją czynności kory nadnerczy. W przypadku konieczności zastosowania dawek wyższych niż zalecane, należy rozważyć dodatkowe pokrycie kortykosteroidami ogólnoustrojowymi, w sytuacjach stresowych lub planowanych zabiegach chirurgicznych.
Ogólnie, dawkę flutykazonu podawanego donosowo należy zmniejszyć do najmniejszej dawki, która może skutecznie kontrolować objawy nieżytu nosa. Nie badano dawek większych niż zalecane (patrz punkt 4.2) z produktem Dymista. Podobnie jak w przypadku wszystkich kortykosteroidów podawanych donosowo, należy rozważyć całkowite ogólnoustrojowe obciążenie kortykosteroidami, ilekroć przepisywane są inne, współistniejące formy leczenia kortykosteroidami.
U dzieci leczonych kortykosteroidami wziewnymi w zatwierdzonych dawkach zgłaszano opóźnienie wzrostu. Ponieważ wzrost występuje również u młodzieży, zaleca się regularne monitorowanie młodzieży otrzymującej długotrwałą terapię wziewnymi kortykosteroidami. W przypadku spowolnienia wzrostu należy zweryfikować terapię w celu, jeśli to możliwe, zmniejszenia dawki do najniższego poziomu, który może skutecznie kontrolować objawy.
Uważne monitorowanie jest wymagane u pacjentów z zaburzeniami widzenia lub z wywiadem podwyższonego ciśnienia ocznego, jaskry i (lub) zaćmy.
Jeśli istnieją jakiekolwiek powody, by sądzić, że czynność nadnerczy jest upośledzona, należy zachować ostrożność podczas zmiany leczenia steroidami ogólnoustrojowymi na Dymista.
U pacjentów z gruźlicą, jakimkolwiek nieleczonym zakażeniem, którzy niedawno przeszli operację lub niedawno przebyli uraz nosa lub jamy ustnej, należy rozważyć możliwe korzyści z leczenia produktem Dymista w porównaniu z możliwym ryzykiem.
Infekcje dróg oddechowych nosa należy leczyć terapią przeciwbakteryjną lub przeciwgrzybiczą, ale nie stanowią one swoistego przeciwwskazania do leczenia produktem Dymista.
Dymista zawiera chlorek benzalkoniowy, który może powodować podrażnienie błony śluzowej nosa i skurcz oskrzeli.
04.5 Interakcje z innymi produktami leczniczymi i inne formy interakcji
Propionian flutykazonu
W normalnych warunkach po podaniu donosowym propionianu flutykazonu w osoczu osiągane są niskie stężenia z powodu intensywnego metabolizmu pierwszego przejścia i wysokiego luz układowy, cytochrom P450 3A4 mediowany w jelicie i wątrobie Klinicznie istotne interakcje z lekami mediowane propionianem flutykazonu są zatem mało prawdopodobne.
Badanie interakcji leków przeprowadzone na zdrowych ochotnikach wykazało, że rytonawir (silny inhibitor cytochromu P450 3A4) może znacząco zwiększać stężenie propionianu flutykazonu w osoczu, powodując znaczne zmniejszenie stężenia kortyzolu w surowicy. rytonawir i propionian flutykazonu podawane donosowo lub wziewnie, co powoduje ogólnoustrojowe działanie kortykosteroidów, takie jak zespół Cushinga i zahamowanie czynności kory nadnerczy.W związku z tym należy unikać jednoczesnego podawania propionianu flutykazonu i rytonawiru, chyba że potencjalne korzyści dla pacjenta nie przewyższają ryzyka wpływ kortykosteroidów.
Badania wykazały, że inne inhibitory cytochromu P450 3A4 powodują nieistotny (erytromycyna) i niewielki (ketokonazol) wzrost ekspozycji ogólnoustrojowej na propionian flutykazonu, bez znaczącego zmniejszenia stężenia kortyzolu w surowicy.Jednakże podczas równoczesnego podawania zaleca się ostrożność. P450 3A4 (np. ketokonazol), ponieważ istnieje potencjalne ryzyko zwiększonej ogólnoustrojowej ekspozycji na propionian flutykazonu.
Chlorowodorek azelastyny
Nie przeprowadzono specjalnych badań dotyczących interakcji z aerozolem do nosa chlorowodorkiem azelastyny. Przeprowadzono badania interakcji między dawkami doustny wysoka. Jednakże nie mają one znaczenia dla aerozolu do nosa z azelastyną, ponieważ zalecane dawki wziewne powodują znacznie mniejsze „narażenie ogólnoustrojowe. Należy jednak zachować ostrożność podczas podawania chlorowodorku azelastyny pacjentom przyjmującym jednocześnie leki uspokajające lub leki na ośrodkowy układ nerwowy, ponieważ działanie uspokajające może być wzmocnione. Alkohol może również nasilać ten efekt (patrz punkt 4.7).
04.6 Ciąża i laktacja
Płodność
Istnieje ograniczona ilość danych dotyczących płodności (patrz punkt 5.3).
Ciąża
Brak danych lub istnieją ograniczone dane dotyczące stosowania azelastyny chlorowodorku i propionianu flutykazonu u kobiet w ciąży, dlatego produkt Dymista należy stosować w okresie ciąży tylko wtedy, gdy potencjalne korzyści uzasadniają potencjalne ryzyko dla płodu (patrz punkt 5.3).
Czas karmienia
Nie wiadomo, czy chlorowodorek azelastyny, propionian flutykazonu lub ich metabolity przenikają do mleka kobiecego po podaniu wziewnym. Produkt Dymista należy stosować w okresie karmienia piersią tylko wtedy, gdy potencjalna korzyść uzasadnia potencjalne ryzyko dla noworodka/niemowlęcia (patrz punkt 5.3).
04.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn
Dymista ma znikomy wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn.
W pojedynczych przypadkach podczas stosowania leku Dymista może wystąpić zmęczenie, zmęczenie, wyczerpanie, zawroty głowy lub osłabienie, również spowodowane samą chorobą.W takich przypadkach może dojść do upośledzenia zdolności prowadzenia pojazdów i obsługiwania maszyn.Alkohol może nasilać to działanie.
04.8 Działania niepożądane
Zwykle po podaniu mogą wystąpić zaburzenia smaku, charakterystyczny dla leku nieprzyjemny smak (często z powodu niewłaściwego sposobu aplikacji, tj. zbytniego odchylenia głowy do tyłu podczas podawania).
Działania niepożądane według klasyfikacji układów i narządów oraz częstości są wymienione poniżej. Częstotliwości definiuje się w następujący sposób:
Bardzo często (≥1/10)
Często (≥1/100,
Niezbyt często (≥1/1000 do
Rzadko (≥1/10 000,
Bardzo rzadkie (
Nieznana (częstość nie może być określona na podstawie dostępnych danych)
* Po długotrwałym leczeniu donosowym propionianem flutykazonu zidentyfikowano bardzo niewielką liczbę zgłoszeń spontanicznych.
** Po zastosowaniu donosowych kortykosteroidów zgłaszano perforację przegrody nosowej.
Działanie ogólnoustrojowe niektórych wziewnych kortykosteroidów może wystąpić, zwłaszcza gdy są one przepisywane w dużych dawkach przez dłuższy czas (patrz punkt 4.4).
U dzieci leczonych kortykosteroidami wziewnymi zgłaszano opóźnienie wzrostu. Opóźnienie wzrostu jest również możliwe u młodzieży (patrz punkt 4.4).
W rzadkich przypadkach obserwowano osteoporozę, gdy glikokortykosteroidy wziewne były podawane przez dłuższy czas.
04.9 Przedawkowanie
Nie przewiduje się reakcji przedawkowania w przypadku donosowej drogi podania.
Brak danych pacjentów dotyczących skutków ostrego lub przewlekłego przedawkowania donosowego propionianu flutykazonu.
Donosowe podanie 2 miligramów propionianu flutykazonu (10-krotność zalecanej dawki dobowej), dwa razy na dobę przez siedem dni zdrowym ochotnikom, nie miało wpływu na czynność osi podwzgórze-przysadka-nadnercza (HPA).
Podawanie dawek wyższych niż zalecane przez dłuższy czas może spowodować czasowe zahamowanie czynności nadnerczy.
U tych pacjentów leczenie produktem Dymista należy kontynuować w dawce wystarczającej do opanowania objawów. Czynność nadnerczy zostanie wznowiona po kilku dniach i można ją sprawdzić, mierząc poziom kortyzolu w osoczu.
W przypadku przedawkowania po przypadkowym przyjęciu doustnym, na podstawie wyników badań na zwierzętach możliwe jest wystąpienie zaburzeń ośrodkowego układu nerwowego wywołanych przez chlorowodorek azelastyny (w tym sen, splątanie, śpiączka, tachykardia i niedociśnienie).
Leczenie tych zaburzeń musi być objawowe. Zaleca się płukanie żołądka na podstawie ilości spożytej substancji.Nie jest znane antidotum.
05.0 WŁAŚCIWOŚCI FARMAKOLOGICZNE
05.1 Właściwości farmakodynamiczne
Grupa farmakoterapeutyczna: leki zmniejszające przekrwienie i inne preparaty do nosa do stosowania miejscowego, połączenia kortykosteroidów/flutykazonu.
Kod ATC: R01AD58.
Mechanizm działania i efekty farmakodynamiczne
Dymista zawiera chlorowodorek azelastyny i propionian flutykazonu, które mają różne mechanizmy działania i wykazują synergistyczne działanie w zakresie łagodzenia objawów alergicznego nieżytu nosa i nieżytu nosa i spojówek.
Propionian flutykazonu
Propionian flutykazonu jest syntetycznym trójfluorowanym kortykosteroidem, który ma szczególnie wysokie powinowactwo do receptora glukokortykoidowego i ma silne działanie przeciwzapalne, 3-5 razy silniejsze niż deksametazon, na podstawie badań ekspresji genów i wiązania sklonowanych ludzkich receptorów glukokortykoidowych.
Chlorowodorek azelastyny
Azelastyna, pochodna ftalazynonu, jest klasyfikowana jako silny, długo działający środek przeciwalergiczny o selektywnym działaniu antagonistycznym na receptory H1 oraz właściwościach przeciwzapalnych i stabilizujących komórki tuczne. Dane uzyskane z badań in vivo (przedkliniczne) e in vitrowykazują, że azelastyna hamuje syntezę lub uwalnianie chemicznych mediatorów odpowiedzialnych za wczesne i późne reakcje alergiczne, takich jak leukotrieny, histamina, czynnik aktywujący płytki krwi (czynnik aktywujący płytki krwi - PAF) i serotoniny.
Złagodzenie objawów alergii nosa zaobserwowano w ciągu 15 minut od podania.
Dymista
W 4 badaniach klinicznych przeprowadzonych u dorosłych i młodzieży z alergicznym nieżytem nosa „podawanie leku Dymista do każdego otworu nosowego dwa razy na dobę znacząco zmniejszyło objawy ze strony nosa (w tym katar, przekrwienie błony śluzowej nosa, kichanie i swędzenie nosa) w porównaniu z placebo. chlorowodorek azelastyny i propionian flutykazonu raz Dymista znacząco zmniejszyła objawy oczne (w tym swędzenie, łzawienie i zaczerwienienie) i poprawiła jakość życia pacjenta (Kwestionariusz jakości życia nieżytu nosa i spojówek - RQLQ) we wszystkich 4 badaniach.
Znaczącą poprawę objawów (50% zmniejszenie nasilenia objawów ze strony nosa) osiągnięto stosując Dymista w znacznie krótszym czasie (3 lub więcej dni) niż dostępny w handlu aerozol do nosa z propionianem flutykazonu. Większa skuteczność preparatu Dymista w porównaniu z propionianem flutykazonu w aerozolu została utrzymana w trakcie pełnego rocznego badania u pacjentów z przewlekłym przewlekłym alergicznym zapaleniem błony śluzowej nosa i niealergicznym/naczynioruchowym zapaleniem błony śluzowej nosa.
05.2 Właściwości farmakokinetyczne
Wchłanianie
Po donosowym podaniu dwóch wdechów do nozdrza (548 μg chlorowodorku azelastyny i 200 μg flutikazonu) preparatu Dymista, średnie maksymalne stężenie w osoczu (± odchylenie standardowe) (Cmax) wynosiło 194,5 ± 74,4 pg / ml dla azelastyny i 10,3 ± 3,9 pg / mL dla propionianu flutykazonu, a pole pod krzywą (AUC) wynosiło 4217 ± 2618 pg / ml * godz. dla azelastyny i 97,7 ± 43,1 pg / ml * godz. dla flutykazonu Średni czas do osiągnięcia maksymalnego stężenia (tmax) po podaniu pojedynczej dawki wynosił 0,5 godziny dla azelastyny i 1,0 godziny dla flutikazonu.
Ekspozycja ogólnoustrojowa na flutikazon była zwiększona o 50% w przypadku produktu Dymista w porównaniu z komercyjnym aerozolem do nosa zawierającym flutikazon, Ekspozycja ogólnoustrojowa na azelastynę w przypadku produktu Dymista była równoważna z komercyjnym aerozolem do nosa zawierającym azelastynę. Nie było dowodów na interakcje farmakokinetyczne między chlorowodorkiem azelastyny a propionianem flutykazonu.
Dystrybucja
Propionian flutykazonu wykazuje dużą objętość dystrybucji w stan stabilny (około 318 litrów). Wiązanie z białkami osocza wynosi 91%.
Objętość dystrybucji azelastyny jest duża i wysoce sugeruje jej rozpowszechnienie w tkankach obwodowych. Wiązanie z białkami wynosi 80-90%. Oba leki mają również „szerokie okno terapeutyczne: dlatego jest mało prawdopodobne, aby rozwinęły się reakcje wypierania leku.
Biotransformacja
Propionian flutykazonu jest szybko usuwany z krążenia ogólnego, głównie w wyniku metabolizmu wątrobowego, przez enzym CYP3A4 cytochromu P450 do nieaktywnego metabolitu kwasu karboksylowego.Propionian flutykazonu podawany doustnie również podlega intensywnemu metabolizmowi pierwszego przejścia.Azelastyna jest metabolizowana. Nie.-desmetyloazelastyna poprzez różne izoenzymy CYP, głównie CYP3A4, CYP2D6 i CYP2C19.
Eliminacja
Szybkość eliminacji propionianu flutykazonu podawanego dożylnie jest liniowa w zakresie dawek od 250 do 1000 mikrogramów i charakteryzuje się luz podwyższone osocze (CL = 1,1 l / min). Maksymalne stężenie w osoczu zmniejsza się o około 98% w ciągu 3-4 godzin i tylko niskie stężenia w osoczu są związane z końcowym okresem półtrwania wynoszącym 7,8 godziny. luz nerkowy propionian flutykazonu jest znikomy (żółć.
Okresy półtrwania eliminacji z osocza po podaniu pojedynczej dawki azelastyny wynoszą około 20-25 godzin dla azelastyny i 45 godzin dla terapeutycznie czynnego metabolitu. Nie.-desmetyloazelastyna. Wydalanie następuje głównie z kałem.Przedłużone wydalanie niewielkich ilości dawki z kałem wskazuje na możliwość pewnego stopnia krążenia jelitowo-wątrobowego.
05.3 Przedkliniczne dane o bezpieczeństwie
Propionian flutykazonu
Wyniki ogólnych badań toksykologicznych są podobne do tych obserwowanych w przypadku innych glikokortykosteroidów i są związane z zaostrzoną aktywnością farmakologiczną. Jest mało prawdopodobne, aby wyniki te miały znaczenie dla ludzi, biorąc pod uwagę zalecane dawki wziewne, które skutkują minimalną ekspozycją ogólnoustrojową. Brak działania genotoksycznego flutykazonu Propionian obserwowano w konwencjonalnych testach genotoksyczności.Ponadto nie zgłoszono związanego z lekiem zwiększenia częstości występowania nowotworów w dwuletnich badaniach inhalacyjnych na szczurach i myszach.
W badaniach na zwierzętach wykazano, że glikokortykosteroidy wywołują wady rozwojowe, w tym rozszczep podniebienia i wewnątrzmaciczne opóźnienie wzrostu. Jest mało prawdopodobne, aby wyniki te miały znaczenie dla ludzi, biorąc pod uwagę zalecane dawki wziewne, które powodują minimalną ekspozycję ogólnoustrojową (patrz punkt 5.2).
Chlorowodorek azelastyny
Chlorowodorek azelastyny nie wykazywał żadnego działania uczulającego u świnek morskich. Azelastyna nie wykazała genotoksyczności w serii testów in vitro I in vivoani żadnego potencjału rakotwórczego u szczurów lub myszy. U samców i samic szczurów azelastyna podawana doustnie w dawkach większych niż 3 mg/kg/umierać powodował zależne od dawki zmniejszenie wskaźnika płodności. Podczas badań toksyczności przewlekłej nie wykryto żadnych zmian związanych z lekiem w narządach rozrodczych próbek płci męskiej lub żeńskiej; jednak działanie embriotoksyczne i teratogenne wystąpiło u szczurów, myszy i królików, jedynie w przypadku działania toksycznego na matkę. dawki (np. wady rozwojowe szkieletu obserwowano u szczurów i myszy przy dawkach 68,6 mg/kg/umierać).
Dymista
Badania toksyczności po podaniu wielokrotnym donosowym u szczurów przez okres do 90 dni i u psów przez 14 dni preparatu Dymista nie wykazały żadnych nowych działań niepożądanych w odniesieniu do poszczególnych składników.
06.0 INFORMACJE FARMACEUTYCZNE
06.1 Zaróbki
Wersenian disodowy
Glicerol
Celuloza mikrokrystaliczna
Karmeloza sodowa
Polisorbat 80
Roztwór chlorku benzalkonium
Alkohol fenyloetylowy
Woda oczyszczona
06.2 Niekompatybilność
Nieistotne.
06.3 Okres ważności
3 lata.
Okres ważności w użyciu (po pierwszym podaniu): 6 miesięcy.
06.4 Specjalne środki ostrożności przy przechowywaniu
Nie przechowywać w lodówce ani nie zamrażać.
06.5 Rodzaj opakowania bezpośredniego i zawartość opakowania
Fiolka ze szkła oranżowego typu I, wyposażona w pompkę rozpylającą, aplikator donosowy (dozownik) z polipropylenu i ochronną nasadkę przeciwpyłową, zawierająca zawiesinę 6,4 g (co najmniej 28 rozpyleń) i 23 g (co najmniej 120 wypłat).
Wielkości opakowań:
1 fiolka z zawiesiną 6,4 g w fiolkach po 10 ml (co najmniej 28 dawek), 1 fiolka z zawiesiną 23 g w fiolkach po 25 ml (co najmniej 120 dawek)
Opakowania zbiorcze zawierające 64 g (10 fiolek po 6,4 g) aerozolu do nosa, zawiesina, opakowania zbiorcze zawierające 69 g (3 fiolki po 23 g) aerozolu do nosa, zawiesina
Nie wszystkie rozmiary opakowań mogą być wprowadzone na rynek.
06.6 Instrukcje użytkowania i obsługi
Brak specjalnych instrukcji dotyczących utylizacji.
07.0 PODMIOT POZWOLENIA NA DOPUSZCZENIE DO OBROTU
Meda Pharma S.p.A.
Viale Brenta 18
20139 Mediolan
08.0 NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
041808015 - "137 mcg / 50 mcg / DOZOWANIE SPRAYU DO NOSA, ZAWIESZENIE" 1 SZKLANA BUTELKA Z 6,4 G / 28 DOZOWANIAMI
041808027 - "137 mcg / 50 mcg / DOZOWANIE SPRAYU DO NOSA, ZAWIESZENIE" 10 SZKLANYCH BUTELEK Z 6,4 G / 28 DOZOWANIAMI
041808039 - "137 mcg / 50 mcg / DOZOWANIE SPRAYU DO NOSA, ZAWIESZENIE" 1 SZKLANA BUTELKA Z DOZAMI 23 G / 120
041808041 - "137 mcg / 50 mcg / DOZOWANIE SPRAYU DO NOSA, ZAWIESZENIE" 3 SZKLANE BUTELKI Z DOZAMI 23 G / 120
09.0 DATA PIERWSZEGO ZEZWOLENIA LUB PRZEDŁUŻENIA ZEZWOLENIA
Data pierwszej autoryzacji: 27 maja 2013 r.
10.0 DATA ZMIAN TEKSTU
maj 2013